8-Hydroxynaphthalin-1,6-disulfonsäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 8-Hydroxynaphthalin-1,6-disulfonsäure | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C10H8O7S2 | ||||||||||||||||||
| Kurzbeschreibung |
roter Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 304,30 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt |
Verkohlt beim Erhitzen[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
8-Hydroxynaphthalin-1,6-disulfonsäure ist ein Zwischenprodukt zur Herstellung von Azofarbstoffen. Die Säure enthält die funktionellen Gruppen aromatischer (benzoider) Sulfonsäuren und eine phenolische Hydroxygruppe. Sie ist ein Derivat der Naphthalin-1,6-disulfonsäure und wird aus dieser hergestellt. Die 8-Hydroxynaphthalin-1,6-disulfonsäure wird auch als ε-Säure bezeichnet und ist ein Vertreter der Buchstabensäuren.
Geschichte
[Bearbeiten | Quelltext bearbeiten]Die Erforschung der Teerfarben im 19. Jahrhundert brachte u. a. Sulfonsäuren des Teerbestandteils Naphthalin hervor. Für die Derivate dieser Sulfonsäuren bürgerten sich zahlreiche Trivialnamen ein. Der Actiengesellschaft für Anilinfabrikation in Berlin, die Keimzelle der Firma AGFA, wurde im Jahr 1888 ein Deutsches Reichspatent erteilt; als Erfinder wurde M. Andresen genannt, offensichtlich Momme Andresen.[3] Die chemische Verbindung wurde daher auch als Andresen's Säure bezeichnet. Der Entdecker nannte sie ε-Säure (epsilon-Säure).
Herstellung
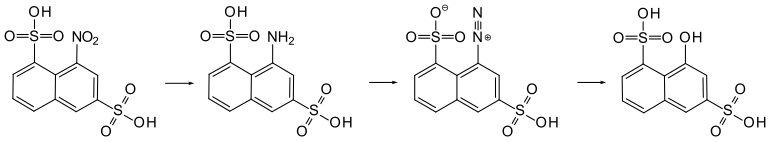
[Bearbeiten | Quelltext bearbeiten]Nach D.R.P. Nr. 45776 wird Naphthalin-1,6-disulfonsäure nitriert. Reduktion der Nitrogruppe liefert 8-Aminonaphthalin-1,6-disulfonsäure, die anschließend diazotiert wird. Die Diazoverbindung wird mit verdünnter Schwefelsäure erhitzt (Phenolverkochung), wodurch 8-Hydroxynaphthalin-1,6-disulfonsäure gebildet wird.[3] Das Verfahren wurde teilweise in einer Doktorarbeit an der ETH Zürich überprüft und optimiert.[2]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Die 8-Hydroxynaphthalin-1,6-disulfonsäure ist in Wasser leicht löslich. Konzentriert man die bei der Synthese anfallenden wässrigen Lösungen, so werden zuerst Hydrate gebildet. Reine Epsilonsäure bildet ein Pentahydrat und ein Trihydrat.[2] Wässrige Lösungen der Epsilonsäure und ihrer Salze fluoreszieren mit grüner Farbe.[2]
Von der 8-Hydroxynaphthalin-1,6-disulfonsäure sind zahlreiche neutrale und saure Salze bekannt, die zur Isolierung dienen, so mit Natrium, Kalium, Calcium. Auch diese liegen als Hydrate vor, enthalten also Kristallwasser. Die rohe Säure wurde durch Zusatz von Kreidepulver, d. h. Calciumcarbonat, als Calciumsalz isoliert ("Kalkung"). Zur Reinigung der Säure kann das Bariumsalz verwendet werden, welches mit Schwefelsäure behandelt wird. Schwerlösliches Bariumsulfat fällt aus, und die wässrige Lösung enthält die "freie" 8-Hydroxynaphthalin-1,6-disulfonsäure.[3]
Reaktionen
[Bearbeiten | Quelltext bearbeiten]Das Natriumsalz der Epsilonsäure reagiert mit Phosphorpentoxid zu einem Sulton. Dabei wird eine intramolekulare Esterbindung zwischen der 8-Hydroxygruppe und der Sulfonsäuregruppe in 1-Stellung gebildet. Anstelle von Phosphorpentoxid kann u. a. auch konzentrierte Schwefelsäure verwendet werden.[4] Die wichtigste Reaktion ist jedoch die Umsetzung mit Diazoniumsalzen zu Azofarbstoffen, welche am Kohlenstoffatom C-7 erfolgt.

Verwendung
[Bearbeiten | Quelltext bearbeiten]Durch Kupplung mit diazotiertem 4-Nitroanilin wird aus dem Naphtholderivat der Farbstoff Epsilonblau hergestellt.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d Datenblatt 8-Hydroxynaphthalin-1,6-disulfonsäure (PDF) bei BLD Pharmatech, Katalognummer: BD59740, abgerufen am 1. April 2022.
- ↑ a b c d Robert Felix Edelmann: Ueber die 1,4,8-, 2,4,8-, 1,3,8-, 1,4,7- und 2,4,7-Amino-Naphthalin-Disulfosäuren. 1925, doi:10.3929/ethz-a-000097131 (Dissertation, ETH Zürich).
- ↑ a b c M. Andresen, D.R.P Nr. 45776. Verfahren zur Darstellung einer neuen α-Naphtoldisulfosäure, Abdruck in: Paul Friedlaender, Fortschritte der Teerfarbenfabrikation und verwandter Industriezweige, Bd. II, S. 253 (1888)
- ↑ D.R.P. 55094A für B.A.S.F. vom 10. April 1889: Verfahren zur Ueberführung der Naphtoldisulfosäure des Patentes Nr. 45 776 in die Naphtosultonsulfosäure des Patentes Nr. 52724.
