Cumol
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
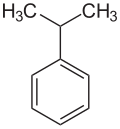
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Cumol | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C9H12 | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit scharfem, aromatischem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 120,19 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||
| Dichte |
0,86 g·cm−3 (20 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
152 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Brechungsindex |
1,49146 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Cumol ist eine organisch-chemische Verbindung aus der Stoffgruppe der aromatischen Kohlenwasserstoffe. Aufgrund der eleganten Überführung in Phenol und Aceton nach dem Hock-Verfahren und dessen großtechnischer Verbreitung in den fünfziger Jahren wurde es zu einem bedeutenden Zwischenprodukt der chemischen Industrie.
Geschichte
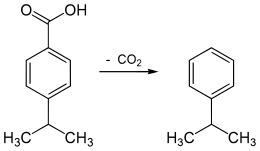
[Bearbeiten | Quelltext bearbeiten]Cumol wurde 1840 bei der Decarboxylierung von Cuminsäure entdeckt. Der erste Namensvorschlag der Entdecker war Cumen, sie verwendeten den ersten Wortbestandteil der Cuminsäure. Justus v. Liebig schlug dann den Namen Cumol vor, der fortan Eingang in die deutsche Literatur fand.[6]
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Die technisch ausschließlich genutzte Methode zur Herstellung von Cumol beruht auf der Friedel-Crafts-Alkylierung von Benzol mit Propen. Die Umsetzung erfolgt entweder in der Flüssig- oder Gasphase. Als Katalysatoren werden vorwiegend Lewis- oder Brønsted-Säuren sowie neuerdings auch saure Zeolithe eingesetzt.
Flüssigphase
[Bearbeiten | Quelltext bearbeiten]Im Flüssigphasenprozess setzt man Benzol mit Propen bei 35–40 °C und niedrigem Propendruck von etwa 7 bar in Gegenwart von Aluminiumchlorid (AlCl3) zu Cumol um.[7]

Außerdem ist ein Verfahren mit Fluorwasserstoff bei 50–70 °C und ebenfalls geringem Propendruck bekannt. Bei der säurekatalysierten Alkylierung wird selten und vereinzelt noch Schwefelsäure eingesetzt.[7]
Gasphase
[Bearbeiten | Quelltext bearbeiten]Die Alkylierung von Benzol mit Propen in der Gasphase wird bei Temperaturen von 200–250 °C und Drücken von 20–40 bar an Phosphorsäure-Katalysatoren, welche auf Siliciumdioxid geträgert sind und Bortrifluorid als Promotor enthalten, durchgeführt. Die gesamte Reaktion läuft dabei im Festbettreaktor ab.[7]
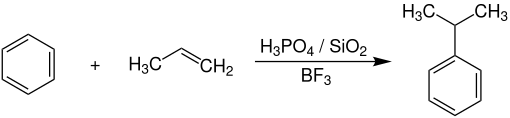
Die Selektivitäten erreichen hierbei 96–97 % bezogen auf Benzol und 91–92 % bezogen auf Propen. Als Nebenprodukte entstehen nur geringe Mengen an Di- und Triisopropylbenzol sowie Propylbenzol. Nach einer destillativen Aufarbeitung erhält man Cumol in einer Reinheit von mehr als 99,5 %.[7]
Die weltweiten Herstellkapazitäten für Cumol betrugen im Jahr 2004 mehr als 10,5 Millionen Jahrestonnen.[7] Im Jahr 2019 steigerte sich die globale Kapazität auf 19 Millionen Tonnen.[8] Seit den 1990ern werden zunehmend Zeolite als Katalysatoren verwendet.[9]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Cumol hat einen charakteristischen, aromatischen Geruch, die Geruchsschwelle liegt bei 0,04–6,4 mg·m−3. In vielen gängigen organischen Lösungsmitteln, z. B. Ether und Ethanol, ist Cumol löslich, in Wasser hingegen sehr schwer löslich.
Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Cumol ist eine farblose Flüssigkeit, die unter Normaldruck bei 152 °C siedet.[1] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,05419, B = 1455,811 und C = −65.948 im Temperaturbereich von 343,2 K bis 426,5 K.[10] Wichtige thermodynamische Größen werden in der folgenden Tabelle gegeben:
| Eigenschaft | Typ | Wert [Einheit] | Bemerkungen |
|---|---|---|---|
| Standardbildungsenthalpie | ΔfH0liquid ΔfH0gas |
−41,2 kJ·mol−1[11] 3,92 kJ·mol−1[11] |
als Flüssigkeit als Gas |
| Verbrennungsenthalpie | ΔcH0liquid | −5215,44 kJ·mol−1[11] | als Flüssigkeit |
| Wärmekapazität | cp | 215,4 J·mol−1·K−1 (25 °C)[12] 1,79 J·g−1·K−1 (25 °C) |
als Flüssigkeit |
| Kritische Temperatur | Tc | 631 K[13] | |
| Kritischer Druck | pc | 32,1 bar[13] | |
| Kritische Dichte | ρc | 2,32 mol·l−1[14] | |
| Verdampfungsenthalpie | ΔVH | 41,2 kJ·mol−1[15] | bei 364 K |
| Schmelzenthalpie | ΔfusH | 7,326 kJ·mol−1[12] | am Schmelzpunkt |
Sicherheitstechnische Kenngrößen
[Bearbeiten | Quelltext bearbeiten]Cumol bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von 31 °C.[1] Der Explosionsbereich liegt zwischen 0,8 Vol.‑% (40 g/m3) als untere Explosionsgrenze (UEG) und 6 Vol.‑% (300 g/m3) als obere Explosionsgrenze (OEG).[1][16] Der untere Explosionspunkt liegt bei 29 °C.[1] Die Grenzspaltweite wurde mit 1,05 mm bestimmt.[1][16] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIA.[16] Die Zündtemperatur beträgt 420 °C.[1][16] Der Stoff fällt somit in die Temperaturklasse T2.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Cumol dient als Zwischenprodukt zur Herstellung von Phenol und Aceton nach dem Cumolhydroperoxid-Verfahren (Hock-Verfahren).[17]

In seltenen Fällen wird es auch als Lösungsmittel eingesetzt. Cumol wird auch als Klopfschutzmittel im Flugtreibstoff verwendet. Gegenüber dem auch verwendbaren Benzol besitzt es einen wesentlich niedrigeren Stockpunkt von ca. −96 °C.
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Cumol ist entzündlich und reizt die Atmungsorgane. Es kann zudem die Haut (Brennen/Jucken) und die Augen reizen, die Leber schädigen und zu Schwindel und Benommenheit führen. Die Internationale Agentur für Krebsforschung stufte Cumol im Jahr 2013 als möglicherweise krebserzeugend ein.[18]
Cumol wurde auf der Grundlage neuer Karzinogenitätsdaten aus den USA neu bewertet. Cumol zeigte eine krebserregende Aktivität bei Ratten und Mäusen aufgrund erhöhter Inzidenzen von Nasen- und Nierentumoren bei Ratten und Lungen- und Lebertumoren bei Mäusen. Die PDE für Cumol wurde von 55 mg/Tag (Klasse 3) auf 0,7 mg/Tag (Klasse 2) gesenkt.[19]
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Eintrag zu Cumol. In: P. J. Linstrom, W. G. Mallard (Hrsg.): NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j k l m n o p q r s Eintrag zu Cumol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ Eintrag zu Cumol. In: Römpp Online. Georg Thieme Verlag, abgerufen am 19. Juni 2014.
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ Eintrag zu Cumene im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 26. Juli 2023. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 98-82-8 bzw. iso-Propylbenzol), abgerufen am 15. September 2019.
- ↑ Christian Wiegand: Entstehung und Deutung wichtiger organischer Trivialnamen. I. Kohlenwasserstoffe der Benzolreihe. In: Angewandte Chemie. 60 (4), 1948, S. 109–111; doi:10.1002/ange.19480600407.
- ↑ a b c d e Hans-Jürgen Arpe: Industrielle Organische Chemie - Bedeutende Vor- und Zwischenprodukte. 6. Auflage. WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim 2007, ISBN 978-3-527-31540-6, S. 380 ff.
- ↑ Andy Nicholson: The Downstream Functional Aromatics Market. In: Jacques Mortier (Hrsg.): Industrial Arene Chemistry: Markets, Technologies, Sustainable Processes and Cases Studies of Aromatic Commodities. WILEY-VCH Verlag GmbH, Weinheim 10. März 2023, doi:10.1002/9783527827992.ch2.
- ↑ Manfred Weber, Werner Pompetzki, Ralf Bonmann, Markus Weber: Acetone. In: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, Germany 2014, ISBN 978-3-527-30673-2, S. 1–19, doi:10.1002/14356007.a01_079.pub4 (wiley.com [abgerufen am 4. Juli 2024]).
- ↑ C. B. Williamham, W. J. Taylor, J. M. Pignocco, F. D. Rossini: Vapor Pressures and Boiling Points of Some Paraffin, Alkylcyclopentane, Alkylcyclohexane, and Alkylbenzene Hydrocarbons. In: J. Res. Natl. Bur. Stand. (U.S.), 35, 1945, S. 219–244, doi:10.6028/jres.035.009.
- ↑ a b c E. J. Prosen, R. Gilmont, F. D. Rossini: Heats of combustion of benzene, toluene, ethyl-benzene, o-xylene, m-xylene, p-xylene, n-propylbenzene, and styrene. In: J. Res. Natl. Bur. Stand. (U.S.), 34, 1945, S. 65–70. (PDF)
- ↑ a b K. Kishimoto, H. Suga, S. Syuzo: Calorimetric study of the glassy state. VIII. Heat capacity and relaxational phenomena of isopropylbenzene. In: Bull. Chem. Soc. Japan. 46, 1973, S. 3020–3031, doi:10.1246/bcsj.46.3020.
- ↑ a b C. Tsonopoulos, D. Ambrose: Vapor-Liquid Critical Properties of Elements and Compounds. 3. Aromatic Hydrocarbons. In: J. Chem. Eng. Data. 40, 1995, S. 547–558, doi:10.1021/je00019a002.
- ↑ J. L. Hales, R. Townsend: Liquid Densities from 293 to 490 K of Nine Aromatic Hydrocarbons. In: J. Chem. Thermodyn. 4, 1972, S. 763–772, doi:10.1016/0021-9614(72)90050-X.
- ↑ Emilio Cepeda, Cristina Gonzalez, Jose M. Resa: Isobaric vapor-liquid equilibrium for the cumene-phenol system. In: J. Chem. Eng. Data. 34, 1989, S. 270–273, doi:10.1021/je00057a004.
- ↑ a b c d E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen. Band 1: Brennbare Flüssigkeiten und Gase. Wirtschaftsverlag NW – Verlag für neue Wissenschaft, Bremerhaven 2003.
- ↑ Siegfried Hauptmann: Organische Chemie. 2. Auflage. Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, ISBN 3-342-00280-8, S. 334.
- ↑ Some chemicals present in industrial and consumer products, food and drinking-water (= IARC monographs on the evaluation of carcinogenic risks to humans. Nr. 101). IARC, Lyon 2013, ISBN 978-92-832-1324-6, S. 325–348 (iarc.fr).
- ↑ ICH guideline Q3C (R8) on impurities: guideline for residual solvents



