1,5-Dihydroxynaphthalin
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
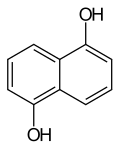
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 1,5-Dihydroxynaphthalin | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C10H8O2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Nadeln[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 160,17 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[3] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
sehr schwer löslich in Wasser (0,6 g·l−1 bei 20 °C)[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
1,5-Dihydroxynaphthalin (abgeleitet von Naphthalin) ist eine chemische Verbindung aus der Gruppe der Naphthalindiole.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]1,5-Dihydroxynaphthalin kann durch alkalische Hydrolyse des Dinatriumsalzes von Naphthalin-1,5-disulfonsäure bei Temperaturen von 270 bis 290 °C und bei 14 bis 20 bar gewonnen werden.[5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]1,5-Dihydroxynaphthalin ist ein brennbarer schwer entzündbarer Feststoff mit schwachem Geruch. Er zersetzt sich bei Erhitzung über 250 °C.[3] Aus wässrigem Methylglycol kristallisiert 1,5-Dihydroxynaphthalin in farblosen Nadeln. Die Verbindung ist sublimierbar, leicht löslich in Diethylether und Aceton, jedoch schwerlöslich in Wasser und Kohlenwasserstoffen.[2]
Verwendung
[Bearbeiten | Quelltext bearbeiten]1,5-Dihydroxynaphthalin wird als Zwischenprodukt zur Herstellung von Azofarbstoffen, Pharmazeutika und für Fotochemikalien verwendet.[6]
Beispielsweise erhält man durch Umsetzung von 1,5-Dihydroxynaphthalin als Kupplungskomponente mit diazotierter 3-Amino-4-hydroxybenzolsulfonsäure den Beizenfarbstoff C.I. Mordant Black 9.[2]
Die Reaktion von 1,5-Dihydroxynaphthalin mit Peressigsäure im Überschuss liefert ein Gemisch aus Juglon und 2-Hydroxy-1,4-naphthochinon.[7]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu 1,5-NAPHTHALENEDIOL in der CosIng-Datenbank der EU-Kommission, abgerufen am 22. März 2022.
- ↑ a b c Gerald Booth: Naphthalene Derivatives. In: Ullmann’s Encyclopedia of Industrial Chemistry. Band 32. Wiley-VCH Verlag & Co. KGaA, Weinheim, Germany 2000, S. 681, doi:10.1002/14356007.a17_009.
- ↑ a b c d e Eintrag zu Naphthalin-1,5-diol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Januar 2024. (JavaScript erforderlich)
- ↑ W. L. F. Armarego, Christina Chai: Purification of Laboratory Chemicals. Butterworth-Heinemann, 2009, ISBN 978-0-08-087824-9, S. 278 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Patent DE3840618C1: Verfahren zur Herstellung von 1,5-Dihydroxy- und 1,5-Diamino-naphtalin. Angemeldet am 2. Dezember 1988, veröffentlicht am 15. März 1990, Anmelder: Bayer AG, Erfinder: Horst Behre et al.
- ↑ Datenblatt 1,5-Dihydroxynaphthalene, 98% bei Alfa Aesar ( vom 29. Dezember 2016 im Internet Archive)
- ↑ Christoph Grundmann: A New Synthesis of Juglone. In: Synthesis. Band 1977, Nr. 9, September 1977, S. 644–645, doi:10.1055/s-1977-24517.


