3,4-Epoxycyclohexylmethyl-3′,4′-epoxycyclohexancarboxylat
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
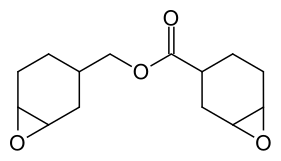
| |||||||||||||||||||
| Komplexes Stereoisomerengemisch – Strukturformel ohne Stereochemie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 3,4-Epoxycyclohexylmethyl-3′,4′-epoxycyclohexancarboxylat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C14H20O4 | ||||||||||||||||||
| Kurzbeschreibung |
farb- und geruchlose, viskose Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 252,306 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
1,17 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt |
−37 °C[1] | ||||||||||||||||||
| Löslichkeit |
wenig löslich in Wasser (13,85 g·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Brechungsindex |
1,498 (20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
3,4-Epoxycyclohexylmethyl-3′,4′-epoxycyclohexancarboxylat (ECC) ist ein cycloaliphatisches Epoxidharz, das zahlreiche industrielle Anwendungen besitzt. Es wird durch kationische Polymerisation mit Hilfe thermolatenter Photoinitiatoren zu vernetzten, unlöslichen Duroplasten umgesetzt. Formulierungen, die auf cycloaliphatischen Epoxidharzen wie ECC basieren sind dafür bekannt, durch Härtung in Duroplaste mit hoher Wärme- und Chemikalienbeständigkeit sowie guter Haftung überzugehen.[3]
Geschichte
[Bearbeiten | Quelltext bearbeiten]Die Homopolymerisation von 3,4-Epoxycyclohexylmethyl-3′,4′-epoxycyclohexancarboxylat basiert auf kationischer Strahlenhärtung, welche über eine photochemische Bildung einer Supersäure und anschließende kationische Polymerisation verläuft. Dies wurde das erste Mal in den 1970er-Jahren erkannt.[4]
Herstellung
[Bearbeiten | Quelltext bearbeiten]3,4-Epoxycyclohexylmethyl-3′,4′-epoxycyclohexancarboxylat kann über eine Claisen-Tiščenko-Reaktion mit nachfolgender Epoxidierung durch eine Persäure hergestellt werden.[5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]3,4-Epoxycyclohexylmethyl-3′,4′-epoxycyclohexancarboxylat besitzt bei 25 °C eine dynamische Viskosität von 400 mPa·s.[3]
Reaktivität
[Bearbeiten | Quelltext bearbeiten]Zur Homopolymerisation werden dem Monomer 3,4-Epoxycyclohexylmethyl-3′,4′-epoxycyclohexancarboxylat 1,5 bis 3 Gew.-% eines Initiators zugesetzt. Oberhalb von 3 Gew.-% Initiator wurde keine Beschleunigung mehr gefunden, steigende Anteile von Initiatoren erhöhen jedoch die Sprödigkeit des Duroplasten.[6] Nach einer Photopolymerisation ist meist noch ein Post-Curing für die komplette Aushärtung notwendig.[6]
Es ist bekannt, dass die Reaktivität des Monomers geringer ist, als sie sein könnte, da die enthaltene Estergruppe mit dem reaktiven Kettenende reagiert und diesen so stabilisiert. Es reagiert daher deutlich langsamer als andere Moleküle ohne Estergruppe.[7][3] Die Polymerisationsrate von ECC ist zudem deutlich langsamer als die radikalischer Monomere. Es ist daher das Ziel der Forschung, kationische Systeme mit höheren Polymerisationsgeschwindigkeit aber gleicher Performance zu erfinden.[3]
Vernetztes ECC
[Bearbeiten | Quelltext bearbeiten]Kationisch vernetztes 3,4-Epoxycyclohexylmethyl-3′,4′-epoxycyclohexancarboxylat wird in einer Vielzahl von industriellen Anwendungen eingesetzt, wegen seiner geringen Viskosität, ausgezeichnete elektrische Eigenschaften und hohen Zuverlässigkeit u. a. als elektrischer Isolator, Beschichtung und Klebstoff oder Druckfarbe.[8] Homopolymerisiertes ECC ist jedoch ausgesprochen spröde, was nachteilhaft ist. Diesem Problem kann durch Integration von Elastomerpartikel in die Epoxidmatrix, wie Gummi oder Silikon, durch Integration von anorganischen Füllstoffen[9] oder durch Plastifizierung aufgrund der Polymerisation in Gegenwart von Polyesterpolyolen[10] begegnet werden. Letztere werden über den Aktivierten-Monomer-Mechanismus auch kovalent in das Polymernetzwerk eingebunden.[11]
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]3,4-Epoxycyclohexylmethyl-3′,4′-epoxycyclohexancarboxylat wurde 2013 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von 3,4-Epoxycyclohexylmethyl-3′,4′-epoxycyclohexancarboxylat waren die Besorgnisse bezüglich Exposition von Arbeitnehmern und hohes Risikoverhältnis (Risk Characterisation Ratio, RCR) sowie der Gefahren ausgehend von einer möglichen Zuordnung zur Gruppe der CMR-Stoffe und der vermuteten Gefahren durch sensibilisierende Eigenschaften. Die Neubewertung fand ab 2013 statt und wurde von Irland durchgeführt. Anschließend wurde ein Abschlussbericht veröffentlicht.[12][13]
Literatur
[Bearbeiten | Quelltext bearbeiten]- Ellis Bryan: Polymers: a property database. 2. Auflage. CRC Press, Boca Raton FL [u.a.] 2009, ISBN 978-0-8493-3940-0, S. 150 (englisch, eingeschränkte Vorschau in der Google-Buchsuche).
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Eintrag zu 3,4-Epoxycyclohexylmethyl-3,4-epoxycyclohexylcarboxylat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ Datenblatt 3,4-Epoxycyclohexylmethyl 3,4-epoxycyclohexanecarboxylate bei Sigma-Aldrich, abgerufen am 24. März 2015 (PDF).
- ↑ a b c d Hiroshi Sasaki: Curing properties of cycloaliphatic epoxy derivatives. In: Progress in Organic Coatings. 58. Jahrgang, Nr. 2–3, Februar 2007, S. 227–230, doi:10.1016/j.porgcoat.2006.09.030.
- ↑ J. V. Crivello, J. H. W. Lam: Dye-sensitized photoinitiated cationic polymerization. In: Journal of Polymer Science: Polymer Chemistry Edition. 16. Jahrgang, Nr. 10, Oktober 1978, S. 2441–2451, doi:10.1002/pol.1978.170161004.
- ↑ Brian Dillman, Julie L. P. Jessop: Chain transfer agents in cationic photopolymerization of a bis-cycloaliphatic epoxide monomer: Kinetic and physical property effects. In: Journal of Polymer Science Part A: Polymer Chemistry. 51. Jahrgang, Nr. 9, 1. Mai 2013, S. 2058–2067, doi:10.1002/pola.26595.
- ↑ a b Atsushi Udagawa, Yasuhiko Yamamoto, Yoshio Inoue, Riichirô Chûjô: Dynamic mechanical properties of cycloaliphatic epoxy resins cured by ultra-violet- and heat-initiated cationic polymerizations. In: Polymer. 32. Jahrgang, Nr. 15, Januar 1991, S. 2779–2784, doi:10.1016/0032-3861(91)90108-U.
- ↑ James V. Crivello, Ulrike Varlemann: Mechanistic study of the reactivity of 3,4-epoxycyclohexylmethyl 3′,4′-epoxycyclohexancarboxylate in photoinitiated cationic polymerizations. In: Journal of Polymer Science Part A: Polymer Chemistry. 33. Jahrgang, Nr. 14, Oktober 1995, S. 2473–2486, doi:10.1002/pola.1995.080331421.
- ↑ Cristina Mas, Ana Mantecón, Angels Serra, Xavier Ramis und Josep Maria Salla: Improved thermosets obtained from cycloaliphatic epoxy resins and γ-butyrolactone with lanthanide triflates as initiators. I. Study of curing by differential scanning calorimetry and Fourier transform infrared. In: Journal of Polymer Science Part A: Polymer Chemistry. 43. Jahrgang, Nr. 11, 1. Juni 2005, S. 2337–2347, doi:10.1002/pola.20711.
- ↑ Hendrik Lützen, Peter Bitomsky, Kurosch Rezwan, Andreas Hartwig: Partially crystalline polyols lead to morphology changes and improved mechanical properties of cationically polymerized epoxy resins. In: European Polymer Journal. 49. Jahrgang, Nr. 1, Januar 2013, S. 167–176, doi:10.1016/j.eurpolymj.2012.10.015.
- ↑ Emmanouil Spyrou: Radiation initiated cationic polymerization with tailor-made polyesters. In: Progress in Organic Coatings. 43. Jahrgang, Nr. 1–3, November 2001, S. 25–31, doi:10.1016/S0300-9440(01)00240-5.
- ↑ Yusuf Yagci, Wolfram Schnabel: On the mechanism of photoinitiated cationic polymerization in the presence of polyols. In: Die Angewandte Makromolekulare Chemie. 270. Jahrgang, Nr. 1, 1. September 1999, S. 38–41, doi:10.1002/(SICI)1522-9505(19990901)270:1<38::AID-APMC38>3.0.CO;2-S.
- ↑ Europäische Chemikalienagentur (ECHA): Substance Evaluation Conclusion and Evaluation Report.
- ↑ Community Rolling Action Plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): 7-oxabicyclo[4.1.0]hept-3-ylmethyl 7-oxabicyclo [4.1.0]heptane-3-carboxylate, abgerufen am 26. März 2019.
