Nitrobenzaldehyde
(Weitergeleitet von 4-Nitrobenzaldehyd)
Die Nitrobenzaldehyde bilden in der Chemie eine Stoffgruppe, die sich sowohl vom Benzaldehyd als auch vom Nitrobenzol ableitet. Die Struktur besteht aus einem Benzolring mit angefügter Aldehyd- (–CHO) und Nitrogruppe (–NO2). Durch deren unterschiedliche Anordnung (ortho, meta oder para) ergeben sich drei Konstitutionsisomere mit der Summenformel C7H5NO3.
Vertreter
[Bearbeiten | Quelltext bearbeiten]| Nitrobenzaldehyde | |||||||
| Name | 2-Nitrobenzaldehyd | 3-Nitrobenzaldehyd | 4-Nitrobenzaldehyd | ||||
| Andere Namen | o-Nitrobenzaldehyd | m-Nitrobenzaldehyd | p-Nitrobenzaldehyd | ||||
| Strukturformel | 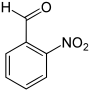
|

|

| ||||
| CAS-Nummer | 552-89-6 | 99-61-6 | 555-16-8 | ||||
| PubChem | 11101 | 7449 | 541 | ||||
| Summenformel | C7H5NO3 | ||||||
| Molare Masse | 151,12 g·mol−1 | ||||||
| Aggregatzustand | fest | ||||||
| Kurzbeschreibung | leicht gelbes kristallines Pulver | ||||||
| Schmelzpunkt | 41–43 °C[1] | 55 °C[2] | 103–106 °C[3] | ||||
| Siedepunkt | 156 °C (20 hPa)[1] | 164 °C (31 hPa)[2] | –[3] | ||||
| GHS- Kennzeichnung |
|
|
| ||||
| H- und P-Sätze | 302‐315‐319‐335 | 302‐411 | 317‐319‐412 | ||||
| keine EUH-Sätze | keine EUH-Sätze | keine EUH-Sätze | |||||
| 261‐305+351+338 | 264‐270‐273‐301+312‐391‐501 | 261‐280‐302+352‐305+351+338 | |||||
Darstellung
[Bearbeiten | Quelltext bearbeiten]- 2-Nitrotoluol wird in der Hitze chloriert. Das entstandene 2-Nitrobenzylidendichlorid wird verseift, wobei 2-Nitrobenzaldehyd entsteht.

- 3-Nitrobenzaldehyd erhält man aus Benzaldehyd durch Umsetzung mit rauchender Salpetersäure in Gegenwart von konzentrierter Schwefelsäure.[4][5]

- 4-Nitrobenzaldehyd erhält man aus 4-Nitrotoluol durch Oxidation mit Chrom(VI)-oxid in Acetanhydrid. Das entstehende 4-Nitrobenzaldiacetat wird mit Schwefelsäure in wässrigem Ethanol hydrolysiert.[6]

Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Die Nitrobenzaldehyde sind leicht gelbe kristalline Feststoffe, die zum Teil bittermandelartig riechen. Der 4-Nitrobenzaldehyd, der die höchste Symmetrie aufweist, besitzt den höchsten Schmelzpunkt.
Im basischen Medium disproportionieren in einer Cannizzaro-Reaktion die Nitrobenzaldehyde zu Nitrobenzoesäuren und Nitrobenzylalkoholen.
Verwendung
[Bearbeiten | Quelltext bearbeiten]- 2-Nitrobenzaldehyd wird als Reagenz auf Isopropanol und Aceton verwendet.
- Mit Aceton reagiert 2-Nitrobenzaldehyd zu Indigo.[7]

Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Eintrag zu 2-Nitrobenzaldehyd in der GESTIS-Stoffdatenbank des IFA, abgerufen am 29. März 2016. (JavaScript erforderlich)
- ↑ a b c Eintrag zu 3-Nitrobenzaldehyd in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ a b c Eintrag zu 4-Nitrobenzaldehyd in der GESTIS-Stoffdatenbank des IFA, abgerufen am 29. März 2016. (JavaScript erforderlich)
- ↑ Versuchsvorschrift: Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd (PDF) der Sammlung Integriertes Organisch-chemisches Praktikum der Universität Regensburg, abgerufen am 30. Oktober 2011.
- ↑ Uni Hamburg: 3-Nitrobenzaldehyd, Versuchsvorschrift ( vom 21. Dezember 2015 im Internet Archive) (PDF; 24 kB).
- ↑ S. V. Lieberman and Ralph Connor: p-Nitrobenzaldehyde In: Organic Syntheses. 18, 1938, S. 61, doi:10.15227/orgsyn.018.0061; Coll. Vol. 2, 1943, S. 441 (PDF).
- ↑ Helmut Schmidt: Indigo – 100 Jahre industrielle Synthese. In: Chemie in unserer Zeit, 31 (3), 1997, S. 121–128; doi:10.1002/ciuz.19970310304.

