Nitroanisidine
Die Nitroanisidine bilden eine Stoffgruppe, die sich sowohl vom Nitrobenzol, Anisol (Methoxybenzol) als auch vom Anilin (Aminobenzol) ableitet. Die Struktur besteht aus einem Benzolring mit angefügter Nitro- (–NO2), Methoxy- (–OCH3) und Aminogruppe (–NH2) als Substituenten. Durch deren unterschiedliche Anordnung ergeben sich zehn Konstitutionsisomere mit der Summenformel C7H8N2O3.
Geht man von den disubstituierten Stammverbindungen aus, so kann man die Nitroanisidine als Methoxyderivate der Nitroaniline, als Aminoderivate der Nitroanisole oder als Nitroderivate der Anisidine ansehen. Die Namensgebung folgte der letzten Variante, weil die Anisidine die einzigen der drei disubstituierten Stammverbindungen sind, die einen komplett eigenen Namen bilden.
| Nitroanisidine | |||||||||
| Stammverbindung | 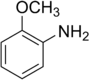
| ||||||||
| o-Anisidin | |||||||||
| Strukturformel | 
|

|

|

| |||||
| Name |
|
|
|
| |||||
| CAS-Nummer | 85-45-0 | 97-52-9 | 99-59-2 | 16554-45-3 | |||||
| ECHA-InfoCard | 100.001.462 | 100.002.354 | 100.002.518 | 100.036.910 | |||||
| PubChem | 66559 | 7337 | 7447 | 85491 | |||||
| Summenformel | C7H8N2O3 | ||||||||
| Molare Masse | 168,15 g·mol−1 | ||||||||
| Aggregatzustand | fest | ||||||||
| Kurzbeschreibung | gelbes geruchloses Pulver[1] | oranges Pulver[2] | |||||||
| Schmelzpunkt | 140–142 °C[1] / 139–143 °C[3] | 118 °C[2] | 73–78 °C[4] | ||||||
| Siedepunkt | > 260 °C (Zersetzung)[1] | ||||||||
| Dichte | 1,45 g·cm−3[1] | ||||||||
| Löslichkeit | 0,2 g/l bei 20 °C in Wasser[1] |
||||||||
| GHS- Kennzeichnung |
|
|
| ||||||
| H- und P-Sätze | 302‐351‐411 | 302 | 302+312+332‐315‐319‐335 | ||||||
| 202‐264‐273‐280‐301+312‐308+313 | 301+312+330 | 301+330+331‐302+352 | |||||||
| Nitroanisidine | |||||
| Stammverbindung | 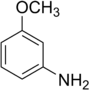
| ||||
| m-Anisidin | |||||
| Strukturformel | 
|

|

|

| |
| Name |
|
|
|
| |
| CAS-Nummer | 16554-47-5 | 16292-88-9 | 586-10-7 | 16133-49-6 | |
| ECHA-InfoCard | 100.197.662 | 100.036.615 | |||
| PubChem | 10464700 | 2755795 | 2759598 | 85300 | |
| Summenformel | C7H8N2O3 | ||||
| Molare Masse | 168,15 g·mol−1 | ||||
| Aggregatzustand | fest | ||||
| Kurzbeschreibung | |||||
| Schmelzpunkt | 125–127 °C[5] | ||||
| Siedepunkt | |||||
| Dichte | |||||
| Löslichkeit | |||||
| GHS- Kennzeichnung |
| ||||
| H- und P-Sätze | 302+312+332‐315‐319‐335 | ||||
| 301+330+331‐302+352 | |||||
| Nitroanisidine | |||||
| Stammverbindung | 
| ||||
| p-Anisidin | |||||
| Strukturformel | 
|

| |||
| Name |
|
| |||
| CAS-Nummer | 96-96-8 | 577-72-0 | |||
| ECHA-InfoCard | 100.002.317 | 100.110.092 100.209.982 | |||
| PubChem | 66793 | 123071 | |||
| Summenformel | C7H8N2O3 | ||||
| Molare Masse | 168,15 g·mol−1 | ||||
| Aggregatzustand | fest | ||||
| Kurzbeschreibung | orange bis violettes geruchloses Pulver[6] |
||||
| Schmelzpunkt | 123–126 °C[7] | ||||
| Siedepunkt | |||||
| Dichte | |||||
| Löslichkeit | |||||
| GHS- Kennzeichnung |
|
| |||
| H- und P-Sätze | 300+310+330‐373‐412 | 317‐319 | |||
| 262‐273‐280‐301+310+330‐302+352+310‐304+340+310 | 280‐305+351+338 | ||||
Weblinks
[Bearbeiten | Quelltext bearbeiten]- The Carcinogenic Potency Project: 5-Nitro-o-anisidine
- Paul E. Fanta and D. S. Tarbell: 2-Nitro-4-Methoxyaniline In: Organic Syntheses. 25, 1945, S. 78, doi:10.15227/orgsyn.025.0078; Coll. Vol. 3, 1955, S. 661 (PDF).
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Eintrag zu 4-Nitro-o-anisidin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Januar 2024. (JavaScript erforderlich)
- ↑ a b c Eintrag zu 5-Nitro-o-anisidin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Januar 2024. (JavaScript erforderlich)
- ↑ Datenblatt 2-Methoxy-4-nitroaniline bei Sigma-Aldrich, abgerufen am 27. Dezember 2019 (PDF).
- ↑ a b Datenblatt 2-Methoxy-6-nitroaniline, 97% bei Alfa Aesar, abgerufen am 27. Dezember 2019 (Seite nicht mehr abrufbar).
- ↑ a b Datenblatt 5-Methoxy-2-nitroaniline, 98% bei Alfa Aesar, abgerufen am 27. Dezember 2019 (Seite nicht mehr abrufbar).
- ↑ a b Eintrag zu 2-Nitro-p-anisidin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Januar 2024. (JavaScript erforderlich)
- ↑ Datenblatt 4-Methoxy-2-nitroaniline bei Sigma-Aldrich, abgerufen am 27. Dezember 2019 (PDF).
- ↑ 4-Methoxy-3-nitroaniline. (pdf) Matrix Scientific, 10. Februar 2017, abgerufen am 27. Dezember 2019 (englisch).



