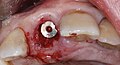
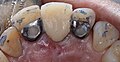
Zahnimplantat

1. Zahnfleisch;
2. Knochengewebe;
3. Schraubenförmiges Implantat aus Titan

implantat



Ein Zahnimplantat (lateinisch implantare ‚einpflanzen‘) ist ein in den Kieferknochen eingesetztes „alloplastisches Konfektionsteil“ (Implantat). Das Teilgebiet der Zahnheilkunde, das sich mit der Insertion (Einsetzen) von Zahnimplantaten in den Kieferknochen befasst, wird als Implantologie (von altgriechisch λόγος lógos, deutsch ‚Wort‘, ‚Lehre‘) bezeichnet. Durch ihre Verwendbarkeit als Träger von Zahnersatz übernehmen Zahnimplantate die Funktion künstlicher Zahnwurzeln. Hierzu werden sie entweder mittels Schraubgewinde in den Kieferknochen (enossale[1] Implantate) eingedreht oder eingesteckt. Sie verbinden sich innerhalb von 3 bis 6 Monaten mit dem umgebenden Knochen zu einer festen, äußerst belastbaren Trägereinheit (Osseointegration).
Von der Implantatform hängt die chirurgische Insertionstechnik ab. Aus der Gestalt des Abutments, des aus dem Kieferknochen herausragenden Implantatteils, resultiert die Anfertigung der Suprakonstruktion, des auf den Implantaten einzugliedernden Zahnersatzes. Zahnimplantate bestehen seit den 1980er Jahren üblicherweise aus Titan, aber auch aus keramischen Materialien oder Kunststoff (PEEK).[2]
In der Zahnmedizin bietet die festsitzende Versorgung eine optimale Lösung für Patienten mit zahnlosem Kiefer. Abhängig von der Kieferform und dem Knochenangebot werden 4, 6 bis 8 Zahnimplantate eingesetzt. Wenn ein einzelner Zahn verloren geht, können Zahnimplantate eine empfohlene Lösung sein. Dadurch bleiben die gesunden Nachbarzähne von einem Beschliff und einer Überkronung verschont. Der Verlust der Backenzähne kann auch die Kaufunktion beeinträchtigen. Bei Verlust eines, mehrerer oder aller Zähne, wenn der Patient keinen herausnehmbaren Zahnersatz akzeptieren möchte, bevorzugt eine feste und dauerhafte Lösung, anstatt herausnehmbaren Zahnersatz zu tragen. Auf diesen Implantaten wird dann eine Brücke befestigt, die nicht mehr abgenommen werden muss.[3]
Geschichte der Implantologie
[Bearbeiten | Quelltext bearbeiten]Frühe Implantate
[Bearbeiten | Quelltext bearbeiten]Die ersten Implantationen zum Ersatz von Zähnen sind aus dem 7. bis 8. Jahrhundert bei den Mayas durch den italienischen Professor für Implantologie an der Universität von Santos (Brasilien), Amedeo Bobbio, nachgewiesen. In einem Fragment des Unterkieferknochens einer jungen Frau befinden sich drei Implantate aus einer zugeschliffenen Muschelschale. Auf Grund der röntgenologisch nachgewiesenen Osseointegration wurden diese Muschelimplantate zu Lebzeiten und nicht post mortem eingesetzt. Ein anderes Fragment aus der Zeit der Mayas, das durch den Archäologen R. R. Andrews gefunden und beschrieben wurde, in das ein „schwarzer Stein“ als Unterkieferfrontzahn eingepflanzt gewesen sein sollte, ist nicht mehr auffindbar. Bis zum Nachweis durch Bobbio im Jahre 1970 galten die Muschelimplantate als post mortem eingesetzt, im Sinne eines Begräbnisrituals.[4]
Andere Versuche, fehlende Zähne zu ersetzen, sind nicht als Implantate zu bezeichnen, wie beispielsweise die Transplantation oder Reimplantation von Zähnen und Zähnen aus organischen oder anorganischen Materialien, wie beispielsweise Elfenbein oder Walrosszähnen und deren Befestigung an den vorhandenen Zähnen mittels Goldfäden oder Goldbändern. Hierzu zählten auch vorgenommene Transplantationen der Zähne von Toten, wie sie etwa im Mittelalter bei Abulcasis, in der Frühen Neuzeit bei Pierre Fauchard und Ambroise Paré und vielen anderen sowie während der Schlacht bei Waterloo (1815) und anderen Kriegen erwähnt wird.[5][6][7][8][9]
Von großer Bedeutung für die weitere Entwicklung der Implantologie war die Erfindung des künstlichen Keramikzahns durch Giuseppangelo Fonzi im Jahre 1806. Seine mit Platinhaken direkt in die Alveole eingepflanzten Kunstzähne erfüllten sowohl ästhetische als auch funktionale Anforderungen. Ein erstes Metallimplantat aus Gold wurde von dem Italiener J. Maggiolo im Jahre 1809 entworfen und in eine frische menschliche Extraktionswunde eingesetzt. Maggiolo praktizierte in Paris und veröffentlichte seine Erkenntnisse in seinem Buch Le Manuel de l’Art du Dentiste in Nancy.[10]
Um 1840 versuchten sich Chapin Aaron Harris und Horace Henry Hayden, Gründer des Baltimore College of Dental Surgery, an enossalen Implantaten mit Zähnen aus Eisen, später aus Blei.[11] Mehrere ähnliche Fallberichte folgten durch Rogers (1845), Younger (1885), Edmunds (1886), Edwards (1889) und Payne (1898). 1895 berichtete William Gibson Arlington Bonwill über Gold- und Iridiumpfeiler, die er in Alveolen implantiert hat, um einzelne Zähne zu ersetzen und ganze Zahnbögen wiederherzustellen.[12]
Die Entwicklung im 20. Jahrhundert
[Bearbeiten | Quelltext bearbeiten]Alvin Strock setzte 1937 in den USA das erste Vitallium-Schraubenimplantat als Zahnwurzelersatz ein. Vitallium war das erste biokompatible Metall, das ein Jahr zuvor von Charles Venable, einem orthopädischen Chirurgen, entwickelt worden war.[13] Der Beginn der enossalen Implantologie wird Manlio Formigini zugeschrieben, der eine Helikoidalschraube (altgriechisch ἑλικοειδής helikoeidēs, deutsch ‚wie gewunden‘) aus Tantal empfahl. Er wird als Vater der modernen Implantologie bezeichnet. Es folgten die Schraube nach Raphaël Cherchève oder die Tantalschrauben und Nadelimplantate nach Jacques Scialom und Ernst-Helmut Pruin.[14] Einen Seitenweg bildeten die komplikationsbehafteten subperiostalen, unter der Knochenhaut sitzenden Gerüstimplantate, die 1937 von Müller entwickelt worden waren und in den 1950er und 1960er Jahren Verbreitung fanden.[15]
In den 1960er Jahren wurde das Blattimplantat von Leonard I. Linkow konzipiert (Linkow-Blade),[16] ebenso das stabilisierte Klingenimplantat 1975 von Benedict Heinrich.[17]
Zu Beginn der zahnärztlichen Implantologie in Deutschland um das Jahr 1969 wurden zunächst von einigen wenigen hauptsächlich in eigener Praxis niedergelassenen Zahnärzten Zahnimplantate gegen den jahrelang erklärten Widerstand vieler Universitätskliniken und Kieferchirurgen eingesetzt.[18] Die Nachfrage nach Zahnimplantaten der Patienten war andererseits von Anfang an sehr groß.
Die moderne Entwicklung der Implantologie begann mit der Entdeckung der Biokompatibilität der Titanoberfläche durch den schwedischen Orthopäden Per-Ingvar Brånemark im Jahr 1967. Im Jahr 1978 fand die erste Zahnimplantat Consensus Conference statt, die gemeinsam vom National Institutes of Health und der Harvard University gesponsert war. Es war ein historisches Ereignis, an dem retrospektive Daten von Zahnimplantaten gesammelt und analysiert sowie Kriterien und Normen für die moderne Implantologie etabliert wurden.[19] Ende der 1970er Jahre entwickelte der 1934 in Concepción (Chile) geborene und bis 1980 an der Universität München als Professor tätige Zahnmediziner Georg Jorge Dietz ein endodontisches enossales Stiftimplantat[20] (den FS-Stift nach Dietz).[21]
Im Jahr 1982 präsentiert Brånemark in Toronto seine Arbeit, die 15 Jahre früher in Göteborg begonnen hatte. Seine Entdeckung und Anwendung der Osseointegration oder der biologischen Fusion von Knochen mit einem Fremdkörper war einmalig. Die wissenschaftliche Dokumentation der Implantologie war zuvor noch nie so umfassend gewesen. Die Torontoer Konferenz führte zu einer breiten Anerkennung der Brånemark’schen Implantatmethoden und -materialien. Sie ist einer der bedeutendsten wissenschaftlichen Durchbrüche in der Zahnmedizin seit den späten 1970er Jahren.
Daraufhin erfolgte in Deutschland 1982 die wissenschaftliche Anerkennung der zahnärztlichen Implantologie. Im Jahr 1988 wurden die mit der Implantologie verbundenen zahnärztlichen Leistungen in die Gebührenordnung für Zahnärzte (GOZ) mit einem kleinen Positionskatalog von 10 Gebührennummern (GOZ-Nr. 900–909) aufgenommen, einzeln beschrieben und mit einem Honorar bewertet.
Unter allen Implantatmaterialien hat sich Titan seit den 1970er Jahren durchgesetzt. Die Verbindung zwischen der Titanoberfläche und dem Knochen hat sich als zuverlässig erwiesen. Es kommt nur selten zu Frakturen des Implantatkörpers, weil die Elastizitätsmoduln von Knochen und Titan ähnlich sind.
Ende der 1980er Jahre implantierten etwa 1.500 Zahnärzte (ca. 2,5 %), im Jahr 2006 bereits etwa 5.000–7.000 Zahnärzte (ca. 8–12 % der ca. 60.000 bundesdeutschen Zahnärzte) mehr oder weniger regelmäßig. Zahlreiche Zahnärzte arbeiten interdisziplinär eng mit einem implantologisch tätigen Oralchirurgen oder Facharzt für Mund-, Kiefer- und Gesichtschirurgie zusammen, der den chirurgischen Teil übernimmt und die Implantate einsetzt, während der Zahnarzt anschließend die Suprakonstruktion (den Zahnersatz auf den Implantaten) eingliedert.[22] Die Suprakonstruktionen dürfen bei bestehender Fachgebietsbegrenzung in einigen Bundesländern nicht vom Kieferchirurgen angefertigt und eingegliedert werden.
An den Universitäten ist die Implantologie kein eigenes Ausbildungsfach, so dass die Zahnärzte sich im Rahmen einer postgraduierten Fortbildung die einschlägigen Kenntnisse aneignen.
Implantatformen
[Bearbeiten | Quelltext bearbeiten]Grundsätzlich lassen sich einteilige von zusammengesetzten Implantaten unterscheiden. Es haben sich überwiegend zusammengesetzte Zahnimplantate durchgesetzt, weil sie durch ihre Kombinationsmöglichkeit zwischen dem Wurzel- und Kronenanteil den gegebenen Verhältnissen am besten angepasst werden können. Außerdem ist durch das zweizeitige Vorgehen gewährleistet, dass die Osseointegration des Implantats durch eine zu frühe Belastung nicht beeinträchtigt wird. Mehrteilige Implantate bestehen aus dem im Knochen verankerten Implantatkörper, seltener einem separaten im Bereich der Mundschleimhaut liegenden Halsteil und dem Kopfteil, dem Abutment, das die Suprakonstruktion aufnimmt. Die zwei bzw. drei Teile werden meistens miteinander verschraubt. Die darauf angebrachten Suprakonstruktionen (Kronen, Brücken- oder Prothesenanker) werden verschraubt, zementiert oder verklebt.[23]
Bei einteiligen Zahnimplantaten ragt der Implantatkopf aus der Schleimhaut heraus, womit eine vorzeitige Belastung während der Einheilphase oft nicht zu vermeiden ist.
Schraubenimplantate
[Bearbeiten | Quelltext bearbeiten]Nach Jahrzehnten mit verschiedenen heute zum Teil naiv anmutenden Implantatformen aus der Vorkriegszeit haben sich rotationssymmetrische Implantate (meist Schraubenimplantate) durchgesetzt. Bei diesen Implantaten ist der Implantatkörper im Querschnitt kreisrund, sodass die Implantatkavität, der Hohlraum, der das Implantat aufnehmen soll, mit rotierenden Instrumenten, beispielsweise einem Kanonenbohrer, in den Kieferknochen präpariert werden kann. Die Schraubenimplantate unterscheiden sich vor allem in ihrer Konizität und in der Art des Gewindes.
Um die Anforderungen an Belastung und Stabilität zu erfüllen, werden Implantatlängen und Durchmesser innerhalb bestimmter Grenzen verwendet. Ist das Knochenangebot jedoch dafür nicht ausreichend, können unter bestimmten Voraussetzungen auch durchmesser- und/oder längenreduzierte Implantate verwendet werden. Das Verwenden solcher Implantate geht mit einem erhöhten Risiko an Komplikationen einher und ist daher nur in bestimmten Fällen sinnvoll (beispielsweise wenn Knochenaufbauten nicht durchgeführt werden können).
Dieses chirurgische Vorgehen belastet den Patienten weniger als frühere Implantationstechniken und führt selten zu Komplikationen bei der Wundheilung. Zudem haben Schraubenimplantate den Vorteil, dass sie sich durch ihr Gewinde sofort im Knochen „festsetzen“ (primäre Stabilität). Das verkürzt die Einheilzeit, weil nur wenig Knochen „nachwachsen“ muss. Bei einem Teil der Implantate verjüngt sich die zylindrische Grundform apikalwärts, zum Ende hin, sodass insgesamt eine Konusform entsteht.

Hohlzylinderimplantate
[Bearbeiten | Quelltext bearbeiten]Die in den 1980er Jahren[24] entwickelten Hohlzylinderimplantate (auch Körbchenimplantate genannt) sollten die osseointegrierende Oberfläche vergrößern, jedoch haben sie sich nicht bewährt, da der im Zylinder befindliche Knochenanteil mangels ausreichender Durchblutung zu Komplikationen geführt hatte. In veränderter Form als Kurzimplantat mit breitem Durchmesser und mit neuer OP-Technik erleben sie zurzeit eine Renaissance.
Blattimplantate
[Bearbeiten | Quelltext bearbeiten]Neben diesen zylinderförmigen Implantaten mit oder ohne Schraubgewinde gibt es auch flache, blattförmige Implantate (Extensionsimplantate), die entlang des Knochenverlaufes der Kiefer in einen ca. 1 mm breiten, dort hineinpräparierten Schlitz von 4 bis 14 mm Länge eingesenkt werden und dort festwachsen. Diese Implantate haben zusätzlich Durchbohrungen, durch die der Knochen auch horizontal hindurchwachsen kann.
Diskimplantate
[Bearbeiten | Quelltext bearbeiten]Diskimplantate gehören zur Gruppe der BASAL-Implantate. Sie haben die Form eines skelettierten Zylinders und werden seitlich in den Kiefer eingesetzt. Der Halt erfolgt in der harten und gut durchbluteten Außenwand des Knochens. Diskimplantate können unter Umständen sofort belastet werden. Wegen ihrer besonderen Form sollen sie auch bei geringer Knochenhöhe bzw. fortgeschrittenem Kieferabbau eine stabile Einheilung gewährleisten.
Subperiostale Implantate
[Bearbeiten | Quelltext bearbeiten]Die subperiostalen Implantate liegen möglichst großflächig unter der Schleimhaut direkt dem Knochen auf. Sie wurden vor allem bei hochgradigem Knochenschwund eingesetzt, wenn der Kieferknochen für Zylinder- oder Extensionsimplantate zu flach oder zu schmal war. Die bloße Auflagerung des flachen subperiostalen Implantates unter die Knochenhaut (Periost) führte oft zu großflächigen Entzündungen mit z. T. erheblichen ausgedehnten Knocheneinschmelzungen, weil ein wirksamer Infektionsschutz durch einen bakteriendichten Abschluss an der Durchtrittsstelle des Kopfteils naturgemäß fehlt.
Obwohl es in den USA große Erfolge bei subperiostalen Implantaten gibt (über 95 % nach fünfjähriger Verweildauer bei einseitigen Unterkieferimplantaten),[25] ist deren wissenschaftliche Entwicklung in Deutschland nicht weiter vorangetrieben worden. Der Grund liegt im Wesentlichen darin, dass die Erkenntnisse der Knochenbiologie im Hinblick auf die zuverlässige Regeneration des Knochengewebes Möglichkeiten eröffnen, durch geeignete chirurgische Kieferaufbauverfahren auch in Fällen eines knappen Knochenangebotes Zylinderimplantate einzusetzen. Es gibt in Deutschland keinen Hersteller von subperiostalen Gerüstimplantaten.
Material
[Bearbeiten | Quelltext bearbeiten]Titan
[Bearbeiten | Quelltext bearbeiten]
Im Gegensatz zur Orthopädie, in der vornehmlich Titanlegierungen eingesetzt werden, werden Zahnimplantate aus Reintitan hergestellt. Titan weist eine hohe Biokompatibilität auf, die keine allergischen oder Fremdkörperreaktionen auslöst. Titan geht im Gegensatz zu anderen Materialien eine direkte molekulare Verbindung mit dem Knochen ein. Hierbei spielt die raue morphologische Oberflächengestaltung mit einer Mikro-Porentiefe von durchschnittlich 5 bis 100 µm eine Schlüsselrolle. Zu Beginn wurde dies durch Aufspritzen („additives Verfahren“) von Titanpulver unter Argon und Hochtemperatur erreicht (Titan-Plasma-Spray „TPS“).[26] Dieses Verfahren ist verhältnismäßig teuer, so dass viele Hersteller seit etwa dem Jahr 2000 auf das billigere Säure-Ätz-Verfahren („acid etching“ oder Kombinationen davon, „SLA“ genannt) durch ein Gemisch von Salzsäure und Schwefelsäure zurückgreifen („subtraktive Verfahren“), das der additiven Methode gleichwertig oder sogar überlegen gegenübersteht.
Die Eigenschaft des Titans, mit Sauerstoff eine schützende Oxidschicht auf der Oberfläche zu bilden, ist die Ursache für seine besonders gute Verträglichkeit. Beide Methoden weisen eine hohe Erfolgsquote (über 95 % bei einer fünfjährigen Verweildauer) auf. Implantate müssen eine Zertifizierung der Gesundheitsbehörden als sichere Medizinprodukte (CE- oder eine FDA-Zulassung) besitzen. Ausnahmen bestehen gemäß Medizinproduktegesetz (MPG) für Individual-Implantate, die für einen einzigen Patienten auf Verschreibung des Zahnarztes angefertigt werden.
Keramik
[Bearbeiten | Quelltext bearbeiten]Keramikimplantate werden von einer Reihe von Herstellern entwickelt und vertrieben und haben in den letzten zehn Jahren an Popularität gewonnen.[27] Sie sind eine hervorragende Alternative zu Zahnimplantaten aus Titan für die orale Rehabilitation mit vergleichbarem marginalen Knochenverlust und Überlebensrate.[28][29] Zirkonoxidimplantate gelten als ästhetischere Option, insbesondere in Bereichen mit dünnem Zahnfleischgewebe, in denen das Implantat durch den Rand hindurch gesehen werden könnte.[30] Studien haben eine Überlebensrate für Zirkonoxidimplantate von 87 % bis 100 % mit Nachbeobachtungszeiträumen von einem bis 7,8 Jahren berichtet.[31]
Polyetheretherketon
[Bearbeiten | Quelltext bearbeiten]Eine Alternative zu Implantaten aus Titan und Zirkon sind Implantate aus dem Hochleistungspolymer Polyetheretherketon (PEEK).
Indikationen
[Bearbeiten | Quelltext bearbeiten]Die Indikationsklassen implantologischer Versorgungen wurden in einer Konsensuskonferenz implantologisch Tätiger Verbände und Gesellschaften im November 2014 definiert. Die Konsensuskonferenz beschreibt die Indikationsklassen i.S. eines Goldstandards, die sich bewährt haben. Ein Abweichen von diesem Standard ist nicht per se falsch. Es gibt eine Vielzahl von Gründen, aus denen sich ein Patient eine höherwertige implantatgetragene Versorgung nicht leisten will, oder umgekehrt eine Pfeilervermehrung gegenüber der Standardzahl medizinisch notwendig ist.[32]
Die optimale Therapie des Zahnverlustes ist der Ersatz jedes einzelnen Zahnes durch ein Implantat. Dabei ist der 8. Zahn eines Quadranten in der Regel nicht zu ersetzen und die Notwendigkeit des Ersatzes des 7. Zahnes individuell kritisch zu würdigen. Da dieses Optimum aus verschiedensten Gründen (insbesondere anatomische, wirtschaftliche) nicht immer erreicht werden kann, sind die nachfolgenden Regelfallversorgungen aufgestellt.
Klasse I: Einzelzahnersatz
[Bearbeiten | Quelltext bearbeiten]Klasse Ia: Frontzähne
[Bearbeiten | Quelltext bearbeiten]- Wenn bis zu vier Zähne der OK-Front fehlen, die Nachbarzähne klinisch intakt sind: 1 Implantat je fehlendem Zahn.
- Wenn bis zu vier Zähne der UK-Front fehlen, die Nachbarzähne klinisch intakt sind: 2 Implantate sollen die fehlenden Zähne ersetzen.
Klasse Ib: Seitenzähne
[Bearbeiten | Quelltext bearbeiten]- Fehlen im Seitenzahnbereich Zähne aus der geschlossenen Zahnreihe, so soll bei nicht behandlungsbedürftigen Nachbarzähnen jeder fehlende Zahn durch ein Implantat ersetzt werden.
Klasse II: Reduzierter Restzahnbestand
[Bearbeiten | Quelltext bearbeiten]Grundsatz: Bei der implantologischen Versorgung des reduzierten Restgebisses ist die Bezahnung des Gegenkiefers bei der Planung zu berücksichtigen. Darüber hinaus gelten die Regeln der konventionellen Prothetik.
Klasse IIa: Lückengebiss
[Bearbeiten | Quelltext bearbeiten]- Für eine festsitzende Versorgung im Oberkiefer werden 8 Pfeiler benötigt, im Unterkiefer 6 Pfeiler. Natürliche Pfeilerzähne können angerechnet werden, wenn diese an statisch günstiger Position stehen und eine gute Prognose aufweisen.
- Für eine herausnehmbare Versorgung im Oberkiefer werden 6 Pfeiler benötigt, im Unterkiefer 4 Pfeiler. Natürliche Pfeilerzähne können angerechnet werden, wenn diese an statisch günstiger Position stehen und eine gute Prognose aufweisen.
Klasse IIb: Freiende
[Bearbeiten | Quelltext bearbeiten]- Zähne 7 und 8 fehlen: keine Indikation zur Implantation
- Zähne 6–8 fehlen: 1–2 Implantate
- Zähne 5–8 fehlen: 2–3 Implantate
- Zähne 4–8 fehlen: 3 Implantate
Klasse III: Zahnloser Kiefer
[Bearbeiten | Quelltext bearbeiten]Klasse IIIa: Zahnloser Oberkiefer
[Bearbeiten | Quelltext bearbeiten]- Für die Verankerung eines festsitzenden Zahnersatzes im zahnlosen Oberkiefer: 8 Implantate
- Für die Verankerung eines herausnehmbaren Zahnersatzes im zahnlosen Oberkiefer: 6 Implantate
Klasse IIIb: Zahnloser Unterkiefer
[Bearbeiten | Quelltext bearbeiten]- Für die Verankerung eines festsitzenden Zahnersatzes im zahnlosen Unterkiefer: 6 Implantate
- Für die Verankerung eines herausnehmbaren Zahnersatzes im zahnlosen Unterkiefer: 4 Implantate
Die definitive Anzahl der Implantate richtet sich stets nach der jeweiligen Situation und Position der natürlichen Zähne, sodass die endgültige Entscheidung dem Behandler in Absprache mit seinem Patienten obliegt. Neuere Implantatkonzepte ermöglichen ein Abweichen vom definierten Goldstandard mit guten Erfolgen. Beispielsweise wird beim All-on-four-Konzept eine Klasse III mit 4 Implantaten festsitzend versorgt.[33][34][35]
Indikationsverteilung
[Bearbeiten | Quelltext bearbeiten]
Bei teilbezahnten Patienten (> 90 %) sind Implantate die häufigste Indikation, wobei Einzelzahnlücken mit über 50 % die häufigste Indikation für die Implantatbehandlung darstellen. Augmentationstechniken wurden bei rund 40 % der Fälle zusätzlich angewandt in Form von Membrantechnik oder Sinusbodenelevation. Die häufige Anwendung der beiden Augmentationstechniken führt dazu, dass mit 53 % mehr Implantate im Oberkiefer inseriert wurden als im Unterkiefer.[36]
Eine Schweizer Studie der Universität Bern zeigt folgende Verteilung:
- Einzelzahnlücken 51,6 %
- Freiendsituationen 23,5 %
- Schaltlücken 16,9 %
- Zahnlose Kiefer 8 %
Kontraindikationen
[Bearbeiten | Quelltext bearbeiten]Es bestehen zahlreiche Kontraindikationen für eine Implantatversorgung.[37]
Allgemeinmedizinische Kontraindikationen
[Bearbeiten | Quelltext bearbeiten]- Kachexie
- starke Adipositas
- Medikation
- Hämatologische Erkrankungen
- Herz-Kreislauf-Erkrankung
- Kollagenosen
- Osteogenesis imperfecta
- Zustand nach Radiatio
- Unsaniertes Gebiss
- Osteoporose
Bisphosphonate
[Bearbeiten | Quelltext bearbeiten]Etwa seit 1999 ist eine unbeherrschbare Komplikation bei Patienten bekannt, die wegen Osteoporose oder einer Krebserkrankung mit einem Wirkstoff aus der Gruppe der Bisphosphonate behandelt wurden. Nach zahnchirurgischen Eingriffen entsteht eine Atrophie (Rückbildung) des Knochengewebes im Operationsgebiet, selektiv im Bereich des Kieferknochens. Die Ursache ist noch nicht geklärt. Ob es die Kombination von Chemotherapie mit Bisphosphonaten ist, die diese Erscheinung hervorruft, ist noch unbekannt. Derzeit gelten kieferchirurgische Eingriffe aller Art, selbst beispielsweise Zahnextraktionen, bei gleichzeitiger Einnahme von Bisphosphonaten als kontraindiziert. Es ist nicht bekannt, wie lange Bisphosphonate benötigen, bis sie nach ihrer Absetzung ihre destruktive Wirkung im Knochen verlieren. Sie lagern sich ähnlich wie Tetracycline im Knochen ein. Es kann sich um bis zu 10 Jahre handeln, da eine Hydrolysierung über Phosphatasen wegen der Molekülstruktur nicht erfolgt. Die Einnahme von Bisphosphonaten bedarf wegen dieser gravierenden unerwünschten Nebenwirkung einer strengen Indikation. Bei einer umfassenden deutschen Studie aus dem Jahr 2006 wurde festgestellt, dass in Deutschland etwa 780.000 Menschen davon betroffen sind.[38]
Da Bisphosphonate die Knochenneubildung, die Heilung von Knochenverletzungen und die Bildung neuer Gefäße hemmen, heilen Knochenverletzungen im Kiefer in einigen Fällen nicht aus, sondern können sich infizieren und zu einer zunehmenden Kiefernekrose führen.
Knochenqualität
[Bearbeiten | Quelltext bearbeiten]Die Knochenqualität ist von entscheidender Bedeutung für die Osseointegration. Sie resultiert aus dem Verhältnis zwischen der dichten Compacta und der weniger dichten Spongiosa. Letztere ist mit zahlreichen Hohlräumen durchsetzt. Die Spongiosa liegt im Inneren des Knochens und wird nach außen hin von der Kortikalis (Substantia compacta) umhüllt. In den Hohlräumen des von den Spongiosabälkchen gebildeten „Schwammes“ befindet sich das Knochenmark, so dass hier der mechanische Kontakt zum Implantat geringer ist als beim dichten Knochen der Knochenaußenschicht (Compacta). Die Spongiosa ist ein wichtiger Ort der Knochenneubildung und vor allem der Blutbildung.
Die Knochenqualität wird nach Klassen eingeteilt, wobei sich neben der Einteilung nach Carl E. Misch[39] nachfolgende Einteilung durchgesetzt hat:
| Klasse 1 | Fast ausschließlich Kompakta | |
| Klasse 2 | Breite Kompakta | engmaschige Spongiosa |
| Klasse 3 | Dünne Kompakta | engmaschige Spongiosa |
| Klasse 4 | Dünne Kompakta | weitmaschige Spongiosa |
Darüber hinaus kann eine Klassifizierung der Knochenqualität in Hounsfield-Einheiten [HE] erfolgen, woraus die resultierenden Implantateinheilzeiten folgen.[41]
| Knochenqualität | Knochendichte [HE] | Implantateinheilzeit [Monate] |
|---|---|---|
| D1 | 1500 | 3–4 |
| D2 | 500 | 4–5 |
| D3 | 250 | 4–6 |
| D4 | 100 | 6–9 |
Besonderheiten der Knochenbiologie im Frontzahnbereich
[Bearbeiten | Quelltext bearbeiten]Die Ernährung des Gewebes erfolgt im Wesentlichen über die Blutzufuhr. Im Oberkiefer geschieht dies hauptsächlich durch zwei große Arterien (Arteria palatina), die vom hinteren Rand in der seitlichen Kerbe des Oberkiefers beiderseits nach vorne ziehen. Somit wird der Gaumen gut durchblutet, während die vestibuläre Seite des Knochens durch die Zahnreihe hindurch und mittels der wangenseitigen Schleimhaut ernährt werden muss. Diese relative Mangelernährung des Knochens auf der Wangenseite führt auch unter natürlichen Umständen dazu, dass sich die Kontur der Zahnwurzeln in der knöchernen Unterlage des dortigen Zahnfleisches abbildet, vor allem im Eckzahnbereich gut sichtbar. Aus diesem Grunde kann es im Frontzahnbereich nach einer Implantation dazu kommen, dass sich die dünne Alveolenwand zurückbildet, und mit ihr auch das Zahnfleisch. Dies hat unangenehme kosmetische Effekte, so dass man den metallisch-dunklen Implantatkörper, besonders beim Lachen, sehen kann.
Um hier Abhilfe zu schaffen, besann man sich wieder auf die weißen Keramiken, die früher verwendet wurden. Seinerzeit wurden diese Werkstoffe verlassen, weil sie nicht elastisch genug waren und unter der Durchbiegung des Knochens oftmals in der Tiefe brachen. Seit einiger Zeit gibt es ein extrem hartes Material, das Zirkon, das diesen Belastungen standhält und wegen seiner weißen Farbe bei einer eventuellen Rückbildung des Knochens und des Zahnfleisches kosmetisch nicht so störend ist. Leider geht diese Keramik keine dem Titan vergleichbare Verbindung mit dem Knochen ein. Die Erfahrungen mit diesem Werkstoff sind noch nicht ausreichend, um wirklich als Alternative zum Titan zu gelten. Hier muss noch abgewartet werden.
Da die Rückbildung des Knochens in der Front mit der Ernährung des Knochens zusammenhängt, lässt sich dieses Problem jedoch lösen, wenn man ein schmaleres oder anders geformtes Implantat nimmt. Neben Blattimplantaten gibt es einen ebenfalls zylindrisch geformten Implantattyp, der sich dadurch auszeichnet, dass er wie eine Säule von Geldmünzen mit großen Abständen zueinander aussieht. Der Kern ist dabei sehr dünn. Diese Konstruktion hat den Vorteil, dass vor allem in waagerechter Richtung die Ernährung des Knochens gewährleistet ist. Außerdem ist sein oberer Rand kegelförmig abgeschrägt und entspricht damit in der Kontur eher dem zugespitzten Kieferkamm. Dadurch bleibt die Knochenschicht am oberen Rand sehr viel dicker und kann das Zahnfleisch besser ernähren. Der Rückgang des Knochens und der Gingiva im ästhetisch besonders wichtigen Bereich der Front ist somit weniger wahrscheinlich.
Die Ernährung des Knochens in den empfindlichen Frontzahnbereichen wird auch vermindert, wenn zu viele Implantate dort eingesetzt werden, beispielsweise für jeden fehlenden Zahn ein Implantat. Im Gegensatz zum natürlichen Zahn, bei dem eine Ernährungswechselwirkung zwischen Zahn und dem ihn umgebenden Knochen existiert (Tarnow, New York University), fehlt diese Ernährung beim Implantatkörper. Vor allem der dünne Knochenspalt zwischen den Implantaten führt oft dazu, dass sich dieser „Restknochen“ nicht selbst ernährt und dann zugrunde geht. Es kommt also auf das richtige Verhältnis von lebender Substanz zu toter Fremdsubstanz an. Wird der Kieferknochen durch zu viel metallische Fremdsubstanz ersetzt wie bei dicken Implantatzylindern, die zudem auch noch sehr eng stehen, zieht er sich wegen Mangelernährung zurück. Wie dieser Quotient zwischen Knochensubstanz und Metall aber aussehen muss, ist bisher noch nicht definiert und ist damit Gegenstand zukünftiger Untersuchungen. Für den minimalen Abstand zwischen Implantatkörper und ihren die zukünftige Zahnkrone tragenden Pfeilern gilt ein Erfahrungswert von 1,5 bis 2 mm im oberen Bereich an der Durchtrittsstelle durch das Zahnfleisch, und zwar rundherum, also auch lippenseitig. Dieser Wert muss verhältnismäßig oft in der Front unterschritten werden, zumal das natürliche Zahnfach (Alveole) genau dort oft weniger als 1 mm Randdicke hat. Sehr oft zieht sich das Zahnfleisch auch beim natürlichen Zahn gerade dort zurück, wo man es am meisten sieht (scheinbar lange Zähne). Das Implantat vergrößert das Problem.
Abhilfe könnte hier eine ovale statt kreisrunde Implantatform schaffen, wie sie ja auch beim natürlichen Frontzahn gegeben ist. Diese ovale Form würde die Knochenschicht zwischen den Implantaten verbreitern, wenn sie jeweils so gedreht werden, dass die schmalen Kanten nach außen und innen ausgerichtet werden. Damit wäre aber das Problem der zu dünnen knöchernen Außenschicht (lippenseitig) des Implantatlagers weiterhin ungelöst. Das Einbringen dieses ovalen Implantates wäre außerdem für den Behandler schwieriger als bei einem kreisrunden Implantat.
Zweifellos gibt es trotz enormer Erfolge bei Implantaten im Mundbereich noch zahlreiche Verbesserungsmöglichkeiten.
Planung
[Bearbeiten | Quelltext bearbeiten]Die Planung einer Implantation geschieht je nach Komplexität der Situation mittels eines einfachen Zahnröntgens, oder durch Zuhilfenahme weiterer Hilfsmittel. Mit Hilfe einer Computertomographie (CT) oder einer Digitalen Volumentomographie (DVT) kann die Position des Implantats vor dem Eingriff festgelegt werden. Die Planung erfolgt dreidimensional am Computer und wird anhand einer individuell hergestellten Bohrschablone umgesetzt.[42] Nachteilig hierbei sind die Strahlenbelastung und die zusätzlichen Kosten für den Patienten.
Backward-Plannings
[Bearbeiten | Quelltext bearbeiten]Beim Backward-Planning geht die Planung der Implantation nicht von der Kiefer- und Knochensituation aus, sondern vom Zahnersatz. Die Position der Implantate richtet sich sozusagen rückwärts nach der Stellung der neuen implantatgetragenen Zähne. Aufgrund von Abformungen und dreidimensionalen Bilddaten entwickelt das Zahnlabor ein Modell des späteren Zahnersatzes. Anhand dieses Modells ermittelt der Implantologe – mit computergestützter 3D-Implantatplanung – die geeignete Zahl, Position, Länge, Ausrichtung und Bohrtiefe für die Implantate. Auch hier wird die individuelle Knochen- und Weichteilsituation berücksichtigt.[42]
Per Bohrschablone wird für eine präzise Platzierung die digitale Simulation in den Mund übertragen.
- Optimales ästhetisches Erscheinungsbild
- Patienten können ihr Ergebnis im Vorfeld begutachten und Wünsche einbringen
- Hygienefähige Positionierung der Implantate
- Direkt verschraubbare Implantatkronen
Chirurgie
[Bearbeiten | Quelltext bearbeiten]Behandlungszeitpunkt
[Bearbeiten | Quelltext bearbeiten]Man unterscheidet zwischen Sofortimplantaten direkt nach dem Zahnverlust, verzögerten Sofortimplantaten 2–8 Wochen nach Zahnverlust und Spätimplantaten nach vollständiger knöcherner Ausheilung des Zahnfachs. Sofortimplantate sollten nur eingesetzt werden, wenn direkt nach der Extraktion des Zahnes die Alveole entzündungsfrei ist. Verzögerte Sofortimplantationen und Spätimplantationen verringern das Risiko einer Infektion. Bei einwurzeligen Zähnen in Regionen mit dünnen vestibulären Knochenlamellen (beispielsweise im Frontzahngebiet) hat die Sofortimplantation oder verzögerte Sofortimplantation (innerhalb von 2 Wochen) jedoch den Vorteil, dass der Knochenverlust und damit das Risiko eines ästhetischen Misserfolgs minimiert wird.
Sofortimplantate
[Bearbeiten | Quelltext bearbeiten]Unter einem Sofortimplantat versteht man das Einsetzen eines Implantats unmittelbar im Anschluss an die Entfernung oder den Verlust eines eigenen Zahnes in die noch frische (Extraktions-)Wunde (Alveole). Implantatformen, deren unteres Ende verjüngt ist (konische Schraubenimplantate) kommen der natürlichen Wurzelform am nächsten und scheinen insbesondere bei Sofortimplantationen sinnvoll, um die vorhandenen knöchernen Strukturen zu schonen. Die zylinderförmigen, parallelwandigen Implantate gewährleisten eine bessere Primärstabilisierung, weil im Bereich der Spitze des leeren Zahnfachs eine höhere Friktion erreicht wird. Kontrovers wird diskutiert, ob eine Einheilphase vonnöten ist. Für eine sofortige Belastung muss eine ausreichende Knochendichte vorhanden sein.
Operationstechnisch sind konische, wurzelförmige Implantate mit dem Nachteil behaftet, dass die Einsetztiefe durch die Form des Implantats nicht variabel ist und somit den gegebenen anatomischen Verhältnissen nicht immer ausreichend angepasst werden kann. Durch die zunehmende Zahl verschiedener Durchmesser und Längen der Implantate lässt sich auch bei konischen Implantaten eine befriedigende primäre Stabilität erreichen.
Hinsichtlich der Primärstabilität sollen Implantate bei einer Sofortimplantation anguliert eingesetzt werden, um eine optimale Positionierung zu erhalten. Damit kann ein Knochenaufbau teilweise umgangen werden.[43][44] Voraussetzung ist eine gute gesundheitliche Verfassung.
Die Wurzeln von natürlichen Zähnen befinden sich am Außenradius des Kieferknochens. Im Alter erfolgt ein Abbau des Kiefers von außen nach innen, deshalb sollte die Einbringrichtung des Implantates durch ein individuelles Vorbereiten des Implantatbettes hin zum Innenradius des Kiefers erfolgen.
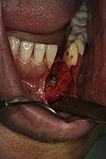
- Ablauf einer Sofortimplantation an einem oberen Schneidezahn mit Versorgung eines Brückenlangzeitprovisoriums.
-
Zahn 11 (mit Krone) vor Extraktion aufgrund einer Wurzelfraktur und Sofortimplantation.
-
Situation nach Entfernen der Zahnkrone 11 mit Wurzelstift.
-
Entfernte Zahnwurzel und Zahnkrone mit Ansicht der Wurzelfraktur.
-
Alveole nach Extraktion der frakturierten Zahnwurzel.
-
Situation nach Bohrung des Implantatbettes in der Extraktionsalveole.
-
Achsenkontrolle und Längenmessung der Implantatbohrung vor Setzen des geplanten Implantates.
-
Gesetzes Implantat in vorgebohrter Extraktionsalveole (mit Einbringpfosten).
-
Inzisale Ansicht des gesetzten Implantates nach Eindrehen der Einheilschraube.
-
Knochenaufbau mit Eigenknochen (gesammelte Bohrspäne). Einbringen in verbliebene Hohlräume und Spalten.
-
Eingeklebtes Brückenprovisorium Regio 11 nach Okklusionskontrolle mit Okklusionspapier (Ansicht von palatinal).
-
Eingeklebtes Brückenprovisorium Regio 11 unmittelbar nach Extraktion und Sofortimplantation.
Ein individuell angefertigtes Implantat soll unmittelbar nach der Extraktion eine oder mehrere Wurzeln eines einzelnen Zahns ersetzen. Da ein individuell angefertigtes Implantat in die frische Alveole passen muss, kann es nur unmittelbar nach einer Zahnextraktion eingesetzt werden.[45][46] Mit den neuen Druckergenerationen lässt sich der extrahierte Zahn scannen und aus Zirkondioxid nachdrucken. Die Genauigkeit für „gedruckte“ definitive Zahnrestaurationen ist derzeit noch nicht ausreichend für eine verlässliche klinische Anwendung. Daher werden experimentell derzeit gefräste CAD/CAM-Lösungen bevorzugt.[47] Einem Review vom August 2018 ist zu entnehmen, dass bislang nur wenige Studien zum mechanischen und biologischen Nutzen sowie keine Langzeitstudien vorliegen.[48] In einer 2020 publizierten Untersuchung der Berliner Charité und dem Universitätsklinikum Freiburg an 28 Patienten wurde eine Überlebensrate der "gedruckten" wurzelanalogen Sofortimplantate (RAI) von 94,4 % nach einem mittleren Beobachtungszeitraum von 18,9 ± 2,4 Monaten ermittelt.[49]
Operationstechnik
[Bearbeiten | Quelltext bearbeiten]Eine zahnärztliche Implantation wird in Lokalanästhesie in der Regel ambulant durchgeführt. An der geplanten Stelle wird nach einem Mukoperiostschnitt die Schleimhaut aufgeklappt und die Implantatbohrung stufenweise nach individuell festgelegter Länge und Durchmesser aufbereitet. Zur Vermeidung einer Überhitzung des Knochens wird die Präparation mit geringer Drehzahl des rotierenden Instrumentes, geringem Druck und permanenter Kühlung mit physiologischer Kochsalzlösung ausgeführt.

Das Implantat wird mit Hilfe eines Drehmomentschlüssels eingebracht. Je nach Knochenqualität sollen dabei bis zu 55 N·cm angewendet werden, um die nötige Primärstabilität zu erreichen. Nach dem Einbringen wird das Zahnfleisch wieder vernäht. Bei entsprechender Nachsorge (kühle Umschläge, Medikamente) lassen sich Komplikationen (Schwellungen usw.) weitgehend vermeiden. Nach zehn Tagen ist die äußere Wundheilung normalerweise abgeschlossen. Eine unbelastete Einheilphase, abhängig von der Knochenqualität, schließt sich an.[23] In der Einheilphase wird ein provisorischer Zahnersatz eingegliedert.
Navigierte Implantologie
[Bearbeiten | Quelltext bearbeiten]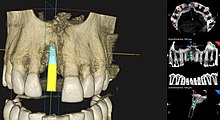
Die navigierte Implantologie ist ein prothetisch-chirurgisches Hilfsverfahren, um das richtige Setzen von Zahnimplantaten in den Kieferknochen zu erleichtern. Die Indikationen und Anwendungseinschränkungen für eine navigierte Implantation sind in den Guidelines der European Association of Osseointegration (EAO)[50] sowie für den deutschsprachigen Raum in der S2-K-Leitlinie der Deutschen Gesellschaft für Zahn-, Mund- und Kieferheilkunde (DGZMK) festgehalten.[51] Die meisten Indikationen beziehen sich auf eine Erweiterung der diagnostischen Möglichkeiten zur dreidimensionalen Darstellung der Kieferknochen und deren Nachbarstrukturen, um vor allem bei einem geringen Knochenangebot oder dessen unklarer Darstellung in den konventionellen Aufnahmetechniken eine verbesserte Einschätzung des OP-Gebietes zu ermöglichen.[42]

Bei einem minimalinvasiven Vorgehen wird das Implantatbett für das Miniimplantat präpariert, ohne einen Mukoperiostlappen zu bilden. Die vereinfachte und kürzere Operation kann eventuelle postoperative Beschwerden reduzieren. Orientierungshilfe bietet eine Bohrschablone.[42]
-
Implantat-Bohrschablone intraoral bei Implantation (Aufsicht)
-
Implantat-Bohrschablone intraoral bei Implantation (Ansicht von vorne)
-
Implantat-Bohrschablone intraoral bei Implantation (Aufsicht)
Knochenaufbau
[Bearbeiten | Quelltext bearbeiten]Unter Kieferkammaufbau oder Kieferaugmentation werden operative Verfahren verstanden, die insbesondere dazu dienen, abgebauten Alveolarknochen in zahnlosen Anteilen des Oberkiefers oder Unterkiefers wieder aufzubauen. Zu diesem Zweck wird Knochenersatzmaterial auf den resorbierten verbliebenen Kieferkamm aufgetragen. Für eine Höhe von mehr als 3 mm werden körpereigene Knochentransplantate am Kieferknochen fixiert und müssen dann monatelang anheilen.[52] Der Knochenabbau des Kieferknochens kann durch Zahnverlust, Parodontitis oder durch den Auflagedruck von Zahnprothesen erfolgen.
Knochenverdichtung
[Bearbeiten | Quelltext bearbeiten]Mit dem Verfahren der Knochenverdichtung (englisch Bone condensing) kann die Stabilität des Zahnimplantats im Kieferknochen erhöht werden, beispielsweise bei Vorliegen eines sehr weitmaschigen Knochens der Klasse 4[53] kann der Einsatz der Knochenverdichtungsmethode zur deutlich besseren primären Stabilität des Zahnimplantats beitragen. Da der Oberkiefer häufig eher in diese Kategorie fällt, wird die Knochenverdichtung fast ausschließlich dort eingesetzt.[54] In Verbindung mit der Sinuslift-Operation findet diese Methode ebenfalls häufig ihre Anwendung.
Nachsorge
[Bearbeiten | Quelltext bearbeiten]Unmittelbar nach einer implantologischen Versorgung soll die Operationsstelle nicht belastet werden. Auch zu intensive Reinigungsmaßnahmen (beispielsweise mit einer harten Zahnbürste) direkt an der Naht sind zu vermeiden, wohingegen das restliche Gebiss sehr sorgfältig gereinigt werden muss. Als zusätzliches Hilfsmittel stehen antiseptische Mundspüllösungen (beispielsweise mit Chlorhexidin) zur Verfügung. So kommt der Infektionsprophylaxe in den ersten 48 Stunden nach der Operation eine Schlüsselrolle zu. Wichtig ist auch, möglichst keine Prothesen im Operationsgebiet zu verwenden oder diese zumindest „hohl zu legen“, weil diese andernfalls unkontrollierte Belastungen auf das Implantat übertragen könnten. Die Dauer der Einheilphase bis zur direkten Belastung des Implantates wird wissenschaftlich derzeit noch diskutiert – mit tendenziell abnehmender Dauer (siehe auch Belastungszeitpunkt) bis hin zur Sofortbelastung.



Zahnimplantate müssen wegen der Infektionsgefahr regelmäßig kontrolliert werden. Rechtzeitig erkannte Infektionen sind deutlich erfolgreicher zu behandeln als fortgeschrittene, die bereits zu einem Abbau von Knochenmaterial geführt haben. Daher sollen Zahnimplantate alle 6 Monate vom behandelnden Zahnarzt bzw. Implantologen kontrolliert werden. In klinischer Erfahrung hat sich gezeigt, dass es insbesondere bei großen kieferchirurgisch-implantologischen Maßnahmen in beiden Kiefern sinnvoll sein kann, den Patienten nach dem Eingriff kurz stationär nachzuversorgen, beispielsweise bei großvolumigen Knochenaufbauten mit Knochentransplantationen aus der Hüfte oder mit Knochenersatzmaterial. Kernpunkt dieser postoperativen Nachsorge ist die Ernährung des Patienten über einen Venenkatheter, um eine bakterielle Gefährdung der frischen Operationswunden im Mund durch die normale orale Nahrungsaufnahme zu vermeiden.
Entfernung des Implantats
[Bearbeiten | Quelltext bearbeiten]Prothetische Versorgung
[Bearbeiten | Quelltext bearbeiten]

Belastungszeitpunkt
[Bearbeiten | Quelltext bearbeiten]Neben dem Operationszeitpunkt nach einer Zahnentfernung ist auch der Belastungszeitpunkt des Implantates von Bedeutung. Man unterscheidet die Sofortbelastung von der Spätbelastung. Die Sofortbelastung setzt Primärstabilität (hohe Festigkeit des Implantates schon bei der Operation) voraus und bedeutet die sofortige Versorgung des Implantates mit der belastenden Suprakonstruktion (Krone, Brücke, herausnehmbare Prothese). Demgegenüber ist für die Spätbelastung die Primärstabilität nicht entscheidend, weil der Knochen in der Einheilzeit (mehrere Wochen bis Monate) das Implantat immer fester umschließt. Je geringer die Primärstabilität des Implantats bei der Operation ist, desto mehr Zeit muss für die Bildung der ausreichenden Knochensubstanz eingeräumt werden. Über die (in Ncm Eindrehmoment) gemessene Primärstabilität gibt es erst seit 2006 Standards.
Provisorischer Zahnersatz
[Bearbeiten | Quelltext bearbeiten]Für die Einheilzeit des Implantats wird bei Bedarf ein provisorischer Zahnersatz eingesetzt.
Festsitzender Zahnersatz
[Bearbeiten | Quelltext bearbeiten]Hierbei werden auf den (meist abschraubbaren) Pfeilern der Implantate Einzelkronen oder Brückenpfeiler zur Schließung einer Zahnlücke durch eine Brücke festgeschraubt oder einzementiert.
Indikationen:
- Einzelzahnersatz oder kleine Schaltlücke (2 fehlende Zähne einer sonst geschlossenen Zahnreihe)
- Große Schaltlücke (mehr als 2 fehlende Zähne der sonst geschlossenen Zahnreihe)
- Freiendsituation (verkürzte Zahnreihe) (festsitzender Zahnersatz nur bedingt möglich)
Einzelzahnersatz oder kleine Schaltlücken
[Bearbeiten | Quelltext bearbeiten]Gründe für einen Zahnverlust können Karies, Pulpitis, Parodontitis, Allgemeinerkrankungen oder ein Unfall sein.
Bei der Nichtanlage von Zähnen muss eine intensive Abstimmung mit einem Kieferorthopäden erfolgen.
Beim Einzelzahnersatz oder Schließen einer kleinen Schaltlücke müssen gegenüber der konventionellen Versorgung mittels einer Brücke die Nachbarzähne nicht beschliffen werden. Eine Krone kann direkt auf das Implantat gesetzt werden. Das Zahnfleisch legt sich bei einer günstigen Ausgangssituation harmonisch an die Krone an und nichts deutet mehr auf den Zahnverlust hin. In ungünstigeren Fällen muss mittels eines parodontalchirurgischen Eingriffs ein Weichgewebsmanagement durchgeführt werden, um einen ästhetisch zufriedenstellenden Übergang vom Zahn zum Gingivalsaum zu erreichen, was vor allem im sichtbaren Bereich von Bedeutung ist.
Probleme beim Einzelzahnersatz können sich ergeben, wenn die Zahnlücke nicht hinreichend groß ist, was bei einem zu geringen Interdentalabstand der Fall ist. Bis ins Jahr 2003 bemühte man sich möglichst lückenfüllende Implantatdurchmesser einzusetzen, um ein ästhetisches Ergebnis zu erzielen. Nachdem dadurch Misserfolge zu verzeichnen waren, wurde dieses Verfahren von der Erkenntnis abgelöst, dass ein ausreichend großer Mindestabstand von etwa 1,5 bis 2 mm zu den benachbarten natürlichen Wurzeln einzuhalten ist.
-
OPT mit Zahnlücke Regio 26 und Kugellmessaufnahme mit Kugeldurchmesser 5 mm
-
Zahnlücke / Schaltlücke Regio 26 (Seitenansicht)
-
Zahnlücke / Schaltlücke Regio 26 (Aufsicht)
-
Röntgenbild eines Zahnimplantates in Regio 26 unmittelbar nach internem Sinuslift
-
Freigelegtes Zahnimplantat Regio 26
-
Verschraubte Implantatkrone mittels CEREC hergestellt
-
Eingesetzte verschraubte Implantatkrone in Regio 26 (Seitenansicht)
-
Eingesetzte verschraubte Implantatkrone in Regio 26 (Aufsicht)
Große Schaltlücken
[Bearbeiten | Quelltext bearbeiten]
Von großen Schaltlücken spricht man, wenn bis zu vier Zähnen in einem Sextanten fehlen und die Lücke jeweils von einem Zahn begrenzt ist.
Um eine solche Lücke mit festsitzendem Zahnersatz zu schließen, bestehen (soweit eine „normale“ Brücke nicht mehr möglich ist) folgende Möglichkeiten:
- Je zu ersetzendem Zahn wird ein Implantat eingesetzt und jeweils mit einer Krone versehen (sehr aufwändig und kostenintensiv).
- Es werden mindestens zwei Implantate als Brückenpfeiler eingesetzt, bei sehr großen Lücken auch mehr als zwei. Auf diesen Implantaten wird dann eine Brücke befestigt (implantatgetragene Brücke).
- Implantate und natürliche Zähne dienen gemeinsam als Brückenpfeiler (Hybrid-Brücke). Das ist nur in Ausnahmefällen zu empfehlen, weil ein Implantat keine Bewegung zulässt, natürliche Zähne innerhalb gewisser Toleranzgrenzen aber beweglich sind (siehe Zahnhalteapparat).
Freiendsituation
[Bearbeiten | Quelltext bearbeiten]Eine Freiendsituation liegt vor, wenn im distalen Bereich kein natürlicher Brückenpfeiler mehr vorhanden ist, der eine Brücke tragen könnte. Durch entsprechend platzierte Implantate ist in diesen Fällen festsitzender Zahnersatz (Brücke) möglich.
Beispiel für eine zementierte Implantatbrücke auf zwei Implantaten im Unterkiefer
-
Eingeheilte Implantate vor Einsetzen einer Implantatbrücke
-
Eingeschraubte Abutments auf Implantaten kurz vor Einsetzen einer Implantatbrücke
-
Eingesetzte Implantatbrücke auf Abutments
Beispiel für eine verschraubte Implantatbrücke auf zwei Implantaten im Unterkiefer
-
Verschraubte Implantatbrücke auf dem Modell
-
Verschraubte Implantatbrücke ohne Modell
-
Verschraubte Implantatbrücke auf dem Modell (Aufsicht)
-
Freigelegte Implantate im Unterkiefer
-
Verschraubte Implantatbrücke auf Unterkiefer-Implantaten
- Beispiel für eine Freiendbrücke auf zwei Implantaten
-
Ausgangssituation: Zwei Implantate in der Region der Zähne 36 und 37 zur Aufnahme einer Freiendbrücke
-
Eingegliederte Freiendbrücke 35–37 von okklusal (in der Aufsicht)
-
Freiendbrücke mit Keramikverblendung, von bukkal, über einen Spiegel fotografiert
Herausnehmbarer Zahnersatz
[Bearbeiten | Quelltext bearbeiten]Implantatpfeiler können ebenso der Verankerung herausnehmbarer Teilprothesen dienen, die mittels Doppelkronen, Stegen, Geschieben, druckknopfähnlichen Kugelköpfchen oder Magneten an den Implantaten befestigt werden können und damit zum sogenannten Kombinierten Zahnersatz werden.
Indikationen:
- Verankerung kombinierten Zahnersatzes
- Verankerung von Deck- oder Cover-Denture-Prothesen (Hybridprothesen) bei zahnlosem Kiefer
Stark reduzierte Bezahnung
[Bearbeiten | Quelltext bearbeiten]Von einer starken Reduzierung der Bezahnung in einem Kiefer spricht man, wenn etwa nur noch 5–6 eigene Zähne vorhanden sind. Die Beurteilung, wann eine Bezahnung als stark reduziert einzustufen ist, ist von der Verteilung der Restbezahnung abhängig, ob nur Frontzähne vorhanden sind oder ob es sich um eine einseitige oder beidseitige Restbezahnung handelt.
In so einem Gebiss dienen Implantate dazu, die Anzahl der Pfeiler zu vermehren, um eine bessere Abstützung und einen sichereren Sitz einer Prothese oder herausnehmbaren Brücke zu gewährleisten. Eine Befestigung mittels Teleskopkronen ist in diesen Fällen eine mögliche Lösung.
Zahnloser Kiefer
[Bearbeiten | Quelltext bearbeiten]Manche Prothesenträger klagen über einen schlechten Sitz ihrer Prothese oder schmerzhafte Druckstellen. Haftmittel oder mechanische Hilfen lösen diese Probleme oft nicht zufriedenstellend. Implantate können in diesen Fällen das Mittel der Wahl sein. Der Tragekomfort einer Prothese kann so verbessert werden.
Die Befestigung von Totalprothesen an Implantaten wird häufiger im zahnlosen Unterkiefer, als im zahnlosen Oberkiefer durchgeführt, weil Unterkieferprothesen auch häufiger Probleme bereiten. Dies liegt an der geringen Saugwirkung und der kleineren Auflagefläche einer Unterkieferprothese. Im Unterkiefer können zwei Implantate genügen, wobei die Kraftverteilung auf vier Implantate von Vorteil ist. Im Oberkiefer sollten aufgrund der weicheren Knochenstruktur mindestens vier Implantate eingesetzt werden.[55]
Die Implantate können über Stegverbindung (eventuell mit Friktionshilfen) miteinander verbunden werden. Das dient sowohl der Stabilisierung der Implantate als auch der besseren Prothesenverankerung. Bei einer guten Primärstabilität ist in bestimmten Fällen eine Sofortbelastung möglich.
Sind etwa 6 bis 8 Implantate vorhanden, kann eine Totalprothese allein auf diesen abgestützt werden. Eine Belastung der Kieferkämme entfällt dann, so dass kein Knochenabbau zu befürchten ist. Bei dieser Anzahl von Implantaten ist alternativ eine festsitzende Zahnersatzversorgung möglich. Ursprünglich als Sozialindikation gedacht, sind inzwischen verschraubte Brücken auf jeweils vier Implantaten im Ober- oder Unterkiefer möglich.[56][57] Dadurch können Kosten und Behandlungsdauer reduziert werden. Die Verweildauer ist bei dieser Art der Versorgung vergleichbar mit dem konventionellen Vorgehen.[58]
Studien vor allem aus Kanada und Deutschland haben gezeigt, dass ein einziges Implantat in einem zahnlosen Kiefer eine deutliche Verbesserung des Tragekomforts einer Totalprothese bringen kann, wenn aus wirtschaftlichen Gründen nicht mehr Implantate möglich sind.[59][60][61]
- Ein Beispiel für eine Oberkiefer-Teilprothese (Kombinierter Zahnersatz) (hier mit 7 Doppelkronen und einem Steg auf 7 Implantaten)
-
Festsitzender Teil der Oberkiefer-Hybridprothese von okklusal gesehen.
-
Oberkiefer-Hybridprothese auf dem Arbeitsmodell von okklusal gesehen. Beachte: Der harte Gaumen ist nicht mit einer Kunststoffplatte bedeckt.
-
Oberkiefer-Hybridprothese auf dem Arbeitsmodell von vestibulär gesehen.
- Ein Beispiel für eine Cover-Denture-Prothese im Unterkiefer (hier auf 4 Implantaten und 2 Stegen)
-
Festsitzender Teil einer Unterkiefer-Hybridprothese von vestibulär gesehen: 4 Implantate und 2 Stege
-
Festsitzender Teil der Unterkiefer-Hybridprothese von okklusal gesehen
-
Die Unterkiefer-Hybridprothese von krestal gesehen. Bei einer Vergrößerung des Bildes kann man deutlich Retentionsstifte erkennen, die der Friktion der Prothese dienen.
- Ein Beispiel für eine Cover-Denture-Prothese im Unterkiefer (hier auf 2 Implantaten mit Kugelköpfchen)
-
2 Implantate im Unterkiefer mit Patrizen zur Befestigung einer Cover-Denture-Prothese
-
Die dazu passende Unterkiefer-Prothese mit den eingearbeiteten Matrizen
-
Die eingegliederte Unterkiefer-Prothese
Bei einem mehrteiligen Implantat wird nach der Einheilphase das Innengewinde des Implantatkörpers frei gelegt und das Abutment, der Kronenanteil auf dem Implantat, eingeschraubt und die Suprakonstruktion gefertigt und eingegliedert. Auf einem einteiligen Implantat kann nach der Einheilphase die Suprakonstruktion unmittelbar angefertigt und eingegliedert werden.
Komplikationen
[Bearbeiten | Quelltext bearbeiten]Im Vordergrund der Komplikationen stehen alle Faktoren, die eine Infektion im Implantationsbereich begünstigen. Zahnimplantate unterliegen der Gefahr einer Periimplantitis, einer Entzündung des Knochengewebes um das Zahnimplantat herum. Die Verbindung zwischen Implantat und Knochen ist nahezu ausschließlich durch bakterielle Einflüsse zerstörbar (Auflösung der Knochenmatrix durch Matrix-Metalloproteasen, MMPs). Die Ursache ist entweder auf Operationsfehler oder auf eine ungenügende Mundhygiene des Patienten zurückzuführen. Die Periimplantitis führt zu einem Knochenabbau, der letztendlich den Ausfall des Implantats bewirkt. Eine Zahnimplantation wird als Misserfolg gewertet, wenn das Implantat mobil ist oder einen periimplantären Gewebsschwund von mehr als 1 mm im ersten Jahr aufweist. Eine Periimplantitis kann durch prophylaktische Maßnahmen zusammen mit einer Antibiotikatherapie behandelt werden. Eine Periimplantitis ist auf einer Röntgenaufnahme zu erkennen.
Bei zusammengesetzten Implantaten befinden sich zwischen dem eigentlichen Implantat und dem Aufbau (Abutment) Spalten und Hohlräume, in die Keime aus der Mundhöhle eindringen können. Später gelangen diese Keime wieder in das angrenzende Gewebe und können so eine Periimplantitis verursachen. Als Prophylaxe sollten diese Implantatinnenräume versiegelt werden.[62]
Mit abnehmender Empfindlichkeit gegenüber bakteriellen Einflüssen bei gleichzeitiger Zunahme des intensiven Implantat-Knochenkontaktes (BIC: bone to implant contact) unter funktionell-physiologischer Kaubelastung sinkt das Risiko des Implantatverlustes, weil die mechanische Belastung zeit- und intensitätsabhängig zu einer röntgenologisch nachweisbaren gesteigerten Mineralisierung des umgebenden Knochens führt. Dies bedeutet, dass in der Anfangszeit nach der Operation sehr viel größere Aufmerksamkeit auf Zahnreinigung und Mundhygiene verwendet werden muss als beispielsweise nach ca. 2 Jahren ereignisloser Tragezeit. Die Verweildauer ist außerdem abhängig von der Größe der implantatgeometrisch bedingten Oberfläche, von der mikromorphologischen Gestaltung und von der äußeren Form.
Diabetiker müssen gut eingestellt sein, damit die Gefahr der Entzündungsneigung an den Zähnen auf ein beherrschbares Maß reduziert wird.
Bei Patienten, die sich einer Chemotherapie unterziehen müssen, ist nicht nur die Immunabwehr eingeschränkt, sondern auch die Regenerationsfähigkeit des Gewebes während der Einheilungsphase nach der Implantation. Daher soll bei diesen Patienten die Beendigung der Chemotherapie abgewartet und erst einige Monate danach implantiert werden.
Bettlägerige Patienten können gegebenenfalls mit Implantaten versorgt werden, wenn der Eingriff stationär durchgeführt wird.
Eine therapierbare Parodontitis ist kein Ausschlusskriterium.[63]
Das Risiko eines Misserfolges ist bei Rauchern erhöht. Ein Misserfolg kann aber auch dann auftreten, wenn das Implantat nicht richtig positioniert wurde.
Die Erfolgssicherheit zylindrisch orientierter Implantate liegt nach internationalen Statistiken im 5-Jahresintervall bei 85–90 %. Sie ist im Wesentlichen vom Eintreten einer Infektion abhängig. Durch geeignete Maßnahmen, die sich der konsequenten Infektionsprophylaxe unmittelbar postoperativ durch stationäre Nachsorge zuwenden, ist es daher möglich, die Erfolgsquote im 10-Jahresintervall auf nahezu 100 % zu steigern (bei Nichtrauchern).
Mit diesen Zahlen gehört die zahnärztliche Implantologie zu den erfolgreichen medizinischen Eingriffen. Die Erfolgsquoten im Bereich der orthopädischen Implantate liegen mit 75 bis 85 % deutlich darunter. Die Gründe liegen in der erhöhten Elektivität zahnärztlicher Implantate. Auch den endogenen Infektionsfaktoren widmet sich die zahnärztliche Implantologie intensiver. Bei orthopädischen Implantaten ließe sich zudem durch verschiedene Änderungen der mikro- und makromorphologischen Aspekte die Erfolgsquote steigern.
Vor- und Nachteile von Zahnimplantaten
[Bearbeiten | Quelltext bearbeiten]Vorteile:
- verringerter Knochenabbau im zahnlosen Kieferkammbereich
- verringerter Druck auf die Schleimhaut bei Teilprothesen
- Beschleifen der Nachbarzähne kann vermieden werden
- verbesserter Halt einer Prothese
- Befestigung Totaler Prothesen als Cover-Denture-Prothese
Nachteile bzw. mögliche Risiken:
- operativer Eingriff erforderlich
- eventuelle Nervenverletzung (insbesondere des Nervus alveolaris inferior im Mandibularkanal des Unterkiefers, Vincent-Symptom)
- eventuelle Eröffnung der Kieferhöhle mit möglicher Sinusitis bei Oberkieferimplantaten
- Da Zahnimplantate starr in den Knochen einwachsen, wird der Kaudruck nicht wie bei natürlichen Zähnen durch die Sharpey-Fasern abgefedert und kann damit zu einer Überbelastung des Kiefergelenks führen.
- kostenintensiv
- höhere Anforderungen an die Mundhygiene
- lange Behandlungsdauer
- Risiko der Periimplantitis
- Risiko der Implantatlockerung und des Implantatverlusts
- Wenn nicht ausreichend Knochen zur Verfügung steht, kann Knochenersatz notwendig sein.
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Literatur
[Bearbeiten | Quelltext bearbeiten]- Ugo Pasqualini, Marco E Pasqualini: Treatise of Implant Dentistry. The Italian Tribute to Modern Implantology. Carimate, Ariesdue 2009, ISBN 88-903821-1-2 (englisch, Digitalisat englische Vollversion [abgerufen am 22. April 2017]).
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Implantat-Versorgung zur oralen Rehabilitation im Zusammenhang mit Kopf-Hals-Bestrahlung. (PDF) S3-Leitlinie, AWMF-Registernummer 007/089, Stand 05/2015.
- Implantatprothetische Versorgung des zahnlosen Oberkiefers. (PDF) S3-Leitlinie, Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften AWMF-Registernummer: 083-010, Stand: November 2014, Gültig bis: November 2019. Abgerufen am 10. April 2017.
- Patienteninformation. (PDF; 140 kB) Bundeszahnärztekammer und Deutsche Gesellschaft für Zahn-, Mund- und Kieferheilkunde
- Grenzen der Zahnimplantologie: Herz-, Kreislauferkrankungen, Blutgerinnung, Diabetes mellitus – Initiative proDente e. V. auf prodente.de
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ enossal im Wiktionary.
- ↑ A. Nedjat, Das PEEK Implantat als Alternative zum Titan. ( vom 2. März 2014 im Internet Archive) In: Implantologie Journal. Zeitschrift der Deutschen Gesellschaft für Zahnärztliche Implantologie. Nr. 06, 2014, S. 8ff.
- ↑ David Soto-Penaloza, Regino Zaragozí-Alonso, María Penarrocha-Diago, Miguel Penarrocha-Diago: The all-on-four treatment concept: Systematic review. In: Journal of Clinical and Experimental Dentistry. Band 9, Nr. 3, 1. März 2017, ISSN 1989-5488, S. e474–e488, doi:10.4317/jced.53613, PMID 28298995, PMC 5347302 (freier Volltext) – (englisch).
- ↑ Amedeo Bobbio: Maya, the first authentic alloplastic, endosseous dental implant. A refinement of a priority. In: Rev Assoc Paul Cir Dent. Band 27, Nr. 1, 1973, S. 27–36, PMID 4620759 (englisch).
- ↑ Abū al-Qāsim Ḫalaf ibn ʿAbbās az-Zahrāwī: مقالة في العمل باليد. University of California Press, 1973, ISBN 978-0-520-01532-6, S. 276 ff. (arabisch, eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Pierre Fauchard: Le Chirurgien Dentiste. (französisch, bnf.fr – Urschrift, Gallica).
- ↑ La méthode curative des Playes, & Fractures de la Teste humaine. 1561 (französisch).
- ↑ H. D. Pape, R. Heiss: [History of tooth transplantation]. In: Karl Schuchardt, Horst Scheunemann (Hrsg.): Transplantationen im Mund-, Kiefer- und Gesichtsbereich (= Fortschritte der Kiefer- und Gesichts-Chirurgie. Band 20). Thieme, 1976, ISBN 3-13-179001-6, ISSN 0071-7916, S. 121–125, PMID 770274.
- ↑ Stephanie Pain: The great tooth robbery. In: New Scientist. Band 2295, 16. Juni 2001 (englisch, historyhome.co.uk [abgerufen am 22. April 2017]).
- ↑ J. Maggiolo: Le manuel de l’art du dentiste, ou, L’État actuel des découvertes modernes sur la dentition: les moyens de conserver les dents en bon état: les mécaniques nouvelles inventées par M. Maggiolo: et tous les détails pratiques et moyens d’exécution des dents artificielles, etc. Wellcome, 1807 (französisch, archive.org [abgerufen am 22. April 2017]).
- ↑ Paolo Zampetti: L’evoluzione dei materiali utilizzati in implantologia. Considerazioni storico-cliniche. In: Odontoiatria. Rivista degli Amici di Brugg. Band 22, Nr. 1, 2003, S. 65–72 (italienisch).
- ↑ Robert J. Rudy, Paul A. Levi, Jr. u. a.: Intraosseous Anchorage of Dental Prostheses – An Early 20th Century Contribution. In: Compendium of Continuing Education in Dentistry. Band 29, Nr. 4, Mai 2008 (englisch, dentalaegis.com [abgerufen am 22. April 2017]).
- ↑ Geschichte der Zahnmedizin ( vom 14. Juli 2016 im Internet Archive), Complete Dental Guide. Abgerufen am 22. April 2017.
- ↑ K. Müller: Kleines Handbuch der oralen Implantologie. 1978, ISBN 3-9800176-2-1.
- ↑ Norbert Schwenzer: Zahnärztliche Chirurgie: 35 Tabellen. Georg Thieme, 2000, ISBN 978-3-13-116963-1, S. 127 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ David L. Hoexter, A tribute to Dr Leonard I. Linkow: A guiding light ( des vom 24. November 2017 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis., Dental Tribune, 22. Dezember 2010. Abgerufen am 23. September 2014.
- ↑ Bruno E. Gysi, Peter Schärer: Schwerpunkte in der oralen Implantologie und Rekonstruktion. Quintessenz, 1983, ISBN 978-3-87652-288-3, S. 143 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Anke K. Brinkmann, Egon L. W. Brinkmann: Die Geschichte der zahnärztlichen Implantologie in Deutschland. Anke-Verlag, Oldenburg 1995, ISBN 3-00-000527-7. (Dissertation, Universität München 1993).
- ↑ L. B. Shulman, T. D. Driskell: Dental Implants: A Historical Perspective. In: M. Block, J. Kent, L. Guerra: Implants in Dentistry. W. B. Saunders, Philadelphia 1997, ISBN 0-7216-2174-0, S. 2.
- ↑ Vgl. auch George Jorge Dietz: Stiftimplantate. 1978.
- ↑ Walter Habel (Hrsg.): Wer ist wer? Das deutsche Who’s who. 24. Ausgabe. Schmidt-Römhild, Lübeck 1985, ISBN 3-7950-2005-0, S. 224.
- ↑ A. Salti: Die 2000jährige Geschichte der Implantation. (PDF; 408 kB) auf zwp-online.info, ZWP, Implantologie Journal, 2003/1, S. 6–8.
- ↑ a b N. Schwenzer, M. Ehrenfeld: Zahn-Mund-Kiefer-Heilkunde. 5 Bände, Band 3: Zahnärztliche Chirurgie. Thieme Verlag, Stuttgart 2000, ISBN 3-13-116963-X.
- ↑ C. M. ten Bruggenkate, K. Müller, H. S. Oosterbeek: Clinical evaluation of the ITI (F-Type) Hollow cylinder implant. In: ITI Hollow cylinder implant. Chapter 6, ISBN 90-90-03708-X, S. 75–83. PMID 2263324
- ↑ Carl E. Misch (Hrsg.): Contemporary implant dentistry.
- ↑ André Schröder, 1976, Bern
- ↑ Lorusso, F. et al., Scientific Trends in Clinical Research on Zirconia Dental Implants: A Bibliometric Review. Materials (Basel), 2020. 13(23).
- ↑ Hashim, D. et al., A systematic review of the clinical survival of zirconia implants. Clin Oral Investig, 2016. 20(7): p. 1403-17.
- ↑ Cionca, N., D. Hashim, and A. Mombelli, Zirconia dental implants: where are we now, and where are we heading? Periodontol 2000, 2017. 73(1): p. 241–258.
- ↑ Pitta, J. et al., A Systematic Review and Meta-Analysis of the Influence of Abutment Material on Peri-implant Soft Tissue Color Measured Using Spectrophotometry. Int J Prosthodont, 2020. 33(1): p. 39–47.
- ↑ Lorusso, F. et al., Scientific Trends in Clinical Research on Zirconia Dental Implants: A Bibliometric Review. Materials (Basel), 2020. 13(23).
- ↑ Indikationsklassen der Konsensuskonferenz Implantologie, Stand: 7. Oktober 2014. Abgerufen am 27. November 2014.
- ↑ David Soto-Penaloza, Regino Zaragozí-Alonso, María Penarrocha-Diago, Miguel Penarrocha-Diago: The all-on-four treatment concept: Systematic review. In: Journal of Clinical and Experimental Dentistry. Band 9, Nummer 3, 2017, S. 474–88, doi:10.4317/jced.53613
- ↑ Abweichungen vom Goldstandard bei dentalen Implantaten abgerufen am 15. Mai 2023
- ↑ Gabriela Sumie Yaguinuma Gonçalves, Keith Murieli Ferreira de Magalhães, Eduardo Passos Rocha, Paulo Henrique Dos Santos, Wirley Gonçalves Assunção: Oral health-related quality of life and satisfaction in edentulous patients rehabilitated with implant-supported full dentures all-on-four concept: a systematic review In: Clinical Oral Investigations. Band 26, Nummer 1, Januar 2022, S. 83–94, doi:10.1007/s00784-021-04213-y
- ↑ Thomas Sulzer, Michael M. Bornstein, Daniel Buser: Aktuelles Indikationsspektrum in der oralen Implantologie an einer Überweisungsklinik. (PDF). In: Schweiz Monatsschr Zahnmed. 2004, Band 114, S. 444–450.
- ↑ G. Hexdecke: Orale Implantologie. ( vom 13. August 2011 im Internet Archive) (PDF; 1,7 MB) uke.de (Universität Hamburg).
- ↑ Felsenberg, D., Hoffmeister, B., Amling, M., Mundlos, S., Seibel, M. J., Fratzl, P.: Kiefernekrosen nach hoch dosierter Bisphosphonattherapie. In: Deutsches Ärzteblatt. Band 103, Nr. 46, 2006, ISSN 0012-1207 (handle.net [abgerufen am 27. Juni 2023]).
- ↑ Carl E. Misch: Density of bone effect on treatment plans, surgical approach, healing and progressive loading. In: Int J Oral Implantol. 1990, 6(2), S. 23–31.
- ↑ U. Lekholm, G. A. Zarb: Patient selection and preparation. In: P. I. Brånemark, G. A. Zarb, T. Albrektsson: Tissue-integrated prostheses-Osseointegration in Clinical Dentistry. Quintessence Publishing, Chicago 1985, S. 199–209.
- ↑ H. B. Engels: Misserfolge in der oralen Implantologie. Ein kleines Brevier zur Vermeidung von Misserfolgen. In: H. B. Engels: Handbuch zum BDIZ / EDI Implantat-Register. Basic.Dent-Verlag, 2003, S. 273–293.
- ↑ a b c d Heinz-Theo Lübbers, Karl Dula: Digitale Volumentomographie. 1st ed. 2021. Berlin, Heidelberg 2021, ISBN 978-3-662-57405-8.
- ↑ Heather J. Conrad: Accuracy of two impression techniques with angulated implants. In: The journal of prosthetic dentistry. Band 97, Nr. 6, 2007, ISSN 0022-3913, S. 349–356, PMID 17618917.
- ↑ Ashok Sethi: Evolution of the concept of angulated abutments in implant dentistry: 14-year clinical data. In: Implant Dentistry. Band 11, Nr. 1, 2002, ISSN 1056-6163, S. 41–51, PMID 11915544.
- ↑ Martin U. Müller, DER SPIEGEL: Ins alte Knochenloch. Abgerufen am 20. September 2021.
- ↑ Bioimplant – ein neues System für die Zahn-Implantologie? Abgerufen am 20. September 2021.
- ↑ Weiß und verschraubt, Dental Magazin, 14. Juni 2018. Abgerufen am 9. Februar 2019.
- ↑ Miguel Pessanha‐Andrade, Mariane B. Sordi, Bruno Henriques, Filipe S. Silva, Review Article: Custom‐made root‐analogue zirconia implants: A scoping review on mechanical and biological benefits, 2. August 2018. Journal of Biomedical Materials Research Part B: Applied Biomaterials, Band 106, Ausgabe 8, S. 2888–2900, doi:10.1002/jbm.b.34147
- ↑ Mats W. H. Böse, Detlef Hildebrand, Florian Beuer, Christian Wesemann, Paul Schwerdtner: Root-analogue implants for immediate implant placement: A retrospective case series. In: Clinical Oral Implants Research. Band 31, S20, 2020, ISSN 1600-0501, S. 275–275, doi:10.1111/clr.213_13644.
- ↑ D. Harris, K. Horner u. a.: E.A.O. guidelines for the use of diagnostic imaging in implant dentistry 2011. A consensus workshop organized by the European Association for Osseointegration at the Medical University of Warsaw. In: Clinical oral implants research. Band 23, Nummer 11, November 2012, S. 1243–1253, ISSN 1600-0501. doi:10.1111/j.1600-0501.2012.02441.x. PMID 22432473.
- ↑ S2k-Leitlinie: Indikationen zur implantologischen 3D-Röntgendoagnostik und navigationsunterstützen Implantologie ( des vom 23. September 2015 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. (PDF) Deutsche Gesellschaft für Zahn-, Mund- und Kieferheilkunde (DGZMK). Abgerufen am 19. Oktober 2014.
- ↑ Norbert Kübler: Implantologie der Mund-, Kiefer- und Plastische Gesichtschirurgie der UKD. Uniklinik Düsseldorf, 12. April 2016, abgerufen am 14. Februar 2019.
- ↑ U. Lekholm U., G. A. Zarb: Patient selection and preparation. In: P. I. Brånemark, G. A. Zarb, T. Albrektsson: Tissue-integrated prostheses-Osseointegration in Clinical Dentistry. Quintessence Publishing. Chicago 1985, S. 199–209.
- ↑ A. Markovi?, D. Calasan u. a.: Implant stability in posterior maxilla: bone-condensing versus bone-drilling: a clinical study. In: Oral surgery, oral medicine, oral pathology, oral radiology, and endodontics. Band 112, Nummer 5, November 2011, S. 557–563, ISSN 1528-395X. doi:10.1016/j.tripleo.2010.11.010. PMID 21330161.
- ↑ Ingrid Grunert: Der Patient ist zahnlos – was tun? (PDF; 114 kB) BZB, 6/2012, S. 52–57.
- ↑ P. Maló, B. Rangert, M. Nobre: „All-on-Four“ immediate-function concept with Brånemark System implants for completely edentulous mandibles: a retrospective clinical study. In: Clinical implant dentistry and related research. Band 5 Suppl 1, 2003, S. 2–9, ISSN 1523-0899. PMID 12691645.
- ↑ C. Mehl, S. Harder, „Feste dritte Zähne“ an einem Tag. In: ZMK aktuell. Band 03, 2015.
- ↑ P. Malo, M. de Araújo Nobre u. a.: A longitudinal study of the survival of All-on-4 implants in the mandible with up to 10 years of follow-up. In: Journal of the American Dental Association (1939). Band 142, Nummer 3, März 2011, ISSN 1943-4723, S. 310–320. PMID 21357865.
- ↑ Joanne N. Walton, Michael Glick, Michael I. MacEntee: A Randomized Clinical Trial Comparing Patient Satisfaction and Prosthetic Outcomes with Mandibular Overdentures Retained by One or Two Implants. In: Int J Prosthodont. Band 22, 2009, S. 331–339.
- ↑ S. Harder, S. Wolfart u. a.: Three-year clinical outcome of single implant-retained mandibular overdentures–results of preliminary prospective study. In: Journal of Dentistry. Band 39, Nummer 10, Oktober 2011, S. 656–661, ISSN 1879-176X. doi:10.1016/j.jdent.2011.07.007. PMID 21821093.
- ↑ Matthias Kern u. a.: Survival and Complications of Single Dental Implants in the Edentulous Mandible following Immediate or Delayed Loading: A Randomized Controlled Clinical Trial. In: Journal of Dental Research. Band 97, Nummer 2, Februar 2018, S. 163–170, ISSN 0022-0345, PMC 6029143 (freier Volltext), doi:10.1177/0022034517736063. PMID 29045800.
- ↑ C. U. Fritzemeier, W. Schmüdderich: Periimplantitisprophylaxe durch Versiegelung der Implantatinnenräume. In: Implantologie. Band 15, Nr. 1, 2007, S. 71–80.
- ↑ Regina Schindjalova: Fast- & Fixed-Therapiekonzept – auch bei Parodontitis profunda. In: Implantologie Journal. Nr. 8/2012, 2012, ISSN 1435-6139, S. 28–32 (oemus.com [PDF; 472 kB]).