Chloressigsäurechlorid
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
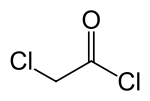
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Chloressigsäurechlorid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C2H2Cl2O | ||||||||||||||||||
| Kurzbeschreibung |
farblose bis gelbliche, stechend riechende Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 112,94 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
1,42 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
105–110 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
in Wasser Zersetzung[1] | ||||||||||||||||||
| Brechungsindex |
1,452–1,454[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 0,05 ml·m−3 bzw. 0,24 mg·m−3[4] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−283,7 kJ/mol[6] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Chloressigsäurechlorid ist eine Chemikalie, genauer die einfach chlorierte Form des Essigsäurechlorids. Die farblose bis leicht gelbliche, stechend riechende Flüssigkeit raucht an feuchter Luft.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Gewonnen werden kann Chloressigsäurechlorid durch Chlorierung von Chloressigsäure mit Phosphortrichlorid, Thionylchlorid, Sulfurylchlorid oder Phosgen.[5] Alternativ kann Vinylidenchlorid mit Sauerstoff in Gegenwart von Radikalinitiatoren (Chlor, UV-Licht) in der Dampfphase zu Chloressigsäurechlorid umgesetzt werden.[7]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Mit Wasser reagiert Chloressigsäurechlorid zu Monochloressigsäure und Chlorwasserstoff.[5]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Chloressigsäurechlorid ist ein wichtiger Baustein für die Synthese organischer Verbindungen, z. B. Pflanzenschutzmitteln, Adrenalin, Diclofenac, Diazepam oder Lidocain.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h Eintrag zu Chloracetylchlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ Eintrag zu Chloressigsäurechlorid bei ChemBlink, abgerufen am 25. Februar 2011.
- ↑ Eintrag zu Chloroacetyl chloride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 79-04-9 bzw. Chloressigsäurechlorid), abgerufen am 2. November 2015.
- ↑ a b c Toxikologische Bewertung von Chloracetylchlorid (PDF) bei der Berufsgenossenschaft Rohstoffe und chemische Industrie (BG RCI), abgerufen am 22. August 2012.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-21.
- ↑ Patent US3674664: Method of preparing chloroacetyl chloride. Angemeldet am 6. März 1970, veröffentlicht am 4. Juli 1972, Anmelder: The Dow Chemical Company, Erfinder: Albert Kent Keller, Eric R. Larsen, Raymond A. Plepys.



