1,4-Dioxan
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | 1,4-Dioxan | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C4H8O2 | |||||||||||||||||||||
| Kurzbeschreibung |
farblose, brennbare, etwas ölige, angenehm riechende Flüssigkeit[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 88,11 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||||||||
| Dichte |
1,03 g·cm−3[1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
101 °C[1] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit |
mischbar mit Wasser, Ethanol, Diethylether und Aceton[1] | |||||||||||||||||||||
| Brechungsindex |
1,422 (20 °C)[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: krebserzeugend (CMR), ernsthafte Auswirkungen auf die menschliche Gesundheit und die Umwelt gelten als wahrscheinlich[5] | |||||||||||||||||||||
| MAK | ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||||||||
1,4-Dioxan ist ein alicyclischer Diether und als solcher eine heterocyclische organische Verbindung.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Die kommerzielle Herstellung von 1,4-Dioxan erfolgt weitestgehend durch säurekatalysierte Dehydratisierung und gleichzeitiger Cyclisierung von Diethylenglycol bei Temperaturen von 130–200 °C und leichtem Unter- bzw. Überdruck von 0,25–1,1 bar.[7]
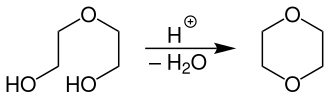
Man verwendet verdünnte Schwefelsäure (bis 5 %), Phosphorsäure, p-Toluolsulfonsäure oder auch stark saure Kationenaustauscher und destilliert das gebildete Dioxan kontinuierlich aus dem Reaktionsgemisch ab. Das Rohprodukt wird neutralisiert und in Rektifikationskolonnen destillativ gereinigt. Bei diesem Prozess sind Ausbeuten im Bereich von 90 % erreichbar.[7]
1,4-Dioxan fällt in großen Mengen als Zwischenprodukt bei der Herstellung von Polyethylenglycol (PEG) und Ethersulfaten wie SLES an.[8][9]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
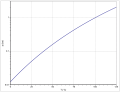
1,4-Dioxan ist eine farblose und niedrigviskose Flüssigkeit, die bei Normaldruck bei 101 °C siedet. Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,58135, B = 1570,093 und C = −31.297 im Temperaturbereich von 293 bis 378 K.[10] In fester Phase existieren zwei unterschiedliche Kristallformen. Bei 0 °C wandelt sich Form II in Form I um, die bei 11 °C schmilzt.[11] Die Umwandlungsenthalpie beträgt 2,351 kJ·mol−1, die Schmelzenthalpie 12,845 kJ·mol−1.[11] Der cyclische Diether ist beliebig mit Wasser mischbar.
Das Molekül liegt wie Cyclohexan oder Pyranosen hauptsächlich in der inversionssymmetrischen Sesselform vor. Für das Dipolmoment von 0,45 D (zum Vergleich: Tetrahydrofuran hat ein Dipolmoment von 1,63 D) sind weitere Konformere, insbesondere die Wannenform verantwortlich.
Dioxan ist mit den meisten organischen Lösungsmitteln und Wasser gut mischbar. Bei Normaldruck wird in dem binären System Dioxan/Wasser bei 82,1 Massenprozent Dioxan ein azeotroper Siedepunkt von 87,6 °C beobachtet.[12]
-
Dampfdruckfunktion von 1,4-Dioxan
-
Binäres Phasendiagramm des Systems 1,4-Dioxan/Wasser
Sicherheitstechnische Kenngrößen
[Bearbeiten | Quelltext bearbeiten]Dioxan bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt bei 11 °C.[2] Der Explosionsbereich liegt zwischen 1,4 Vol.‑% (51 g/m3) als untere Explosionsgrenze (UEG) und 22,5 Vol.‑% (820 g/m3) als obere Explosionsgrenze (OEG).[2] Eine Korrelation der Explosionsgrenzen mit der Dampfdruckfunktion ergibt einen unteren Explosionspunkt von 9 °C sowie einen oberen Explosionspunkt von 58 °C.[2] Der maximale Explosionsdruck beträgt 9,1 bar.[2] Die Grenzspaltweite wurde mit 0,7 mm bestimmt.[2][13] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIB.[13] Die Zündtemperatur beträgt 375 °C.[13] Der Stoff fällt somit in die Temperaturklasse T2. Die elektrische Leitfähigkeit ist mit 5·10−13 S·m−1 sehr gering.[14]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Da 1,4-Dioxan relativ inert und gut mischbar mit anderen Lösungsmitteln ist, findet es Verwendung als Lösungsmittel z. B. bei der Produktion von Klebstoffen, Abbeizmitteln, Farbstoffen, Entfettern, Gewebereinigern und Papier.[15] Als Methylchloroform noch intensiv eingesetzt wurde, war 1,4-Dioxan der übliche Stabilisator (2–8 % Anteil).[16]
Die EU stufte 1,4-Dioxan 2021 als besonders besorgniserregenden Stoff (SVHC) ein.[5]
Auftreten von 1,4-Dioxan in Umwelt und Trinkwasser
[Bearbeiten | Quelltext bearbeiten]In Oder, Main und Rhein wurde der Stoff in Konzentrationen zwischen 0,86 und 2,2 µg/L nachgewiesen, in deutschen Trinkwässern in Konzentrationen bis zu 0,6 µg/L.[17] Im Beobachtungszeitraum 11/2014–09/2015 wurden im Rhein Konzentrationen zwischen 0,5 µg/L und 2 µg/L nachgewiesen; im Mittel waren noch 0,5 µg/L im Uferfiltrat vorhanden.[18] Der Stoff kann mittels der üblicherweise eingesetzten technischen Methoden der Wasseraufbereitung (Ozonung, Aktivkohlebehandlung) nicht entfernt werden.[19] 2016 wurden in der Alz[20] erhöhte Gehalte an 1,4-Dioxan nachgewiesen. Die Hauptemittenten (Hersteller von Papier, Kunstfasern und Tensiden) wurden identifiziert und Gegenmaßnahmen eingeleitet.[19] Die bislang höchste nachgewiesene Konzentration von 1,4-Dioxan in einem bayerischen oberflächenwasserbeeinflussten Brunnen lag bei 2,4 μg/L.[15]
In Deutschland gilt ein Trinkwasserleitwert von 5 µg/L, der nicht überschritten werden sollte.[19] In den USA hingegen wird eine health-based reference concentration von 0,35 µg/L angewendet.[21] Ein umfangreiches Monitoring der öffentlichen Trinkwasserversorgung in den USA (~35.000 Proben, 4864 Trinkwassersysteme) ergab eine Detektionshäufigkeit von 21 % und in 6,9 % wurde eine Überschreitung der abgeleiteten Referenzkonzentration von 0,35 µg/L festgestellt.[21]
Gesundheitliche Aspekte
[Bearbeiten | Quelltext bearbeiten]Da 1,4-Dioxan als Zwischenprodukt der Synthese von Natriumdodecylpoly(oxyethylen)sulfat anfällt, kann es auch in messbaren Mengen in Kosmetikprodukten wie Shampoo oder Zahnpasta vorkommen. Eine krebserregende Wirkung ist bisher weder sicher nachgewiesen noch sicher auszuschließen.[22] Das National Toxicology Program des amerikanischen Bundesgesundheitsministeriums kommt zu dem Schluss, die Substanz sei „reasonably anticipated to be a human carcinogen based on sufficient evidence of carcinogenicity from studies in experimental animals“, stehe also in dem begründeten Verdacht, in Menschen karzinogen zu sein, nachdem entsprechende Effekte in Tieren nachgewiesen worden sind. Laut amerikanischer Arzneimittelbehörde FDA sind jedoch die gemessenen Werte in Produkten für Endkonsumenten sowohl unbedenklich als auch im Vergleich zur Vergangenheit – aufgrund verbesserter Herstellungsverfahren – rückläufig.[23]
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g Eintrag zu 1,4-Dioxan. In: Römpp Online. Georg Thieme Verlag, abgerufen am 26. Mai 2014.
- ↑ a b c d e f g h i j k l Eintrag zu 1,4-Dioxan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ Datenblatt 1,4-Dioxan bei Sigma-Aldrich, abgerufen am 5. März 2011 (PDF).
- ↑ Eintrag zu 1,4-dioxane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 7. Dezember 2022. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ a b Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 11. Juli 2021.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 123-91-1 bzw. 1,4-Dioxan), abgerufen am 2. November 2015.
- ↑ a b Kenneth S. Surprenant: Dioxane. In: Ullmann’s Encyclopedia of Industrial Chemistry. Wiley‐VCH Verlag, 15. Juni 2000, doi:10.1002/14356007.a08_545.
- ↑ 1,4-Dioxan: Was tun?, PROCESS 4-2006.
- ↑ Lead the charge to reformulate for 1,4-Dioxane limits, BASF US.
- ↑ J. L. Crenshaw, A. C. Cope, N. Finkelstein, R. Rogan: The Dioxanates of the Mercuric Halides. In: J. Am. Chem. Soc. 60, 1938, S. 2308–2311, doi:10.1021/ja01277a010.
- ↑ a b C. J. Jacobs, G. S. Parks: Thermal data on organic compounds. XIV. Some heat capacity, entropy and free energy data for cyclic substances. In: J. Am. Chem. Soc. 56, 1934, S. 1513–1517, doi:10.1021/ja01322a020.
- ↑ C. H. Schneider, C. C. Lynch: The Ternary System: Dioxane-Ethanol-Water. In: J. Am. Chem. Soc. 65 (6), 1943, S. 1063–1066, doi:10.1021/ja01246a015.
- ↑ a b c E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen. Band 1: Brennbare Flüssigkeiten und Gase. Wirtschaftsverlag NW – Verlag für neue Wissenschaft, Bremerhaven 2003.
- ↑ Technische Regel für Gefahrstoffe TRGS 727, BG RCI Merkblatt T033 Vermeidung von Zündgefahren infolge elektrostatischer Aufladungen, Stand August 2016, Jedermann-Verlag Heidelberg, ISBN 978-3-86825-103-6 (PDF).
- ↑ a b LfU Bayern: PM 44/16: Umweltmonitoring wird ausgeweitet, 30. November 2016.
- ↑ Thomas K.G. Mohr, Santa Clara Valley Water District: Solvent Stabilizers White Paper, 14. Juni 2001.
- ↑ Daria K. Stepien, Peter Diehl, Johanna Helm, Alina Thoms, Wilhelm Püttmann: Fate of 1,4-dioxane in the aquatic environment: from sewage to drinking water. In: Water Research. Band 48, 1. Januar 2014, S. 406–419, doi:10.1016/j.watres.2013.09.057, PMID 24200013.
- ↑ Arbeitsgemeinschaft Rhein-Wasserwerke e. V.: Jahresbericht 2015. Hrsg.: Geschäftsstelle der Arbeitsgemeinschaft Rhein-Wasserwerke e. V. 2015 (riwa-rijn.org [PDF]).
- ↑ a b c Heinz Rüdel, Wolfgang Körner, Thomas Letzel, Michael Neumann, Karsten Nödler: Persistent, mobile and toxic substances in the environment: a spotlight on current research and regulatory activities. In: Environmental Sciences Europe. Band 32, Nr. 1, Dezember 2020, S. 5, doi:10.1186/s12302-019-0286-x.
- ↑ 1,4-Dioxan. LfU Bayern, abgerufen am 5. August 2022.
- ↑ a b David T. Adamson, Elizabeth A. Piña, Abigail E. Cartwright, Sharon R. Rauch, R. Hunter Anderson: 1,4-Dioxane drinking water occurrence data from the third unregulated contaminant monitoring rule. In: Science of the Total Environment. Band 596–597, 15. Oktober 2017, S. 236–245, doi:10.1016/j.scitotenv.2017.04.085, PMID 28433766.
- ↑ BASF: Lead the charge to reformulate for 1,4-Dioxane limits, abgerufen am 9. Januar 2023.
- ↑ FDA: 1,4-Dioxane in Cosmetics: A Manufacturing Byproduct, abgerufen am 9. Januar 2023.