Europium(III)-oxid
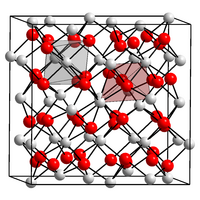
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| _ Eu3+ _ O2− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Europium(III)-oxid | |||||||||||||||
| Andere Namen |
Europiumsesquioxid | |||||||||||||||
| Verhältnisformel | Eu2O3 | |||||||||||||||
| Kurzbeschreibung |
weißer bis hellrosafarbener geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 351,92 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
7,42 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
4118 °C[1] | |||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Europium(III)-oxid ist eine chemische Verbindung aus der Gruppe der Oxide des Europiums.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Nach der aufwendigen Abtrennung der anderen Lanthanoide aus deren Erzen wird letztendlich Europium(III)-oxalat Eu2(C2O4)3·10 H2O gewonnen, das anschließend zu Europiumoxid Eu2O3 verglüht wird.
Um Nanokristalle des Materials zu erhalten, wird eine Synthese durch Kalzinierung des entsprechenden Hydroxids oder Oxalates verwendet.[3]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
Europium(III)-oxid ist ein hygroskopischer weißer bis hellrosafarbener geruchloser Feststoff, der praktisch unlöslich in Wasser ist.[1] Es besitzt eine monokline Kristallstruktur.[3]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Es findet als Dotierungsmittel für Kathodenstrahlröhren Verwendung, in Plasmabildschirmen wandelt es Ultraviolettstrahlung in sichtbares Licht um. Die Fluoreszenz wird ebenfalls als Sicherheitsmerkmal auf Eurobanknoten genutzt.[4]
Durch Reduktion von Europium(III)-oxid mit elementarem Europium und Siliciumdioxid bei 1100 °C kann Europium(II)-silicat hergestellt werden.[5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h Eintrag zu CAS-Nr. 1308-96-9 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 25. Januar 2012. (JavaScript erforderlich)
- ↑ a b Datenblatt Europium(III) oxide, 99.999 % trace metals basis bei Sigma-Aldrich, abgerufen am 25. Januar 2012 (PDF).
- ↑ a b Ginya Adachi, Nobuhito Imanaka, Zhen Chuan Kang: Binary rare earth oxides. 2004, Springer Netherlands, ISBN 978-1-4020-2568-6, S. 138 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Hermann Sicius: Seltenerdmetalle: Lanthanoide und dritte Nebengruppe: Eine Reise durch das Periodensystem. Springer-Verlag, 2015, ISBN 978-3-658-09840-7, S. 44.
- ↑ C. Funk, J. Köhler, I. Lazar, D. Kajewski, K. Roleder, J. Nuss, A. Bussmann-Holder, H. Bamberger, J. van Slageren, D. Enseling, T. Jüstel, T. Schlei: Old and New Insights into Structure and Properties of Eu2[SiO4]. In: Crystal Growth & Design. Band 18, Nr. 10, 3. Oktober 2018, S. 6316–6325, doi:10.1021/acs.cgd.8b01265.

