Ammoniumhydrogensulfat
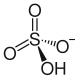
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Ammoniumhydrogensulfat | |||||||||||||||
| Andere Namen |
Ammoniumbisulfat | |||||||||||||||
| Summenformel | NH4HSO4 | |||||||||||||||
| Kurzbeschreibung |
weißer geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 115,10 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
1,79 g·cm−3 (bei 20 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
leicht in Wasser (ca. 1000 g·l−1 bei 20 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Ammoniumhydrogensulfat ist ein Ammoniumsalz der Schwefelsäure. Es besitzt die Formel NH4HSO4.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Ammoniumhydrogensulfat entsteht bei Zersetzung von Ammoniumsulfat bei Temperaturen über 100 °C, wobei Ammoniak frei wird. Ammoniumhydrogensulfat entsteht in großen Mengen als Abscheidungsprodukt in Aktivkoks-Filteranlagen für Schwefeldioxid-haltige industrielle Abgase. Die Filter werden mit Sauerstoff, Ammoniak und Wasserdampf beschickt, wobei über Schwefelsäure das Hydrogensulfat und auch Ammoniumsulfat entstehen:[3]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Ammoniumhydrogensulfat bildet weiße, monokline, hygroskopische Kristalle.[4] Die Substanz zersetzt sich bei Temperaturen über 120 °C, wobei Schwefeloxide, Stickoxide und Ammoniak frei werden. Die Lösung von 100 g Ammoniumhydrogensulfat in 1 l Wasser zeigt bei 20 °C einen pH-Wert von 1,[5] liegt also im stark sauren Bereich.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Verwendung findet es zur Herstellung von Ammoniumperoxodisulfat,[6] als Zusatzstoff in Stickstoffdünger,[7] zur Bekämpfung von Waldbränden als viskose Lösung/Suspension in Wasser und zur Herstellung von Ammoniumalaun und Flammschutzmitteln für Cellulose-Produkte.[1]
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Ammoniumhydrogensulfat ist als schwach wassergefährdend (WGK 1) eingestuft.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Eintrag zu Ammoniumhydrogensulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ Eintrag zu Ammoniumhydrogensulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Oktober 2022. (JavaScript erforderlich)
- ↑ Heinz Brauer (Hrsg.): Handbuch des Umweltschutzes und der Umweltschutztechnik: Band 3: additiver Umweltschutz: Behandlung von Abluft und Abgasen. Springer, 1996, ISBN 978-3-540-58060-7, S. 577.
- ↑ Jean D’Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale. 4. Auflage, Springer, 1997, ISBN 978-3-540-60035-0, S. 596.
- ↑ Datenblatt Ammoniumhydrogensulfat (PDF) bei Carl Roth, abgerufen am 14. Dezember 2010.
- ↑ Arnold Willmes: Taschenbuch chemische Substanzen: Elemente - Anorganika - Organika - Naturstoffe - Polymere. 3. Auflage, Harri Deutsch Verlag, 2007, ISBN 978-3-8171-1787-1, S. 115.
- ↑ Patentanmeldung DE4126806A1: Verfahren zur Herstellung von granuliertem Ammoniumsulfat. Angemeldet am 9. August 1991, veröffentlicht am 11. Februar 1993, Anmelder: Leuna Werke AG, Erfinder: Wolfgang Ermischer et al.



