4-Pyridincarbaldehyd
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
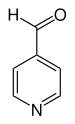
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 4-Pyridincarbaldehyd | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C6H5NO | ||||||||||||||||||
| Kurzbeschreibung |
klare, hellgelbe Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 107,04 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,137 g·cm−3 (bei 20 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
wenig in Wasser löslich (20 g·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
4-Pyridincarbaldehyd (Trivialname Isonicotinaldehyd) ist eine chemische Verbindung, die sich von der Isonicotinsäure ableitet. Es handelt sich um ein Pyridin-Derivat.
Geschichte
[Bearbeiten | Quelltext bearbeiten]Roderich Graf synthetisierte bereits 1936 das Phenylhydrazon von 4-Pyridincarbaldehyd. Allerdings beschrieb er nicht den freien Aldehyd. Das Phenylhydrazon erhielt er aus 2-Picolylamin[3] durch eine Kondensationsreaktion mit Nitrosobenzol in Ethanol (Baeyer-Mills-Reaktion).[4]

Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Der freie Aldehyd wurde erstmals 1951 von Brown et al. synthetisiert. Die Synthese ist analog zu der Synthese von 2-Pyridincarbaldehyd nach Dyson und Hammick. Das Edukt 4-Picolin wird dabei erst in einer Lösung von Kaliumacetat und Acetanhydrid in Essigsäure dreifach chloriert und dann mit Zinn in wässrig / acetoniger Salzsäure zum geminalen Dichlorid (Ketochlorid) reduziert. Die durch Silbernitrat unterstützte Hydrolyse des Ketochlorids liefert den Aldehyd.[5]

Derartige Synthesen aus dem Bereich der klassischen organischen Chemie sind allerdings seit bekanntwerden der Sauermilch-Oxidation obsolet, weil durch diese die das Edukt direkt mit Sauerstoff zum Aldehyd oxidiert werden kann.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]4-Pyridincarbaldehyd hat einen Flammpunkt von 77,8 °C und eine Selbstentzündungstemperatur von 185 °C. Der Octanol-Wasser-Verteilungskoeffizient beträgt bei 30 °C [1]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h Datenblatt 4-Pyridincarbaldehyd bei Sigma-Aldrich, abgerufen am 7. Juli 2022 (PDF).
- ↑ a b Eintrag zu Isonicotinaldehyd in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Januar 2024. (JavaScript erforderlich)
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 1-(4-Pyridinyl)methanamin: CAS-Nr.: 3731-53-1, EG-Nr.: 223-092-6, ECHA-InfoCard: 100.020.993, PubChem: 77317, ChemSpider: 69736, Wikidata: Q27463887.
- ↑ R. Graf: Über die Pyridyl-amino-methane. In: Journal für Praktische Chemie. Band 146, Nr. 1-4, 1936, S. 88–104, doi:10.1002/prac.19361460108.
- ↑ B. R. Brown, D. Ll. Hammick, B. H. Thewlis: 256. ω-Halogenomethyl-pyridines,-quinolines, and-iso quinolines. Part I. Preparation. In: Journal of the Chemical Society (Resumed). 1951, S. 1145–1149, doi:10.1039/JR9510001145.


