Tetrafluormethan
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
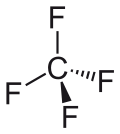
| ||||||||||||||||
| Keile zur Verdeutlichung der Geometrie | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Tetrafluormethan | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | CF4 | |||||||||||||||
| Kurzbeschreibung |
geruch- und farbloses Gas[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 88,01 g·mol−1 | |||||||||||||||
| Aggregatzustand |
gasförmig | |||||||||||||||
| Dichte |
3,72 kg·m−3 (15 °C, 1013 mbar)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | ||||||||||||||||
| Löslichkeit |
schwer in Wasser (20 mg·l−1 bei 20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Treibhauspotential |
7349 (bezogen auf 100 Jahre)[4] | |||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−933,6 kJ/mol[5] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Tetrafluormethan (auch Tetrafluorkohlenstoff) ist eine chemische Verbindung aus der Reihe der Fluorkohlenwasserstoffe. Bei ihm sind alle Wasserstoffatome des Methans durch Fluoratome substituiert. Beide Bezeichnungen sind nach der IUPAC-Nomenklatur korrekt, abhängig davon, ob die Verbindung als organische (Tetrafluormethan) oder anorganische (Tetrafluorkohlenstoff) Verbindung angesehen wird.
Geschichte
[Bearbeiten | Quelltext bearbeiten]Die Verbindung wurde erstmals im Jahr 1926 von den französischen Chemikern Paul Lebeau und Augustin Damiens hergestellt[6] und 1930 charakterisiert.[7][8]
Vorkommen
[Bearbeiten | Quelltext bearbeiten]Tetrafluormethan entsteht in der Atmosphäre bei der UV-Photolyse von Trifluoracetylfluorid, das wiederum ein Abbauprodukt von in der Atmosphäre vorhandener Halogenkohlenwasserstoffe ist.[9]
Große Mengen Tetrafluormethan werden bei der Aluminiumerzeugung freigesetzt. Dies ist darauf zurückzuführen, dass beim Hall-Héroult-Prozess Graphit-Elektroden und Kryolith als Flussmittel (eutektische Schmelzpunkterniedrigung) zum Einsatz kommen – durch Reaktion des Fluors im Kryolith mit dem Kohlenstoff der Elektroden entsteht Tetrafluormethan.[10]
Darstellung
[Bearbeiten | Quelltext bearbeiten]Tetrafluormethan kann einerseits durch Verbrennung von Kohlenstoff in Fluor, andererseits durch elektrische Entladung in einem Kohlenstoffmonoxid-Fluorgemisch dargestellt werden:[11]
Eine weitere Methode ist die Umsetzung von Siliciumcarbid mit Fluor zu Tetrafluormethan und Siliciumtetrafluorid:[12]
Die Umsetzung ist nahezu quantitativ, und die gasförmige Siliciumverbindung kann aus dem Gasgemisch durch Waschen mit einer Natriumhydroxidlösung (Hydrolyse) entfernt werden.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Tetrafluormethan ist ein farb- und geruchloses Gas mit einem Schmelzpunkt von −184 °C und einem Siedepunkt von −128 °C. Tetrafluormethan ist in Wasser sehr schlecht (20 mg pro kg Wasser bei 20 °C[3]) löslich, in Ethanol (ca. 80 mg pro kg Ethanol bei 25 °C[13]) und Benzol (ca. 64 mg pro kg Benzol bei 25 °C[14]) etwas besser.
Chemische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Tetrafluormethan ist sehr reaktionsträge und wird von Säuren und Laugen nicht angegriffen. Lediglich siedende Alkalimetalle und heiße Alkalimetalldämpfe vermögen es langsam anzugreifen.[12] Durch thermische Zersetzung mit (Luft-)Sauerstoff oberhalb 1000 °C entstehen giftige Stoffe (Carbonylfluorid, Kohlenstoffmonoxid), in Gegenwart von Wasser auch der aggressive Fluorwasserstoff.
Es besitzt ein Treibhauspotenzial von 7349[4] und ist damit ein extrem starkes Treibhausgas.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Tetrafluormethan wird als Kältemittel verwendet, jedoch wegen seines kritischen Punktes von −45,5 °C nur für sehr tiefe Temperaturen eingesetzt.[15] Es hat zwar keine abbauende Wirkung auf die Ozonschicht, aufgrund des hohen Treibhauspotenzials wird jedoch in der F-Gase-Verordnung festgelegt, dass Anlagen mit den entsprechenden Gasen möglichst geringe Leckmengen abgeben sollen.
In seltenen Fällen wird es in der Fahrzeugindustrie auch als Gas für hydropneumatische Federungen verwendet.[16]
Tetrafluormethan wird auch beim Plasmaätzverfahren von Silicium in der Elektronikindustrie eingesetzt, wobei das Gas in einer Hochfrequenzentladung bei einem Druck von 0.1–1.0 hPa teilweise in CF3−-Ionen und Fluor zersetzt wird.[17]
Toxikologie
[Bearbeiten | Quelltext bearbeiten]Tetrafluormethan gilt als ungiftig. Es kann jedoch in geschlossenen Räumen durch Verdrängen der Luft zur Erstickung führen. Bei geringeren Konzentrationen ist eine narkotische Wirkung möglich.[2] Da Tetrafluormethan dichter als Luft ist, sammelt es sich am tiefsten zugänglichen Punkt entsprechender Räume an.
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e Eintrag zu Tetrafluormethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- ↑ a b c d Datenblatt Tetrafluoromethane bei Air Liquide.
- ↑ a b B. A. Cosgrove, J. Walkley: Solubilities of gases in H2O and 2H2O. in: J. Chromatogr. A 216, 1981, S. 161–167; doi:10.1016/S0021-9673(00)82344-4.
- ↑ a b G. Myhre, D. Shindell et al.: Climate Change 2013: The Physical Science Basis. Working Group I contribution to the IPCC Fifth Assessment Report. Hrsg.: Intergovernmental Panel on Climate Change. 2013, Chapter 8: Anthropogenic and Natural Radiative Forcing, S. 24–39; Table 8.SM.16 (PDF).
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-19.
- ↑ Rolf Werner Soukup: Chemiegeschichtliche Daten anorganischer Substanzen, Version 2020, S. 85 pdf.
- ↑ P. Lebeau und A. Damiens, Comt. Rend. 182 (1926) 1340.
- ↑ P. Lebeau und A. Damiens, Comt. Rend. 191 (1930) 939.
- ↑ Aaron M. Jubb, Max R. McGillen, Robert W. Portmann, John S. Daniel, James B. Burkholder: An atmospheric photochemical source of the persistent greenhouse gas CF4. In: Geophysical Research Letters. Band 42, Nr. 21, 2015, S. 9505–9511, doi:10.1002/2015GL066193.
- ↑ Jürgen Feßmann, Helmut Orth: Angewandte Chemie und Umwelttechnik für Ingenieure. ecomed, 2002, ISBN 978-3-609-68352-2, S. 95 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ G. Brauer (Hrsg.): Handbook of Preparative Inorganic Chemistry. 2. Auflage, Band 1, Academic Press 1963, S. 203–204.
- ↑ a b Homer F. Priest: Anhydrous metal fluorides. In: Ludwig F. Audrieth (Hrsg.): Inorganic Syntheses. Band 3. McGraw-Hill, Inc., 1950, S. 171–183 (englisch).
- ↑ Shiqing Bo, Rubin Battino, Emmerich Wilhelm: The Solubility of Gases in Liquids. 19. The Solubility of He, Ne, Ar, Kr, Xe, CH4, CF4, SF6 in Normal 1-Alkanols n-CIH2I+1OH (1 ≤ I ≤ 11) at 298.15 K. In: J. Chem. Eng. Data Band 38, Nr. 4, 1993, S. 611–616; doi:10.1021/je00012a035.
- ↑ Graham Archer, Joel H. Hildebrand: The Solubility and Entropy of Solution of Carbon Tetrafluoride and Sulfur Hexafluoride in Nonpolar Solvents. In: J. Phys. Chem. Band 67, Nr. 9, 1963, S. 1830–1833; doi:10.1021/j100803a021.
- ↑ Johann Kuprianoff, Rudolf Plank, Heinz Steinle: Die Kältemittel. Springer Berlin Heidelberg, 2013, ISBN 978-3-642-86286-1, S. 363 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ W. Bauer: Hydropneumatische Federungssysteme. Springer Berlin Heidelberg, 2007, ISBN 978-3-540-73641-7, S. 106 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Ralf Steudel: Chemie der Nichtmetalle. De Gruyter, 2013, ISBN 978-3-11-030797-9, S. 268 (eingeschränkte Vorschau in der Google-Buchsuche).



