2-Hexanon
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 2-Hexanon | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C6H12O | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit acetonähnlichem, stechenden Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 100,16 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||
| Dichte |
0,81 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
128 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
schlecht in Wasser (17 g·l−1 bei 25 °C)[1] | |||||||||||||||
| Brechungsindex |
1,401 (20 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
Schweiz: 5 ml·m−3 bzw. 21 mg·m−3[4] | |||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
2-Hexanon oder auch Butylmethylketon ist eine farblose Flüssigkeit aus der Gruppe der Ketone.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]
Natürlich kommt 2-Hexanon in Ysop, Spanischem Pfeffer und Pelargonium graveolens vor.[5]
Herstellung
[Bearbeiten | Quelltext bearbeiten]2-Hexanon kann im Labormaßstab durch Hydratisierung von 1-Hexin hergestellt werden:[6]

Durch Oxidation von 2-Hexanol entsteht ebenfalls 2-Hexanon:
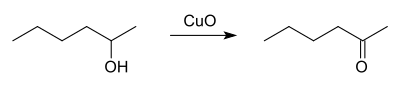
Eine weitere Synthese ist durch eine Grignard-Reaktion mit Acetonitril und Butylmagnesiumbromid möglich:
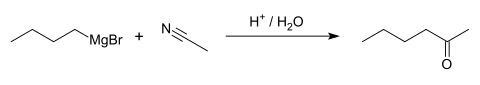
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]2-Hexanon bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von 23 °C.[1][7] Der Explosionsbereich liegt zwischen 1,2 Vol.‑% (50 g/m3) als untere Explosionsgrenze (UEG) und 9,4 Vol.‑% als obere Explosionsgrenze (OEG).)[1][7] Hier ergibt sich ein oberer Explosionspunkt von 51 °C.[1] Die Grenzspaltweite wurde mit 0,98 mm bestimmt.[1][7] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIA.[7] Die Zündtemperatur beträgt 420 °C.[1][7] Der Stoff fällt somit in die Temperaturklasse T2.
Verwendung
[Bearbeiten | Quelltext bearbeiten]2-Hexanon wird als Lösungsmittel für Farbstoffe verwendet.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j k l m n o p q r Eintrag zu 2-Hexanon in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ Datenblatt 2-Hexanone, reagent grade, 98% bei Sigma-Aldrich, abgerufen am 7. Juli 2019 (PDF).
- ↑ Eintrag zu Hexan-2-one im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 591-78-6 bzw. 2-Hexanon), abgerufen am 2. November 2015.
- ↑ 2-HEXANONE (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 28. Juli 2024.
- ↑ Autorengemeinschaft: Organikum, 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, S. 266.
- ↑ a b c d e E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen. Band 1: Brennbare Flüssigkeiten und Gase. Wirtschaftsverlag NW – Verlag für neue Wissenschaft, Bremerhaven 2003.


