Molekül

Moleküle [] (älter auch: Molekel []; von lateinisch molecula ‚kleine Masse‘) sind „im weiten Sinn“ zwei- oder mehratomige Teilchen, die durch chemische Bindungen zusammengehalten werden und wenigstens so lange stabil sind, dass sie z. B. spektroskopisch beobachtet werden können. Ein Molekül kann dabei aus mehreren gleichen oder aus verschiedenen Atomen bestehen. Es kann sich um neutrale Teilchen, aber auch um Radikale, Ionen oder auch ionische Addukte handeln. So sind z. B. viele Typen von interstellaren Molekülen unter irdischen Bedingungen nicht stabil. IUPAC nennt solche Teilchen „molekulare Gebilde“ (molecular entity).[1]
Grundsätzliches
[Bearbeiten | Quelltext bearbeiten]
Im engen Sinn und im allgemeinen Sprachgebrauch der Chemie sind Moleküle elektrisch neutrale Teilchen, die aus zwei oder mehreren Atomen aufgebaut sind.[2] Die Atome sind kovalent miteinander verknüpft und bilden einen in sich abgeschlossenen, chemisch abgesättigten Verband.[3][4] Ein so definiertes Molekül ist das kleinste Teilchen eines bestimmten Reinstoffes und hat eine bestimmbare Molekülmasse. Ein Molekül ist kein starres Gebilde, bei Energiezufuhr treten unterschiedliche Molekülschwingungen auf; hierzu reicht schon die Normaltemperatur.
Moleküle können aus Atomen eines einzigen chemischen Elements aufgebaut sein, wie z. B. Sauerstoff (O2) und Stickstoff (N2) (sogenannte Elementmoleküle). Die meisten Moleküle sind jedoch Verbände von Atomen verschiedener Elemente, wie beispielsweise Wasser (H2O) und Methan (CH4). Die Anordnung der Atome (ihre Konstitution) in einem Molekül ist durch die chemischen Bindungen fixiert. So unterscheiden sich trotz gleicher Anzahl der beteiligten Atome Ethanol (H3C–CH2–OH) von Dimethylether (H3C–O–CH3); sie werden durch unterschiedliche chemische Formeln dargestellt. In bestimmten Fällen können Moleküle wie z. B. die Moleküle der Milchsäure Formen mit gleicher Konstitution, aber unterschiedlicher räumlicher Anordnung (der Konfiguration) vorliegen. Dass gleiche Summenformeln unterschiedliche Moleküle zulassen, wird allgemein Isomerie genannt.
Die chemischen Eigenschaften eines Stoffes sowie spektroskopische Eigenschaften treten schon am einzelnen Molekül auf. Die makroskopischen physikalischen Eigenschaften wie Siede- oder Schmelzpunkt eines molekularen Stoffes entstehen erst mit mehreren Molekülen. Sie werden durch zwischenmolekulare Kräfte bestimmt und können bei Feststoffen zur Bildung von Molekülgittern führen. Große Moleküle werden Makromoleküle genannt. Aus Makromolekülen bestehen Kunststoffe wie PET und Biopolymere wie die Stärke.
Die Größe von zweiatomigen Molekülen liegt im Bereich von 10−10 m (1 Å), relativ große Moleküle aus recht vielen Atomen erreichen einen Durchmesser im Bereich von 10−9 m (10 Å), wobei Makromoleküle noch etwas größer sein können. Experimentell lässt sich die Größe von Molekülen z. B. mit dem Ölfleckversuch abschätzen.
Die Bindungsverhältnisse in Molekülen beruhen auf quantenmechanischen Effekten und werden beispielsweise mit dem VSEPR-Modell, der Valenzbindungstheorie oder der MO-Theorie erklärt und beschrieben.
Abgrenzung
[Bearbeiten | Quelltext bearbeiten]Nicht alle chemischen Verbindungen bestehen aus individuellen Molekülen. Keine Moleküle liegen z. B. bei diamantartigen Stoffen, wie Borcarbid (B4C) und Siliciumcarbid (SiC) vor. Die Atome werden zwar durch kovalente Bindungen zusammengehalten, ein typisches Molekül lässt sich jedoch nicht festlegen. Die chemische Formel ist nur eine Verhältnisformel. Die Anordnung der Atome lässt sich durch eine Elementarzelle darstellen, welche sich immer wiederholt und mit formal offenen (ungenutzten) Valenzelektronen an ihrer Oberfläche enden.
Keine Moleküle liegen auch bei Salzen wie Natriumchlorid (NaCl) vor, die durch ionische Bindungen zusammengehalten werden. Auch hier gibt die Formel das Verhältnis der beteiligten Atome wieder und auch hier kann der Verband der Atome prinzipiell eine beliebige Größe haben und den Bereich von einigen Millimetern erreichen. Grundelemente dieses Verbindungstyps sind Teilchen (hier Atome) mit einer Ladung. Solche Teilchen werden allgemein Ionen genannt. Das Natriumatom bildet ein Kation (Na+), das Chloratom ein Anion (Cl−). Im Fall von Natriumsulfat (Na2SO4) besteht das Anion SO42− aus einem Atomverband, der eine Ladung trägt. Atomverbände mit Ladungen sind keine Moleküle im engen Sinn. Dies ist auch in der organischen Chemie üblich: Essigsäure besteht aus Molekülen, das Anion der Säure wird Acetat-Ion genannt. Ein Sonderfall ist die Massenspektrometrie, bei der der Begriff Molekül-Ion verwendet wird.[5]
Mehratomige Radikale sind ebenfalls keine Moleküle im engeren Sinn, da diese Teilchen chemisch nicht abgesättigt sind. Es ist genügend und eindeutig, sie Radikale zu nennen. Die Bezeichnung „Radikale“ impliziert, dass sie aus mehr als einem Atom bestehen. Besonders in der organischen Chemie sind sie hochreaktive Zwischenprodukte in bestimmten chemischen Reaktionen. Es gibt jedoch auch stabile Radikale, wie Stickstoffmonoxid oder TEMPO. Hier führen zwischenmolekulare Kräfte zu physikalischen Eigenschaften der Verbindungen und diese Verbindungen können als molekular betrachtet werden.
Darstellungsweisen
[Bearbeiten | Quelltext bearbeiten]Es gibt verschiedene Möglichkeiten, Moleküle visuell darzustellen, wobei jede Darstellungsart bestimmte Vor- und Nachteile mit sich bringt. Grundsätzlich kann zwischen alphanumerischen oder zeichnerischen Formeldarstellungen und dreidimensionalen Modellen unterschieden werden. Daneben werden Moleküle auch mit mathematischen Modellen beschrieben.
Formeldarstellung
[Bearbeiten | Quelltext bearbeiten]Verhältnisformeln haben den niedrigsten Informationsgehalt und geben nur das Verhältnis der Atome im Molekül an. Aus der Elektronen- und Valenzstrichformel geht bereits hervor, welche Atome miteinander gebunden sind, die sogenannte Konstitution. Am meisten Information steckt in der Keilstrichformel, welche zusätzlich die räumliche Anordnung der Bindungen darstellt, die sogenannte Konfiguration. Daneben existieren weitere Formeldarstellungen, etwa die Fischer-Projektion, welche ebenfalls Information zur Konfiguration enthält, oder die Sägebock- und die Newman-Projektion, welche zusätzlich noch die Konformation darstellen.
| Strukturformeln | Andere Darstellungsweisen | ||||||
|---|---|---|---|---|---|---|---|
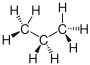
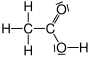
| Elektronenformel | Valenzstrichformel | Keilstrichformel | Skelettformel | Konstitutionsformel | Summenformel | Verhältnisformel | |
| Methan | existiert nicht | CH4 | CH4 | CH4 | |||
| Propan | 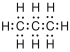
|

|
|
CH3–CH2–CH3 | C3H8 | C3H8 | |
| Essigsäure | 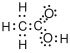
|
|
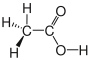
|
CH3–COOH | C2H4O2 | CH2O | |
| Wasser | existiert nicht | existiert nicht | H2O | H2O | |||
Dreidimensionale Modelle
[Bearbeiten | Quelltext bearbeiten]Gebräuchliche räumliche Molekülmodelle sind das Kalottenmodell, das Stäbchenmodell und davon abgeleitet das Kugel-Stab-Modell. Im Kalottenmodell wird die Raumerfüllung eines Moleküls dargestellt, die beiden anderen Modelle zeigen die räumliche Anordnung der Atome und Bindungen.
Mit quantenmechanischen Computermodellen der Moleküle können elektrostatische Potenzialoberflächen berechnet und am Bildschirm dargestellt werden. Sie stellen das elektrostatische Potenzial auf einer Oberfläche mit konstanter Elektronendichte dreidimensional dar und ermöglichen ein rasches Erkennen partiell unterschiedlich geladener Bereiche eines Moleküls. Diese Darstellungen werden verwendet, um Interaktionen zwischen Molekülen zu beurteilen.[6][7]
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Weblinks
[Bearbeiten | Quelltext bearbeiten]- Literatur von und über Molekül im Katalog der Deutschen Nationalbibliothek
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu molecular entity. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.M03986.
- ↑ Eintrag zu molecule. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.M04002.
- ↑ Der Brockhaus, Naturwissenschaft und Technik. F. A. Brockhaus, Mannheim; Spektrum Akademischer Verlag, Heidelberg 2003.
- ↑ Eintrag zu Moleküle. In: Römpp Online. Georg Thieme Verlag, abgerufen am 20. Juni 2014.
- ↑ Eintrag zu molecular ion. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.M03988.
- ↑ Electrostatic Potential maps. 2. Oktober 2013, abgerufen am 2. April 2022 (englisch).
- ↑ Eintrag zu Elektrostatisches Potential. In: Römpp Online. Georg Thieme Verlag, abgerufen am 4. April 2022.