N-Acetylneuraminsäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
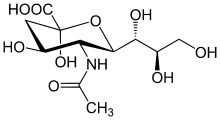
| |||||||||||||||||||
| N-Acetylneuraminsäure, β-Anomer | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | N-Acetylneuraminsäure | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C11H19NO9 | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[3] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 309,27 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
mäßig in Wasser (50 g·l−1 bei 20 °C),[3] löslich in Methanol, schwer löslich in Ethanol, praktisch unlöslich in Aceton[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
N-Acetylneuraminsäure (abgekürzt NANA von englisch: N-acetylneuraminic acid; veraltet: Lactaminsäure) ist ein Vertreter der Sialinsäuren – acylierte Derivate des Aminozuckers Neuraminsäure. Sie ist die häufigste Sialinsäure und wird daher mitunter selbst als Sialinsäure bezeichnet.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]N-Acetylneuraminsäure kann aus Milch, Eiern, Schwalbennestern, Submandibular-Mucinen verschiedener Säugetiere und bakteriellen Neuraminsäure-Polymeren (Colominsäuren) isoliert werden.[6]
Die Herstellung gelingt in einem zweistufigen Verfahren aus N-Acetylglucosamin, wobei im ersten Schritt N-Acetylglucosamin basenkatalytisch oder enzymatisch zu N-Acetylmannosamin epimerisiert wird. im zweiten Schritt wird N-Acetylmannosamin mit einem Überschuss Brenztraubensäure unter enzymatischer Katalyse durch eine immobilisierte N-Acetylneuraminsäure-Aldolase zum Endprodukt umgesetzt.[7][8]
Vorkommen
[Bearbeiten | Quelltext bearbeiten]N-Acetylneuraminsäure ist beim Menschen die einzig vorkommende Sialinsäure, während bei anderen Säugetieren, darunter den Primaten, auch die N-Glycolylneuraminsäure auftritt.[9] Zahlreiche Oligosaccharide, Glykoproteine, Glykolipide und Ganglioside enthalten N-Acetylneuraminsäure als endständigen Zucker in einer α-glycosidischen Bindung.[10]
Oligosaccharide mit N-Acetylneuraminsäure spielen eine wichtige Rolle bei Protein-Kohlenhydrat-Erkennungsprozessen, die wichtige physiologische Vorgänge steuern, beispielsweise bei Entzündungsprozessen oder Virusinfektionen.[6]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]N-Acetylneuraminsäure ist eine labile Verbindung, die sich bereits beim Stehen in wässriger Lösung zersetzt und sehr Alkali-empfindlich ist.[11]
Mittels Röntgenstrukturanalyse kann gezeigt werden, dass N-Acetylneuraminsäure in der β-Konfiguration kristallisiert. In wässriger Lösung stellt sich durch Mutarotation ein Gleichgewichtsgemisch von 8 % α- und 92 % β-N-Acetylneuraminsäure ein.[10]
Medizinische Verwendung
[Bearbeiten | Quelltext bearbeiten]Im März 2024 wurde N-Acetylneuraminsäure (Präparatename: Acenobel) in Japan zur Behandlung der hereditären Einschlusskörpermyositis (GNE-Myopathie, Nonaka-Myopathie) zugelassen.[12] Es handelt sich um eine sehr seltene erbliche Muskelschwunderkrankung, die durch Mutationen im GNE-Gen verursacht wird, das an der N-Acetylneuraminsäure-Biosynthese beteiligt ist.[13] Die Verabreichung erfolgt oral (Einnahme).
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ INN Recommended List 32. In: cdn.who.int. 9. Mai 1981.
- ↑ Eintrag zu ACETYLNEURAMINIC ACID in der CosIng-Datenbank der EU-Kommission, abgerufen am 19. Mai 2020.
- ↑ a b c Eintrag zu N-Acetylneuraminic acid bei Thermo Fisher Scientific, abgerufen am 13. Oktober 2023.
- ↑ Europäisches Arzneibuch 10.0. Deutscher Apotheker Verlag, 2020, ISBN 978-3-7692-7515-5, S. 690.
- ↑ a b Datenblatt N-Acetylneuraminic acid bei Sigma-Aldrich, abgerufen am 15. Dezember 2022 (PDF).
- ↑ a b Eintrag zu N-Acetylneuraminsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. Dezember 2022.
- ↑ Humphrey, Andrew J and Fremann, Claire and Critchley, Peter and Malykh, Yanina and Schauer, Roland and Bugg, Timothy DH: Biological properties of N-acyl and N-haloacetyl neuraminic acids: processing by enzymes of sialic acid metabolism, and interaction with influenza virus. In: Bioorganic & Medicinal Chemistry. Band 10, Nr. 10, 2002, S. 3175–3185, doi:10.1016/S0968-0896(02)00213-4.
- ↑ Udo Kragl, Daniel Gygax, Oreste Ghisalba, Christian Wandrey: Enzymatische zweistufige Synthese von N-Acetylneuraminsäure im Enzym-Membranreaktor. In: Angewandte Chemie. Band 103, Nr. 7, 1991, S. 854–855, doi:10.1002/ange.19911030721.
- ↑ Justin L. Sonnenburg, Tasha K. Altheide, Ajit Varki: A uniquely human consequence of domain-specific functional adaptation in a sialic acid-binding receptor. In: Glycobiology. Bd. 14, Nr. 4, April 2004, S. 339–346, PMID 14693915, doi:10.1093/glycob/cwh039.
- ↑ a b Horst Friebolin, Martin Supp, Reinhard Brossmer, Gunda Keilich, Dietmar Ziegler: 1H-NMR-Untersuchungen zur Mutarotation der N-Acetyl-D-neuraminsäure. In: Angewandte Chemie. Band 92, Nr. 3, 1980, S. 200–201, doi:10.1002/ange.19800920315.
- ↑ E. Klenk: Chemie und Biochemie der Neuraminsäure. In: Angewandte Chemie. Band 68, Nr. 10, 1956, S. 349–352, doi:10.1002/ange.19560681003.
- ↑ “ACENOBEL® Sustained Release Tablet 500 mg” Approved for Distal Myopathy with Rimmed Vacuoles (PDF; 0,2 MB); Pressemitteilung auf nobelpharma.co.jp, Nobelpharma Co., Ltd, 26. März 2024.
- ↑ Madoka Mori‐Yoshimura, Naoki Suzuki, Masahisa Katsuno, Masanori Takahashi, Satoshi Yamashita, Yasushi Oya, Akira Hashizume, Shinichiro Yamada, Mikihito Nakamori, Rumiko Izumi, Masaaki Kato, Hitoshi Warita, Masao Tateyama, Hiroshi Kuroda, Ryuta Asada, Takuhiro Yamaguchi, Ichizo Nishino, Masashi Akiyama: Efficacy confirmation study of aceneuramic acid administration for GNE myopathy in Japan. In: Orphanet Journal of Rare Diseases. 2023, Band 18, Nummer 1. DOI:10.1186/S13023-023-02850-Y.