Neptunium(III)-bromid
| Kristallstruktur | |||||||
|---|---|---|---|---|---|---|---|
 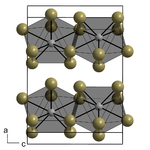
| |||||||
| links: α-NpBr3 _ Np3+ _ Br− rechts: β-NpBr3 _ Np3+ _ Br− | |||||||
| Kristallsystem |
α-NpBr3: hexagonal[1] | ||||||
| Raumgruppe |
α-NpBr3: P63/m (Nr. 176)[1] | ||||||
| Gitterparameter |
α-NpBr3:[1] | ||||||
| Allgemeines | |||||||
| Name | Neptunium(III)-bromid | ||||||
| Andere Namen |
Neptuniumtribromid | ||||||
| Verhältnisformel | NpBr3 | ||||||
| Kurzbeschreibung |
grüner Feststoff[2] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 476,76 g·mol−1 | ||||||
| Aggregatzustand |
fest | ||||||
| Dichte |
6,62 g·cm−3[3] | ||||||
| Gefahren- und Sicherheitshinweise | |||||||
 Radioaktiv | |||||||
| |||||||
| Thermodynamische Eigenschaften | |||||||
| ΔHf0 | |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||
Neptunium(III)-bromid ist eine chemische Verbindung aus den Elementen Neptunium und Brom. Es besitzt die Formel NpBr3 und gehört zur Stoffklasse der Bromide.
Darstellung
[Bearbeiten | Quelltext bearbeiten]Neptunium(III)-bromid kann durch Reaktion von Neptunium(IV)-oxid (NpO2) mit Aluminiumbromid (AlBr3) hergestellt werden.[5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Neptunium(III)-bromid ist ein grüner Feststoff. Es kristallisiert in zwei verschiedenen Formen:
- α-NpBr3 im hexagonalen Kristallsystem in der Raumgruppe P63/m (Nr. 176) mit den Gitterparametern a = 791,7 pm und c = 438,2 pm.[3] Es ist isostrukturell zum Uran(III)-chlorid.
- β-NpBr3 im orthorhombischen Kristallsystem (Plutonium(III)-bromid-Typ) in der Raumgruppe Ccmm (Nr. 63, Stellung 2) mit den Gitterparametern a = 411 pm, b = 1265 pm und c = 915 pm und vier Formeleinheiten pro Elementarzelle.[3] Es ist isostrukturell zu den Bromiden der Actinoidenelemente Plutonium bis Californium.
Das ebenfalls grüne Hexahydrat hat eine monokline Kristallstruktur mit der Raumgruppe P2/n (Nr. 13, Stellung 2).[5]
Chemische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Ein Erhitzen von Neptunium(III)-bromid mit überschüssigem Brom bei 425 °C führt zum Neptunium(IV)-bromid (NpBr4).[3]
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Einstufungen nach der CLP-Verordnung liegen nicht vor, weil diese nur die chemische Gefährlichkeit umfassen und eine völlig untergeordnete Rolle gegenüber den auf der Radioaktivität beruhenden Gefahren spielen. Auch Letzteres gilt nur, wenn es sich um eine dafür relevante Stoffmenge handelt.
Literatur
[Bearbeiten | Quelltext bearbeiten]- Zenko Yoshida, Stephen G. Johnson, Takaumi Kimura, John R. Krsul: Neptunium, in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 699–812. doi:10.1007/1-4020-3598-5_6.
- C. Keller: Die Chemie des Neptuniums. In: Fortschr. chem. Forsch., 1969/70, 13/1, S. 1–124. doi:10.1007/BFb0051170.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f C. Keller: Die Chemie des Neptuniums. In: Fortschr. chem. Forsch., 1969/70, 13/1, S. 69. doi:10.1007/BFb0051170.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1969.
- ↑ a b c d e Gmelins Handbuch der anorganischen Chemie, System Nr. 71, Transurane, Teil C, S. 148–150.
- ↑ Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung. In Bezug auf weitere Gefahren wurde dieser Stoff entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 1268.

