Phosphonsäuren

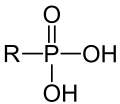
Als Phosphonsäuren werden neben der anorganischen Phosphonsäure H-PO(OH)2 als Stammverbindung auch die daraus abgeleiteten Derivate mit einer P-C-Bindung vom Typ R-PO(OH)2 (R = Alkyl-Rest oder Aryl-Rest) bezeichnet.[1] Die Salze und Ester der Phosphonsäuren werden als Phosphonate bezeichnet. Die Verbindungen vom Typ R-PO(OH)2 zählen dagegen nicht zu den Phosphonaten, sondern zu den organische Phosphonsäuren.[2]
Einige technisch wichtige Phosphonsäuren tragen Amino-Gruppe(n) in der Art NR2-(CH2)x-PO(OH)2 (R = alkyl oder H). Einige diese Aminophosphonsäuren haben strukturelle Ähnlichkeiten mit Komplexbildnern wie EDTA, NTA oder DTPA und haben eine ähnliche Funktion. Sie können Kationen wie beispielsweise Ca2+ in der Lösung ummanteln und das chemische Verhalten des Kations verändern. Im Fall von Calcium verschwindet die Eigenschaft, Wasserhärte zu bilden. Aber auch andere Kationen können ummantelt werden, um damit deren chemische Reaktivität mehr oder weniger abzuschwächen.
Natürliches Vorkommen
[Bearbeiten | Quelltext bearbeiten]1959 wurde mit 2-Aminoethylphosphonsäure die erste natürliche Phosphonsäure identifiziert. Sie kommt in Pflanzen und vielen Tieren vor, vor allem in Membranen. Phosphonsäuren sind in vielen verschiedenen Organismen weit verbreitet, z. B. in Prokaryoten, Eubakterien, Pilzen, Mollusken und Insekten. Die biologische Rolle der Phosphonsäuren und Phosphonate ist noch nicht endgültig geklärt. Bis jetzt wurden keine natürlichen Bis- oder andere Polyphosphonate entdeckt.[3]
Synthese
[Bearbeiten | Quelltext bearbeiten]Mono- und Dialkylphosphonsäuren sind über die Michaelis-Arbuzov-Reaktion darstellbar.[4][5] Halogenierte Phosphonate können durch die Michaelis-Becker-Reaktion dargestellt werden.[6] Silylphosphonate können durch eine Kinnear-Perren-Reaktion erzeugt werden.[7]
Beispiele
[Bearbeiten | Quelltext bearbeiten]| Kürzel | Chemische Namen | CAS-Nummer | Struktur |
|---|---|---|---|
| HEDP | 1-Hydroxyethan-(1,1-diphosphonsäure) | 2809-21-4 |

|
| ATMP NTMP |
Aminotrimethylenphosphonsäure oder auch Amino-tris(methylenphosphonsäure), identisch mit NTMP, Nitrilotris(methylenphosphonsäure) |
6419-19-8 | 
|
| DTPMP | Diethylentriaminpenta(methylenphosphonsäure) oder auch Diethylentriamin-penta(methylenphosphonsäure) |
Als Na-Salz: 22042-96-2 |

|
| EDTMP | Ethylendiamintetra(methylenphosphonsäure) oder auch Ethylendiamin-tetra(methylenphosphonsäure) |
Als Na-Salz: 15142-96-8 |

|
| PBTC | Phosphonobutan-tricarbonsäure 2-Phosphonobutan-1,2,4-tricarbonsäure 3-Carboxy-3-phosphonoadipinsäure |
37971-36-1 | 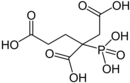
|
Anwendungen
[Bearbeiten | Quelltext bearbeiten]Ein wichtiger industrieller Gebrauch von Phosphonsäuren und Phosphonaten ist in Kühlwassersystemen, Entsalzungsanlagen und bei der Ölförderung, wo sie die Ausfällung von Salzen verhindern. In der Papier- und Textilindustrie werden sie als Stabilisator für die Peroxidbleiche eingesetzt und komplexieren dort Metalle, welche sonst das Peroxid inaktivieren würden.[3] In Waschmitteln werden sie als eine Kombination von Komplexbildnern, zur Verhinderung von Ausfällungen und als Bleichmittelstabilisator eingesetzt. Sie können ähnliche Eigenschaften wie EDTA haben und als Ersatz von Pentanatriumtriphosphat dienen. Sie gehören zu den Chelatkomplexen und dienen vor allem als Wasserenthärter. Als Builder können sie den Ionentauscher bzw. den Enthärter Zeolith A als Carrier unterstützen. Sie können als Korrosionsinhibitoren mitwirken oder als Stabilisator für Peroxide (z. B. in Bleichmitteln) dienen.[3] 1998 wurden weltweit etwa 56.000 Tonnen Phosphonate verwendet – 40.000 Tonnen in den USA, 15.000 Tonnen in Europa und weniger als 800 Tonnen in Japan.[3]
Herbizide
[Bearbeiten | Quelltext bearbeiten]
Eine der bekanntesten und wirtschaftlich bedeutendsten Phosphonsäuren ist Glyphosat (Handelsmarke: Roundup), ein Herbizid von Monsanto, welches eine Phosphonat-, eine Carboxylat- und eine Aminogruppe enthält.[3]
In der Medizin
[Bearbeiten | Quelltext bearbeiten]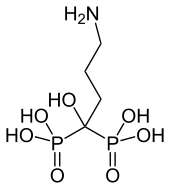
Phosphonate werden in der Medizin verwendet, vor allem zur Behandlung von Knochenkrankheiten und von Ca-Metabolismus-Störungen.[3] Unter Bisphosphonaten wird in der Medizin Verbindungen der Phosphonsäure mit der allgemeinen Konstitutionsformel ((O3P)2-C-R1R2)4− verstanden. Sie sind Analoga zu Diphosphaten (Pyrophosphate) (O3P-O-PO3)4− und greifen in die Calcium-Homöostase ein. Sie werden daher unter anderem zur Behandlung der Osteoporose und von Knochenmetastasen eingesetzt.
Toxikologie
[Bearbeiten | Quelltext bearbeiten]Die Toxizität der in den Beispielen genannten Phosphonsäuren ist gering. Die LC50-Werte für Fische liegen zwischen 0,1 und 1 mM. Auch werden sie praktisch nicht bioakkumuliert. Sie werden im Magen-Darm-Trakt nur sehr schlecht resorbiert und der größte Teil der absorbierten Menge wird über die Nieren wieder ausgeschieden. Die Humantoxizität dieser Phosphonsäuren ist ebenfalls sehr gering.[3] Phosphonate sind den Phosphaten ähnlich. Diese Ähnlichkeit führt häufig dazu, dass Phosphonsäureester Inhibitoren vieler Enzyme sind.
Biologischer Abbau
[Bearbeiten | Quelltext bearbeiten]Bakterien spielen in der Natur eine wichtige Rolle beim Abbau von Phosphonsäuren und Phosphonaten. Bakterien, welche die C-P-Bindung spalten können, können mit organischen Phosphonsäuren und deren Phosphonaten als alleiniger P-Quelle überleben. Aminophosphonate können von manchen Organismen auch als Stickstoffquelle genutzt werden. Die in der Industrie genutzten Polyphosphonate unterscheiden sich von den natürlichen Phosphonaten, da sie viel größer sind, eine starke negative Ladung tragen und mit Metallen komplexiert sind. Abbautests mit Klärschlamm haben gezeigt, dass HEDP und NTMP nicht abgebaut werden. Auch in Standardtests zeigte sich kein Abbau von HEDP, NTMP, EDTMP und DTPMP. Aus verschiedenen Umweltkompartimenten (Böden, Wasser, Klärschlamm, Kompost) konnten Bakterien isoliert werden, welche unter P-Mangel HEDP abzubauen vermögen. Allgemein bauen Bakterien nur Phosphonate mit einer funktionellen Gruppe ab.[3]
Umweltverhalten
[Bearbeiten | Quelltext bearbeiten]Die in den Beispielen genannten Phosphonsäuren haben einige Eigenschaften, welche sie von anderen Komplexbildnern unterscheiden und welche ihr Umweltverhalten bestimmen. Phosphonsäuren reagieren äußerst stark mit Oberflächen, was zu einer starken Elimination in technischen und natürlichen Systemen durch Adsorption führt, obwohl sie biologisch nicht abbaubar sind. Deswegen führen Phosphonsäuren und Phosphonate kaum zu einer Metallmobilisierung in der Umwelt. Der photochemische Abbau von Fe(III)-phosphonaten verläuft schnell. Aminopolyphosphonate werden in Gegenwart von Mangan(II) und Sauerstoff schnell oxidiert; die stabilen Produkte dieser Reaktion wurden in Kläranlagen identifiziert. Der Mangel an Daten über das Umweltverhalten oder Konzentrationen von Phosphonsäuren und Phosphonaten in der Umwelt kommt von analytischen Problemen mit der Spurenanalyse. In natürlichen Wässern kommen Phosphonate hauptsächlich als Ca- und Mg-Komplexe vor.[3]
Literatur
[Bearbeiten | Quelltext bearbeiten]- Philippe Savignac, Bogdan Iorga: Modern Phosphonate Chemistry. CRC Press, 2003, ISBN 0-203-50367-8.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu Phosphonate und Phosphite. In: Römpp Online. Georg Thieme Verlag, abgerufen am 14. November 2021.
- ↑ Eintrag zu Phosphor-organische Verbindungen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 14. November 2021.
- ↑ a b c d e f g h i Eugenia Valsami-Jones: Phosphorus in Environmental Technology: Principles and Applications. IWA Publishing, 2004, ISBN 978-1-84339-001-5, S. 149 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Timothy Carl Radsick: The Use of Functionalized Monoalkyl Phosphates and Phosphonates in the ... ProQuest, 2007, ISBN 978-0-549-39821-9, S. 36 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Abraham Clearfield, Konstantinos D. Demadis: Metal Phosphonate Chemistry: From Synthesis to Applications. Royal Society of Chemistry, 2011, ISBN 978-1-84973-356-4, S. 172 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Robert Engel: Handbook of organophosphorus Chemistry. CRC Press, 1992, ISBN 0-8247-8733-1, S. 280 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Philippe Savignac, Bogdan Iorga: Modern Phosphonate Chemistry. CRC Press, 2003, ISBN 0-203-50367-8, S. 521 (eingeschränkte Vorschau in der Google-Buchsuche).