Acene

Acene zählen in der Chemie zu einer Klasse von organischen Verbindungen, genauer den polycyclischen aromatischen Kohlenwasserstoffen, bestehend aus linear anellierten (kondensierten) Benzol-Ringen. Gemäß Nomenklatur stellt Anthracen den Grundkörper der Reihe dar,[1] vereinzelt wird auch Naphthalin zu den Acenen gezählt.[2][3] Die größeren Vertreter sind potentiell interessant für optoelektronische Anwendungen und aktuell Gegenstand chemischer und elektronischer Forschung. Pentacen wurde eingebaut in organische Transistoren, mit Ladungsbeweglichkeiten bis zu 5 cm2·V−1·s−1.
Kleinere Acene
[Bearbeiten | Quelltext bearbeiten]Die ersten fünf unsubstituierten Acene sind in der Tabelle aufgelistet:
| Name | Summenformel | Anzahl Ringe | Molmasse (g·mol−1) |
CAS-Nummer | Strukturformel |
|---|---|---|---|---|---|
| Anthracen | C14H10 | 3 | 178,23 | 120-12-7 | 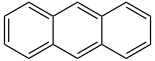
|
| Tetracen | C18H12 | 4 | 228,29 | 92-24-0 | 
|
| Pentacen | C22H14 | 5 | 278,35 | 135-48-8 | 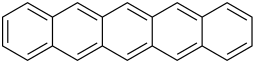
|
| Hexacen | C26H16 | 6 | 328,41 | 258-31-1 | 
|
| Heptacen | C30H18 | 7 | 378,46 | 258-38-8 | 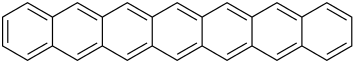
|
Die höheren Vertreter, Hexacen und Heptacen, sind sehr reaktionsfreudig (instabil) und können nur in einer Matrix isoliert werden. Allerdings sind bis(trialkylsilyl)ethynylierte Derivate von Hexacen and Heptacen stabiler und können als kristalline Feststoffe isoliert werden.[3]
Größere Acene
[Bearbeiten | Quelltext bearbeiten]Wegen der zunehmenden Größe des konjugierten π-Elektronensystems sind größere Acene ein aktuelles Forschungsthema.[4] Acene können auch Edukte für die Herstellung von Nanoröhrchen etc. sein. Unsubstituiertes Octacen (allgemeine Strukturformel, n = 6) enthält acht Ringe, Nonacen (n = 7) neun Ringe.[5] Sie wurden nur in einer Matrix isoliert und charakterisiert. Über ein stabiles substituiertes Nonacen wurde ebenfalls berichtet.[6] Im Jahr 2020 konnte eine Forschungsgruppe bereits über die Erzeugung von Dodecacen (n = 10) berichten.[7]
2024 gelang es Forschern, ein Tridecacen auf einer (111)-Gold-Oberfläche herzustellen. Dieses wurde anhand von STM- und STS-Untersuchungen identifiziert.[8]
Isomere
[Bearbeiten | Quelltext bearbeiten]Strukturelle Ähnlichkeit mit den linear aufgebauten Acenen besitzen 1,2-anellierten schraubenförmig aufgebaute Helicene.
Nomenklatur / Definition der Verbindungsklasse
[Bearbeiten | Quelltext bearbeiten]Als Acene werden polycyclische aromatische Kohlenwasserstoffe bezeichnet, die aus linear kondensierten Benzol-Einheiten aufgebaut sind. Während laut IUPAC Gold Book[1] Anthracen das erste Glied in der Reihe der Acene darstellt, ist laut Römpp Naphthalin als kleinstes Acen anzusehen.[2] Grundlage der Definition ist laut Römpp der von Clar 1939 getroffene Nomenklaturvorschlag.[9]
Anders als nach der Definition in Römpp zu vermuten, war jedoch Kernpunkt des Clarschen Vorschlages, die Klasse der linear kondensierten von derjenigen der angular kondensierten Kohlenwasserstoffe zu unterscheiden, indem die jeweiligen Vertreter basierend auf den Grundkörpern Anthracen (bei Clar als Triacen bezeichnet) und Phenanthren (bei Clar als Triphen bezeichnet) benannt werden sollen.
„So wie sich die Reihe der Acene vom Anthracen ableiten läßt, so kann man auch eine Reihe angularer Kohlenwasserstoffe, die als „Phene“ zu bezeichnen wären, vom Phenanthren ableiten: […]“[10]
Obwohl lediglich die Bezeichnung Acen Eingang in die systematische Nomenklatur gefunden hat, so zeigen die Ausführungen von Clar eindeutig, dass Naphthalin oder gar Benzol im Sinne der Nomenklatur nicht zur Klasse der Acene gehören.
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Eintrag zu acenes. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.A00061 – Version: 2.3.3.
- ↑ a b J. Falbe, M Regitz (Hrsg.): Römpp Chemie Lexikon, Stichwort Acene, S. 20, 9. erweiterte und neubearbeitete Auflage, 1995, Georg Thieme Verlag, Stuttgart.
- ↑ a b John E. Anthony: The Larger Acenes: Versatile Organic Semiconductors. In: Angewandte Chemie International Edition. 47. Jahrgang, 2008, S. 452, doi:10.1002/anie.200604045.
- ↑ Sanjio S. Zade, Michael Bendikov: Heptacene and Beyond: the Longest Characterized Acenes. In: Angewandte Chemie International Edition. 2010, S. 4012–4015, doi:10.1002/anie.200906002.
- ↑ Christina Tönshoff, Holger F. Bettinger: Photogeneration of Octacene and Nonacene. In: Angewandte Chemie International Edition. 2010, S. 4125–4128, doi:10.1002/anie.200906355.
- ↑ Irvinder Kaur, Mikael Jazdzyk, Nathan N. Stein, Polina Prusevich, Glen P. Miller: Design, Synthesis, and Characterization of a Persistent Nonacene Derivative. In: Journal of the American Chemical Society. 132. Jahrgang, 2010, S. 1261, doi:10.1021/ja9095472.
- ↑ Frank Eisenhut, Tim Kühne, Fátima García, Saleta Fernández, Enrique Guitián: Dodecacene Generated on Surface: Reopening of the Energy Gap. In: ACS Nano. Band 14, Nr. 1, 28. Januar 2020, S. 1011–1017, doi:10.1021/acsnano.9b08456.
- ↑ Zilin Ruan, Jakob Schramm, John B. Bauer, Tim Naumann, Holger F. Bettinger, Ralf Tonner-Zech, J. Michael Gottfried: Synthesis of Tridecacene by Multistep Single-Molecule Manipulation. In: Journal of the American Chemical Society. 12. Januar 2024, doi:10.1021/jacs.3c09392.
- ↑ Erich Clar: Vorschläge zur Nomenklatur kondensierter Ringsysteme (Aromatische Kohlenwasserstoffe, XXVI. Mitteilung). In: Berichte der deutschen chemischen Gesellschaft (A and B Series). Bd. 72, Ausg. 12, Wiley-VCH Verlag, Weinheim 6. Dezember 1939, doi:10.1002/cber.19390721219, S. 2137–2139.
- ↑ Erich Clar: Aromatische Kohlenwasserstoffe – Polycyclische Systeme. 2. verb. Aufl., Springer, Berlin / Heidelberg 1952, ISBN 978-3-642-85659-4, doi:10.1007/978-3-642-85658-7, S. 6. (eingeschränkte Vorschau in der Google-Buchsuche).