Rubidiumperiodat
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
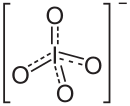
| |||||||
| Allgemeines | |||||||
| Name | Rubidiumperiodat | ||||||
| Summenformel | RbIO4 | ||||||
| Kurzbeschreibung |
farblose Kristalle[1] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 276,37 g·mol−1 | ||||||
| Aggregatzustand |
fest | ||||||
| Dichte |
3,918 g·cm−3[1] | ||||||
| Löslichkeit |
6,5 g·l−1[2] | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||
Rubidiumperiodat ist das Rubidiumsalz der Periodsäure.
Herstellung
[Bearbeiten | Quelltext bearbeiten]Rubidiumperiodat wird durch Einleiten von Chlor in eine heiße konzentrierte Lösung von Rubidiumiodat und Rubidiumhydroxid hergestellt.[2][4]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Rubidiumperiodat kristallisiert im tetragonalen Kristallsystem in der Raumgruppe I41/a (Raumgruppen-Nr. 88) mit den Gitterparametern a = 592,1 pm und c = 1305,2 pm, in der Elementarzelle befinden sich vier Formeleinheiten.[1] Die Kristalle sind mit den Kristallen von Kaliumperiodat isomorph.[2]
Chemische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Beim Erhitzen zersetzt es sich unter Sauerstoffabgabe.[1]
Beim langsamen Eindampfen einer Lösung von Rubidumperiodat mit Rubidiumhydrogencarbonat entsteht Rubidiumorthoperiodat.[5]
Aus Lösungen von Rubidiumperiodat und Rubidiumhydroxid kristallisiert ein binukleares Rubidiumorthoperiodat als Tetrahydrat aus.[5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d Jean D’Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-540-60035-0, S. 688 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c R. Abegg, F. Auerbach: Handbuch der anorganischen Chemie. Verlag S. Hirzel, Bd. 2, 1908. S. 431 (Volltext).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Thomas Vipond Barker: II.—Note on the iodates and periodates of the alkali metals and the ammonium radicle. In: Journal of the Chemical Society, Transactions. 93, 1908, S. 15, doi:10.1039/CT9089300015.
- ↑ a b G. V. Shilov, Z. K. Nikitina, Yu. A. Dobrovol'skii, L. S. Leonova, L. O. Atovmyan: Disubstituted Rubidium Orthoperiodate Rb2H3IO6: Crystal and Molecular Structures and Properties. In: Russian Journal of Coordination Chemistry 2004, 30(7), S. 449–452. doi:10.1023/B:RUCO.0000034783.23782.8d.



