Samarium(II)-iodid
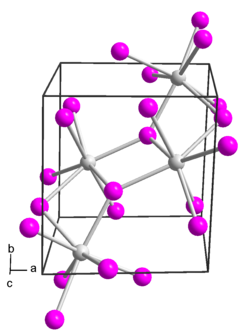
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| _ Sm2+ _ I− | ||||||||||
| Allgemeines | ||||||||||
| Name | Samarium(II)-iodid | |||||||||
| Andere Namen |
| |||||||||
| Verhältnisformel | SmI2 | |||||||||
| Kurzbeschreibung |
dunkelgrüne Kristalle[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 404,17 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
mäßig in Tetrahydrofuran[2] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Samarium(II)-iodid (SmI2) ist eine chemische Verbindung aus den Elementen Samarium und Iod. Samarium(II)-iodid ist ein tiefgrüner bis schwarzer Feststoff, es löst sich in Wasser mit tiefroter Farbe. Seine besondere Bedeutung erlangte es erst durch seine vielfältige Verwendung bei Synthesen in der Organischen Chemie. Samarium(II)-iodid wurde zusammen mit Ytterbium(II)-iodid (YbI2) als Reagenz für organische Synthesen eingeführt.
Darstellung
[Bearbeiten | Quelltext bearbeiten]Samarium gehört zu den Lanthanoiden und besitzt die Elektronenkonfiguration [Xe] 4f6 6s2. In seinen Verbindungen kommt es bevorzugt in der Oxidationsstufe +3 und seltener in der Oxidationsstufe +2 vor.
Über Samarium(II)-iodid wurde erstmals 1906 berichtet.[4] Samarium(II)-iodid ist nicht durch direkte Umsetzung aus den Elementen zugänglich, auf diesem Weg bildet sich nur Samarium(III)-iodid.
Die Darstellung von Samarium(II)-iodid gelingt durch Reduktion von wasserfreiem Samarium(III)-iodid im Wasserstoffstrom bei etwa 750 °C:[1]
Die Darstellung von Samarium(II)-iodid kann auch durch Reduktion von Samarium(III)-iodid mit metallischem Samarium erfolgen:[1]

Etabliert hat sich die Darstellung über Samariummetall und 1,2-Diiodethan in Tetrahydrofuran (THF) bei Raumtemperatur.[5] Aufgrund der Empfindlichkeit der Reagenzien muss dabei wasserfrei und unter Inertgas gearbeitet werden. Bei Anwesenheit von Sauerstoff erfolgt ansonsten eine rasche Oxidation zum Samarium(III). Dies ist optisch an der Farbänderung von dunkelblauer zu gelber Lösung erkennbar. Das Reagenz ist kommerziell als dunkelblaue 0,1 M-Lösung in THF erhältlich, ist jedoch auf Dauer instabil, so dass es besser frisch hergestellt werden sollte.
Ferner kann auch Samariummetall mit Quecksilber(II)-iodid oder mit Iod in THF umgesetzt werden.[6]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Samarium(II)-iodid ist ein tiefgrüner bis schwarzer Feststoff, der sich in Wasser mit tiefroter Farbe löst. SmI2 beginnt bei 0,01 Torr ab 680 °C wiederum in Sm und SmI3 zu disproportionieren und schmilzt unter deutlicher Zersetzung bei 840 °C; dabei gibt das SmI3 wiederum Iod ab. Der Schmelzpunkt kann daher nicht genau bestimmt werden.[1][7][8]
Chemische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Das Redoxpotential Sm2+/Sm3+ beträgt −1,55 V[5], daher ist es ein starkes Reduktionsmittel. Samarium(II)-iodid ist außerdem sehr luft- und feuchtigkeitsempfindlich. Es wird an Luft rasch zu Samarium(III) oxidiert. Die wässrige Lösung zersetzt sich im Laufe von etwa 15 min unter Wasserstoffentwicklung und weitgehender Entfärbung; dabei scheiden sich basische Iodide ab. Mit Säuren verläuft die Reaktion stürmisch.[1]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Samarium(II)-iodid eignet sich in großer Vielfalt für Standardreaktionen:[9]
- Reduktionen (selektives Einelektron-Reduktionsmittel)
- Ringöffnungsreaktionen
- Ringschlussreaktionen
- Dimerisierungen
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f G. Jantsch, N. Skalla: „Zur Kenntnis der Halogenide der seltenen Erden. IV. – Über Samarium(II)jodid und den thermischen Abbau des Samarium(III)jodids“, in: Zeitschrift für anorganische und allgemeine Chemie, 1930, 193, S. 391–405; doi:10.1002/zaac.19301930132.
- ↑ Eintrag zu Samarium(II)-iodid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. September 2014.
- ↑ Datenblatt Samarium(II) iodide, anhydrous, powder, ≥99.9% trace metals basis bei Sigma-Aldrich, abgerufen am 21. Juni 2016 (PDF).
- ↑ C. Matignon, E. Cazes, Ann. Chim. Phys., 1906, 8 (8), S. 417.
- ↑ a b P. Girard, Jean-Louis Namy, Henri B. Kagan: „Divalent Lanthanide Derivatives in Organic Synthesis. 1. Mild Preparation of SmI2 and YbI2 and Their Use as Reducing or Coupling Agents“, in: J. Am. Chem. Soc., 1980, 102 (8), S. 2693–2698; doi:10.1021/ja00528a029.
- ↑ John A. Soderquist: „Samarium(II) Iodide in Organic Synthesis“, in: Aldrichimica Acta, 1991, 24 (1), S. 15–23.
- ↑ G. Jantsch: „Thermischer Abbau von seltenen Erd(III)halogeniden“, in: Die Naturwissenschaften, 1930, 18 (7), S. 155–155; doi:10.1007/BF01501667.
- ↑ Gmelins Handbuch der anorganischen Chemie, System Nr. 39, Band C 6, S. 192–194.
- ↑ www.organic-chemistry.org: Reducing Agents > Samarium (low valent)
Literatur
[Bearbeiten | Quelltext bearbeiten]- Henri B. Kagan, Jean-Louis Namy: „Lanthanides in organic synthesis“, in: Tetrahedron, 1986, 42 (24), S. 6573–6614; doi:10.1016/S0040-4020(01)82098-6.
- Dennis P. Curran, Thomas L. Fevig, Craig P. Jasperse, Michael J. Totleben: „New Mechanistic Insights into Reductions of Halides and Radicals with Samarium(II) Iodide“, in: Synlett, 1992, S. 943–961; doi:10.1055/s-1992-21544.
- Gary A. Molander, Christina R. Harris: „Sequencing Reactions with Samarium(II) Iodide“, in: Chem. Rev., 1996, 96 (1), S. 307–338; doi:10.1021/cr950019y.
- Patrick G. Steel: „Recent developments in lanthanide mediated organic synthesis“, in: J. Chem. Soc., Perkin Trans. 1, 2001, S. 2727–2751; doi:10.1039/a908189e.
- Henri B. Kagan: „Twenty-five years of organic chemistry with diiodosamarium: an overview“, in: Tetrahedron, 2003, 59 (52), S. 10351–10372; doi:10.1016/j.tet.2003.09.101.
- Yusuke Asano, Shoko Suzuki, Tadashi Aoyama, Kosuke Shimizu, Masatsugu Kajitani, Yasuo Yokoyama: „Novel and Efficient Cyanofluoromethylation Promoted by Samarium(II) Species“, in: Synthesis, 2007, S. 1309–1314; doi:10.1002/chin.200736068.
- K. C. Nicolaou, Shelby P. Ellery, Jason S. Chen: „Samarium Diiodide Mediated Reactions in Total Synthesis“, in: Angew. Chem. Int. Ed., 2009, 48 (39), S. 7140–7165; doi:10.1002/anie.200902151; PMID 19714695; PMC 2771673 (freier Volltext).
- David J. Procter, Robert A. Flowers II, Troels Skydstrup: "Organic Synthesis Using Samarium Diiodide", 2009, Royal Society of Chemistry, ISBN 978-1-84755-110-8.



![{\displaystyle \mathrm {Sm\ +\ ICH_{2}CH_{2}I\ {\xrightarrow[{}]{THF}}\ SmI_{2}\ +\ H_{2}C=CH_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/6342c90db5ccd89e3e6bd0dbd3528a804a45cd84)