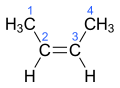Stereoselektive Synthese

Als Stereoselektive Synthese ist ein Begriff der stereochemischen Dynamik und wird in der Chemie eine Synthese bezeichnet, mit dem ein Molekül zielgerichtet mit einer festgelegten räumlichen Struktur aufgebaut wird, so dass von mehreren möglichen Stereoisomeren eines bevorzugt gebildet wird.
Ziel
[Bearbeiten | Quelltext bearbeiten]Neben dem allgemeinen Ziel einer chemischen Synthese, Bindungen kontrolliert zu knüpfen, entstehen hierbei ein oder mehrere neue Stereozentren. Das Ziel einer stereoselektiven Synthese ist nunmehr die selektive, also überwiegende Produktion eines bestimmten Stereoisomers.[1] Eine Sonderform der stereoselektiven Synthese ist die stereospezifischen Synthese, bei der nur ein reines Stereoisomer gebildet wird.
Stereoselektive Synthesen können erfolgen, wenn mindestens eine der an der Reaktion beteiligten Substanzen einen eindeutigen Aufbau (Konfiguration) besitzt. Zum einen werden natürliche Stoffe ("ex chiral pool") als Ausgangsmaterialien oder Hilfsstoffe eingesetzt, zum anderen können diese, oder künstlich hergestellte, Substanzen in einer katalytischen Reaktion eingesetzt werden. Ein Spezialfall der stereoselektiven Katalyse (mit Einschränkungen auch chirale oder asymmetrische Katalyse genannt) ist der Einsatz von Enzymen. Die stereoselektive Synthese ist besonders bei der Herstellung von biologisch aktiven Substanzen und Medikamenten von großer Bedeutung, da die räumliche Struktur bei natürlichen Prozessen oftmals entscheidend für pharmakologische oder allgemeiner biologische Wirkung und den Effekt einer Substanz ist.[2][3][4]
Sowohl in der Industrie als auch in der Wissenschaft gehört die Entwicklung neuer stereoselektiver Synthesen daher zu den am intensivsten beforschten Gebieten der modernen Chemie, besonders der organischen Chemie.
Übergangszustände
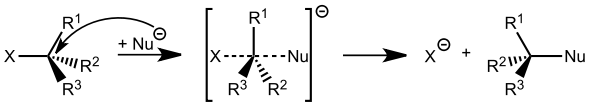
[Bearbeiten | Quelltext bearbeiten]Die Erklärung der Stereoselektivität erfolgt aus der Theorie der Übergangszustände. Der Reaktionsweg mit der niedrigsten Aktivierungsenergie wird bevorzugt durchlaufen, so dass ein Stereoisomer bevorzugt gebildet wird. Ein einfaches Beispiel ist die nukleophile Substitution nach SN2-Mechanismus mit Walden-Umkehr.
Auch bei der Eliminierung von Chlorwasserstoff aus 2-Chlorbutan können das cis- und das trans-Isomere von 2-Buten stereoselektiv entstehen:
-
cis-2-Buten
-
trans-2-Buten
Das Ausmaß der Stereoselektivität hängt von der energetischen Differenz der Übergangszustände und der Reaktionstemperatur ab. Der Übergangszustand kann unter anderem von der stereochemischen Struktur eines eingesetzten Katalysators und dem verwendeten Lösungsmittel beeinflusst werden.
Bei enantioselektiven Reaktionen spricht man dann von diastereotopen Übergangszuständen. Diastereotope Übergangszustände können sich nur dann entwickeln, wenn wenigstens einer der Reaktionspartner chiral ist (induzierte Stereoselektivität). Enzyme wirken als stereoselektive Katalysatoren, indem sie gezielt die Energie eines spezifischen Übergangszustands absenken. Ein Beispiel für eine stereoselektive Reaktion der organischen Synthesechemie ist die Sharpless-Epoxidierung.
Sind theoretisch mehrere Stereoisomere als Reaktionsprodukte denkbar, wird aber ausschließlich ein Übergangszustand durchlaufen, nennt man die Reaktion stereospezifisch. Ein theoretisches Modell der Ausbeuteberechnung von stereoselektiven Reaktionen wurde von Ernst Ruch und Ivar Ugi entwickelt.[5]
Für spezielle Reaktionstypen bestehen Regeln, die die Bildung des bevorzugten Stereoisomers voraussagen. So erlaubt die Cramsche Regel eine qualitative Voraussage des stereochemischen Verlaufs einer diastereoselektiven nucleophilen Addition von metallorganischen Verbindungen an eine Kohlenstoff-Sauerstoff-Doppelbindung, die in α-Position ein Chiralitätszentrum mit drei Substituenten unterschiedlicher Raumerfüllung aufweist.[6]
Literatur
[Bearbeiten | Quelltext bearbeiten]- Lewis N. Mander: Stereoselektive Synthese. Wiley-VCH, 1998, ISBN 978-3-527-29566-1 (Online)
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Bernhard Testa: Grundlagen der Organischen Stereochemie. Verlag Chemie, Weinheim 1983, ISBN 3-527-25935-X, S. 147–162.
- ↑ Miklós Simonyi (Hrsg.): Problems and Wonders of Chiral Molecules. Akadémiai Kiadó, Budapest 1990, ISBN 9630558815.
- ↑ Hermann J. Roth, Christa E. Müller, Gerd Folkers: Stereochemie und Arzneistoffe. Wissenschaftliche Verlagsgesellschaft, Stuttgart 1998, ISBN 3-8047-1485-4.
- ↑ E. J. Ariëns: Stereochemistry, a basis for sophisticated nonsense in pharmacokinetics and clinical pharmacology. In: Eur. J. Clin. Pharmacol. 26. Jahrgang, Nr. 6, 1984, S. 663–668, PMID 6092093 (englisch).
- ↑ Ernst Ruch, Ivar Ugi: Das stereochemische Strukturmodell, ein mathematisches Modell zur gruppentheoretischen Behandlung der dynamischen Stereochemie, in: Theoret. Chim. Acta, 1966, 4, 287–304, doi:10.1007/BF00528481.
- ↑ Donald J. Cram, Fathy Ahmed Abd Elhafez: Studies in Stereochemistry. X. The Rule of "Steric Control of Asymmetric Induction" in the Syntheses of Acyclic Systems. In: J. Am. Chem. Soc.; 1952; 74(23); 5828–5835, doi:10.1021/ja01143a007.