Triamcinolonhexacetonid
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
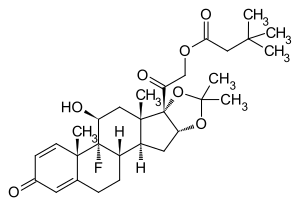
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Triamcinolonhexacetonid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C30H41FO7 | ||||||||||||||||||
| Kurzbeschreibung |
weißes bis fast weißes, kristallines Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Wirkstoffklasse |
Glucocorticoid | ||||||||||||||||||
| Wirkmechanismus |
Corticoid bindet an den entsprechenden cytosolischen Glucocorticoidrezeptor | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 532,64 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser, wenig löslich in wasserfreiem Ethanol und in Methanol[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Triamcinolonhexacetonid ist eine künstlich hergestellte chemische Verbindung aus der Gruppe der Steroide. Durch die Reste an drei der vier aliphatischen Hydroxygruppen im Molekül in Form eines Esters und eines Acetals ist es ein sehr gut fettlösliches Glucocorticoid, das als Arzneistoff zur Behandlung von entzündlichen Prozessen in Gelenken (zum Beispiel Arthritis) seine Anwendung findet.
Klinische Angaben
[Bearbeiten | Quelltext bearbeiten]Anwendungsgebiete (Indikationen)
[Bearbeiten | Quelltext bearbeiten]Intraartikuläre Injektionen
- Persistierende Entzündung in einem oder wenigen Gelenken nach Allgemeinbehandlung von chronisch-entzündlichen Gelenkerkrankungen
- Arthritis bei Chondrokalzinose
- Aktivierte Arthrose
- Posttraumatische, nicht bakteriell bedingte Arthritiden
Infiltrationstherapie
- Nichtbakterielle Tendovaginitis (strenge Indikationsstellung) und Bursitis
- Periarthopathien
- Insertionstendopathien
- Enthesiopathien bei entzündlich-rheumatischen Systemerkrankungen
Sub- und intraläsionale Injektion
- Isolierte Psoriasisherde
- Lichen ruber planus, Lichen simplex chronicus (Neurodermitis circumscripta)
- Alopecia areata
- Lupus erythematodes chronicus discoides
- Keloide
Spezielle Anwendungsgebiete
[Bearbeiten | Quelltext bearbeiten]Anwendungen bei der juvenilen idiopathischen Arthritis (JIA)
- Mittel der ersten Wahl bei intraartikulärer Steroidtherapie im Kindesalter[3]
- Triamcinolonhexacetonid (TH) ist wirksamer als Triamcinolonacetonid (TA), selbst wenn TA in höheren Dosen verabreicht wird[4]
Anwendungen in der Radiosynoviorthese (RSO)
- bei der „Polyethylenkrankheit“ nach Knie-TEP (Total-Endo-Prothese)[5]
- bei persistierender Synovitis im Fußgelenk[6]
- bei rheumatoider Arthritis in mittelgroßen und kleinen Gelenken[7]
- bei Synovialishypertrophie in DIP-Gelenken[8]
Dosierung
[Bearbeiten | Quelltext bearbeiten]Die Dosierung bei der intraartikulären Therapie richtet sich nach der Größe des Gelenks und der Schwere des Befundes. Die folgenden Dosierungsangaben können als Anhaltspunkte dienen: Große Gelenke 10–20 mg, mittlere Gelenke 5–10 mg, kleine Gelenke 2–5 mg Triamcinolonhexacetonid.
Gegenanzeigen (Kontraindikationen)
[Bearbeiten | Quelltext bearbeiten]Bei Überempfindlichkeit gegen Triamcinolonhexacetonid darf dieses Medikament nicht angewandt werden.
Anwendung während Schwangerschaft und Stillzeit
[Bearbeiten | Quelltext bearbeiten]Die Anwendung von Triamcinolon in den ersten fünf Monaten der Schwangerschaft sollte unterbleiben. Bei Langzeitanwendung sind intrauterine Wachstumsstörungen nicht auszuschließen. Bei einer Behandlung zum Ende der Schwangerschaft besteht für den Fetus die Gefahr einer Atrophie der Nebennierenrinde. Glucocorticoide gehen in die Muttermilch über. Ist eine Behandlung mit höheren Dosen oder eine Langzeitbehandlung erforderlich, sollte abgestillt werden.
Unerwünschte Wirkungen (Nebenwirkungen)
[Bearbeiten | Quelltext bearbeiten]Triamcinolonhexacetonid hat geringere systemische Nebenwirkungen für den Patienten als andere Glucocorticoide, da sich aus der hohen Corticoid-Konzentration am Wirkort ein niedriger Corticoid-Plasmaspiegel ergibt.
Pharmakologische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Wirkungsmechanismus (Pharmakodynamik)
[Bearbeiten | Quelltext bearbeiten]Triamcinolonhexacetonid wird aus dem kristallinen Depot freigesetzt und anschließend von Gewebsenzymen (Esterasen) in das Triamcinolonacetonid mit höherer Rezeptoraffinität umgewandelt. Das Corticoid bindet an den entsprechenden cytosolischen Glucocorticoidrezeptor und bewirkt seine Konformationsänderung. Der aktivierte Rezeptor kann jetzt die Genexpression beeinflussen, indem die Synthese proinflammatorischer Mediatoren verringert und die Bildung antiinflammatorischer Proteine erhöht wird. Der entzündliche Prozess in den Gelenken wird somit zurückgedrängt und die Schmerzen werden verringert.

Handelsnamen
[Bearbeiten | Quelltext bearbeiten]Triamcinolonhexacetonid wird als Monopräparat unter dem Handelsnamen Lederlon® in Form von Ampullen zur Injektion vermarktet.[9]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d Eintrag TRIAMCINOLONE HEXACETONIDE CRS beim Europäisches Direktorat für die Qualität von Arzneimitteln (EDQM), abgerufen am 20. Februar 2010.
- ↑ a b Triamcinolone Hexacetonide ( vom 31. Oktober 2016 im Internet Archive)
- ↑ J. Neidel: Die intraartikuläre Steroidtherapie bei entzündlich-rheumatischen Krankheiten des Kindes- und Jugendalters. In: Orthopädie. 31, 2002, S. 1175–1178.
- ↑ F. Zulian, G. Martini, D. Gobber, M. Plebani, F. Zacchello, P. Manners: Triamcinolone acetonide and hexacetonide intra-articular treatment of symmetrical joints in juvenile idiopathic arthritis: a double blind trial. In: Rheumatology. 43, 2004, S. 1288–1291.
- ↑ G. Mödder, R. Mödder-Reese: Radiosynoviorthese nach Knieendoprothesen: EffektiveTherapie bei „Polyethylene disease“. In: Der Nuklearmediziner. 24, Nr. 2, 2001, S. 97–103.
- ↑ F. M. van der Zant, Z. N. Jahangier, J. D. Moolenburgh, W. van der Zee, R. O. Boer, J. W. Jacobs: Radiation synovectomy of the ankle with 75 MBq colloidal 186rhenium-sulfide: effect, leakage, and radiation consideration. In: J Rheumatol. 31(5), 2004, S. 896–901.
- ↑ D. Göbel, S. Gratz, T. von Rothkirch, W. Becker: Chronic polyarthritis and radiosynoviorthesis: a prospective, controlled study of injection therapy with erbium 169 and rhenium 186. In: Z Rheumatol. 56(4), 1997, S. 207–213.
- ↑ G. Mödder: Radiosynoviorthese bei aktivierter Fingerpolyarthrose. In: Der Nuklearmediziner.29, 2006, S. 21–27.
- ↑ Gelbe Liste: Lederlon® 5 Kristallsusp. ( vom 4. August 2012 im Webarchiv archive.today)