Wasserdampf


In der Umgangssprache versteht man unter Wasserdampf meist die sichtbaren Dampfschwaden von kondensiertem Wasserdampf (Nassdampf). Dampfschwaden sind sichtbar, weil sich mikroskopisch kleine Tröpfchen gebildet haben, wie auch in Wolken und bei Nebel, die aufgrund der Mie-Streuung Sonnenlicht streuen, wodurch der Tyndall-Effekt auftritt und die eigentlich farblosen Tröpfchen sichtbar werden.
In Technik und Naturwissenschaft ist Wasserdampf die Bezeichnung für Wasser im gasförmigen Aggregatzustand. Dieser ist unsichtbar wie Luft, wird aber nicht als Wassergas bezeichnet, da dieser Begriff eine andere Bedeutung hat.
Wasserdampfhaltige Abgase kondensieren zu weißen Abgasfahnen, dem Schornstein entweicht also „Dampf“. Rußhaltige schwarze oder graue Abgase hingegen werden als Rauch bezeichnet.
Entstehung und Zustände
[Bearbeiten | Quelltext bearbeiten]Bei einem Standard-Umgebungsdruck von 1,013 bar (101,325 kPa) siedet reines Wasser bei 100 °C. Wird dem verbliebenen Wasser darüber hinaus Energie (Wärme) zugeführt, verdampft Wasser, ohne dass es zu einem weiteren Temperaturanstieg kommt. Aus 1 Liter (entsprechend 1 kg) Wasser entstehen 1,673 m³ Wasserdampf (unter Standardbedingungen), wofür eine Energiezufuhr von 2257 kJ benötigt wird.
Die zugeführte Energie erhöht die innere Energie des Dampfes nur um 2088 kJ. Mit dem Rest der zugeführten Wärmemenge leistet der Dampf gegenüber dem Umgebungsdruck eine Volumenänderungsarbeit W.
W kann auch als „Luftverdrängungsarbeit“ interpretiert werden. Physikalisch handelt es sich um die isobare Verschiebungsarbeit. Nachdem die Luft verdrängt wurde, kann der Dampf kondensiert werden, mit dem dabei entstehenden Unterdruck wurde früher die eigentliche Technische Arbeit gewonnen, die ersten Atmosphärischen Dampfmaschinen arbeiteten nach diesem Prinzip.

Die beiden Beiträge addiert ergeben also die Verdampfungsenthalpie H, die sich in einem Enthalpie-Entropie-Diagramm (h-s-Diagramm) in Form einer Differenz auf der y-Achse als spezifische Größe ablesen lässt. Das hier abgebildete T-s-Diagramm stellt die für die Verdampfung (bei 100 °C) notwendige Wärme in Form der gepunkteten blauen Fläche dar.
Ebenso lässt sich dabei der Zuwachs an Verdampfungsentropie (Delta S) ermitteln:
- = Verdampfungsenthalpie
- = Siedetemperatur in K
Wie aus dem Phasendiagramm entnommen wird, siedet Wasser bei einem Luftdruck von 0,4 bar schon bei etwa 75 °C (so etwa auf dem Mount Everest). Die aufzuwendende Verdampfungsenthalpie ist entsprechend größer, ebenso die Volumenzunahme des Dampfes. Mit steigendem Druck nimmt die Verdampfungsenthalpie des Wassers ab, bis sie im kritischen Punkt gleich Null ist. Daraus folgend die kleiner werdenden Flächen im T-s-Diagramm.
Erscheinungsformen
[Bearbeiten | Quelltext bearbeiten]
Der Dampfdruck des Wassers ist temperaturabhängig. Bei Temperaturen unterhalb des Siedepunktes spricht man von Verdunstung. In gesättigter Umgebungsluft stellt sich ein Gleichgewicht zwischen verdunstendem Wasser und kondensierendem Wasserdampf ein. Die Übergangsbedingungen zwischen flüssigem Wasser und Wasserdampf sind in der Siedepunktkurve des Zustandsdiagramms dargestellt. Daneben kann dem Wasser auch der Zustand „Überkritisches Fluid“ zugewiesen werden, ein besonders dichter und heißer Zustand, bei dem das Wasser keine Flüssigkeit mehr ist, aber auch nicht die typischen Eigenschaften eines Gases hat.
Nassdampf
[Bearbeiten | Quelltext bearbeiten]Wenn Dampf in eine kältere Umgebung strömt, kondensieren Teile des gasförmigen Wassers zu feinsten Tröpfchen. Ein solches Gemisch bezeichnet man als Nassdampf, der zum Beispiel beim Wasserkochen, oder auch beim Ausatmen im Winter beobachtet werden kann. Im T-s-Diagramm erstreckt sich der Bereich des Nassdampfes bis zum kritischen Punkt bei 374 °C und 221,2 bar.
Der Inhalt des Nassdampfes an reinem Dampf ist durch den Massenanteil x gekennzeichnet, der sich mit folgender Formel berechnen lässt
Diese Definition begrenzt den Dampfgehalt zwischen 0 ≤ x ≤ 1.
Über die ideale Gasgleichung können äquivalente Definitionen abgeleitet werden, die den Bereich des Dampfgehaltes nicht beschränken:
Darin bezeichnet das spezifische Volumen, die Enthalpie und die Entropie.
Der Zustand der gesättigten Flüssigkeit wird durch gekennzeichnet, der des gesättigten Dampfes durch .
Heißdampf
[Bearbeiten | Quelltext bearbeiten]Überhitzter Dampf
[Bearbeiten | Quelltext bearbeiten]Überhitzter Dampf ist Dampf mit einer Temperatur oberhalb der Siedetemperatur. Der Dampfgehalt beträgt nach obiger Formel . In Dampfkesseln wird der erzeugte Dampf mittels des Überhitzers in diesen Zustand gebracht. Abhängig vom Grad der Überhitzung werden die Bezeichnungen „Trockendampf“ und „Heißdampf“ verwendet.
Überkritisches Wasser
[Bearbeiten | Quelltext bearbeiten]Werden Temperatur und Druck von Wasser in einem geeigneten Druckbehälter stark erhöht, dann wird irgendwann der so genannte kritische Punkt überschritten und ein „überkritischer“ Zustand erreicht. Im überkritischen Zustand ist die Unterscheidung zwischen Wasserdampf und flüssigem Wasser sinnlos, denn weder in ihrer Dichte noch durch andere Eigenschaften sind sie noch voneinander zu unterscheiden. Es gibt dann keine Phasengrenze und keine Oberflächenspannung mehr. Unterhalb des kritischen Punktes ist der Wasserdampf folglich „unterkritisch“ und kann sich im Gleichgewicht mit flüssigem Wasser befinden. Wird in diesem Bereich das flüssige Wasser vollständig verdampft und dann die Temperatur weiter erhöht, so entsteht „überhitzter Dampf“. Diese Form des Dampfes enthält keine Wassertröpfchen mehr und ist in ihrem physikalischen Verhalten ebenfalls ein Gas.
Überkritisches Wasser hat besonders aggressive Eigenschaften. Es wurden daher Versuche unternommen, mit dessen Hilfe biologisch schwer abbaubare organische Schadstoffe, wie Dioxine, PCB hydrolytisch zu spalten.
Für den Dampfkessel erfordert der Übergang in den überkritischen Zustand eine besondere Bauart. Wegen des geringen Dichteunterschieds zwischen Wasser und Dampf kommt kein Auftrieb und damit kein stabiler Naturumlauf zustande. Kessel, die über oder auch nahe unter dem kritischen Punkt betrieben werden, sind deshalb immer Zwangslaufkessel. Da bei überkritischen Kesseln keine Trennung von Dampf- und Wasserphase mehr notwendig oder möglich ist, entfällt die Trommel und die Bauart ist ein Zwangsdurchlaufkessel, oft vom Typ Benson.
Sattdampf oder trocken gesättigter Dampf
[Bearbeiten | Quelltext bearbeiten]Der Grenzbereich zwischen Nass- und Heißdampf heißt „Sattdampf“, auch gesättigter Dampf oder trocken gesättigter Dampf. Die meisten Tabellenwerte zu Wasserdampfzuständen sind darauf bezogen. Es gibt auch übersättigen bzw. unterkühlten Dampf bzw. unterkühltes Wasser, wobei diese speziellen „metastabilen Zustände“ nicht als eigene Zustände in einem Phasendiagramm zu finden sind.
Grenzkurven
[Bearbeiten | Quelltext bearbeiten]Im T-s-Diagramm kommt den beiden Grenzkurven x = 0 und x = 1 eine besondere Bedeutung zu, die sich im kritischen Punkt treffen.
- Die Kurve x = 0, auch Siedelinie oder untere Grenzlinie, grenzt das Gebiet der Flüssigkeit vom Nassdampf ab, während
- die Kurve x = 1, auch Taulinie, Sattdampfkurve oder obere Grenzlinie, den Nassdampf vom Heißdampf trennt und gleichzeitig den Zustand des Sattdampfes markiert.
Die Schreibweise mit x für den Massenbruch ist hierbei nicht einheitlich definiert, da vor allem in der Chemie der Massenanteil mit w angegeben wird und x hier mehrheitlich für den Stoffmengenanteil steht. Beide Größen lassen sich ineinander umrechnen und gleichen sich in den Grenzwerten 0 und 1.

Erscheinung
[Bearbeiten | Quelltext bearbeiten]Gasförmiger oder überhitzter Wasserdampf ist farblos und eigentlich unsichtbar, wie die meisten Gase. Nassdampf ist durch die mitgerissenen Wassertropfen dagegen sichtbar. Bei Kontakt mit hinreichend kühler Umgebungsluft kommt es zur Unterschreitung des Taupunktes und folglich zu einer Kondensation weiterer feinster Wassertropfen. Die Existenz des Wasserdampfs in der Luft wird durch das an den Tröpfchen gestreute Licht sichtbar.
Wasserdampf kann auch direkt aus der festen Phase von Wasser entstehen: Eis oder Schnee werden „von der Sonne weggeleckt“. Dieses Phänomen wird besonders bei trockener Luft im Hochgebirge beobachtet, wenn verschneite Hänge bei Temperaturen von weit unter 0 °C mit der Zeit schneefrei werden. Das Eis, also das feste Wasser sublimiert zu Wasserdampf. Die Luftfeuchte nimmt durch Abdunsten aus dem Schnee zu, und zuvor verschneite Flächen apern aus, ein Phänomen beispielsweise im Himalaya. Aus denselben Ursachen trocknet im Freien aufgehängte Wäsche auch bei Temperaturen unter Null, sobald die relative Luftfeuchtigkeit gering genug ist.
In der Luft unsichtbar vorhandener Wasserdampf kondensiert unter besonderen Bedingungen (durch Kristallisationskeime) und wird sichtbar, etwa wenn ein Flugzeug in Bodennähe mit hoher Geschwindigkeit fliegt, dieser im Bild deutlich sichtbare Effekt wird oft fälschlich als „die Schallmauer“ bezeichnet, dieser Effekt ist jedoch kein Über- oder Unterschalleffekt. Durch die hohe Anströmgeschwindigkeit der Luft kann aus strömungsmechanischen Gründen, beispielsweise hohe Druckschwankungen, die Temperatur der anströmenden Luft stark und somit unter den Taupunkt abfallen, was zu einer Auskondensation führt. Der Wasserdampf im heißen Abgas wird hingegen von der sich erwärmenden Luft aufgenommen.
Sieden
[Bearbeiten | Quelltext bearbeiten]
In Abhängigkeit von der Wärmestromdichte, die der siedenden Flüssigkeit über eine Heizfläche zugeführt wird, bilden sich unterschiedliche Formen des Siedens.
Liegt die Temperatur der Heizfläche einige Grad über der Siedetemperatur, bilden sich an Unebenheiten Blasenkeime. Bis zu Wärmestromdichten von 2 kW/m² bilden sich Blasen, die beim Hinaufsteigen wieder kondensieren. Diese Siedeform wird als stilles Sieden bezeichnet.
Mit steigender Wärmestromdichte nimmt die Blasenbildung zu, und die Blasen erreichen die Oberfläche. Die an den Heizflächen abreißenden Blasen führen zu einem hohen Wärmeübergangskoeffizienten. Die Wandtemperaturen steigen nicht wesentlich über die Siedetemperatur (bis etwa 30 K). Beim Blasensieden können Wärmestromdichten bis 1000 kW/m² erreicht werden.
Wird die Wärmestromdichte dann noch weiter gesteigert, setzt sprunghaft das Filmsieden ein: Es bildet sich ein durchgehender Dampffilm. Dieser wirkt wie eine Isolierschicht, und der Wärmeübergangskoeffizient wird drastisch reduziert. Wird der Wärmestrom nicht reduziert, so wird erst dann wieder ein Gleichgewichtszustand erreicht, wenn die Wärme durch ausreichend hohe Wärmestrahlung abgegeben werden kann. Dieser Zustand wird aber erst bei einer Überhitzung der Heizfläche von rund 1000 K erreicht. In der Regel wird bei diesem Übergang vom Blasensieden zum Filmsieden die Heizfläche zerstört.
Um einer Zerstörung von Heizflächen an Dampfkesseln vorzubeugen, wird die maximale Wärmestromdichte auf 300 kW/m² begrenzt. In kleineren Fällen gibt es das Überschießen durch einen Siedeverzug.
Tabellen, Diagramme und Formeln
[Bearbeiten | Quelltext bearbeiten]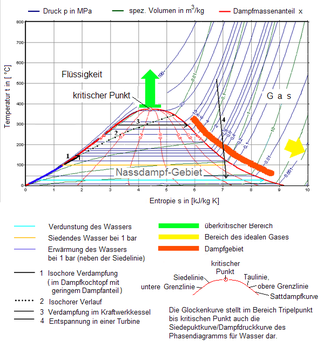

Wegen seiner enormen Bedeutung für die Energiewirtschaft zählt Wasserdampf zu den am besten erforschten Stoffen in der Thermodynamik. Seine physikalischen Eigenschaften wurden durch umfangreiche und häufige Messungen und Berechnungen bestimmt und in umfangreichen Tabellenwerken, den so genannten Wasserdampftafeln,[1] erfasst.
T-s-Diagramm
[Bearbeiten | Quelltext bearbeiten]Im T-s-Diagramm ist zu erkennen, dass beim Übergang von Flüssigkeit zu Dampf die Entropie zunimmt. Dies entspricht der Anschauung, dass die Teilchen einer Flüssigkeit wesentlich geordneter sind als die chaotische Vermengung der Teilchen bei einem Gas. Die Entropie wird auf der Abszisse aufgetragen. Eine weitere Besonderheit des Diagramms ist seine Eigenschaft, die zur Verdampfung des Wassers notwendige Wärmemenge als Fläche darzustellen. Mit der Beziehung: ΔH = T · ΔS ergibt sich für die Verdampfungsenthalpie eine Rechteckfläche, die zwischen T = 0 K und der jeweiligen Verdampfungsgeraden aufgespannt wird.
H-s-Diagramm
[Bearbeiten | Quelltext bearbeiten]Bei einem Mollier-Diagramm wird die Entropie des Dampfes auf der Abszisse und die zugehörige Enthalpie auf der Ordinate aufgetragen. Die grundlegenden physikalischen Eigenschaften des Wasserdampfes lassen sich zwar nicht einfach interpretieren, jedoch können die zur Zustandsänderung des Dampfes nötigen Wärmemengen, also beispielsweise die Verdampfungsenthalpie, direkt von der Ordinate abgelesen werden.
Magnus-Formel
[Bearbeiten | Quelltext bearbeiten]Eine Näherungsformel für die Berechnung des Sättigungsdampfdruckes in Abhängigkeit von der Temperatur ist die Magnus-Formel:
Temperatur θ in °C, Koeffizienten
Diese Formel ist sehr genau (unterhalb 0,22 %) im Bereich zwischen 0 und 100 °C und immer noch gut (unterhalb 4,3 %) zwischen −20 und 374 °C, der maximale Fehler liegt bei 290 °C. Wegen des einfachen Aufbaus und der hohen Genauigkeit wird sie zur Taupunktbestimmung vor allem in der Meteorologie und in der Bauphysik verwendet.
Mit leicht unterschiedlichen Koeffizienten
ergeben sich Werte, die auf 0,1 % mit der in DIN 4108 abgedruckten Tabelle für bauphysikalische Berechnungen übereinstimmt.
Die Magnus-Formel wurde von Heinrich Gustav Magnus empirisch ermittelt und seitdem lediglich durch genauere Werte der Koeffizienten ergänzt. Eine aus der Thermodynamik abgeleitete Gesetzmäßigkeit für Phasendiagramme stellen die Clapeyron-Gleichung und die Clausius-Clapeyron-Gleichung dar. Aufgrund vieler praktischer Probleme in Bezug auf diese eher theoretischen Gleichungen stellt die Magnus-Formel jedoch trotzdem die beste und praktikabelste Näherung dar.
Näherungs-Formel
[Bearbeiten | Quelltext bearbeiten]Eine brauchbare Faustformel für die Berechnung der Sattdampftemperatur aus dem Sattdampfdruck und umgekehrt ist
- ,
wenn man den Druck p in bar (absolut) einsetzt. Die zugehörige Temperatur θ ergibt sich in Grad Celsius. Diese Formel ist im Bereich p kr. > p > p = 3 bar (200 °C > θ > 100 °C) auf etwa 3 % genau.
Klimaeffekte
[Bearbeiten | Quelltext bearbeiten]

Im terrestrischen Wettergeschehen spielt Wasserdampf eine entscheidende Rolle. Ankommende Sonnenstrahlung wird beim Durchdringen der Atmosphäre vom Wasserdampf, oder auch von der Trübung der Luft in ihrer Strahlungsstärke gemindert[3][4]. Ein Kilogramm Luft kann bei 30 °C und 1 bar Druck etwa 26 Gramm Wasserdampf als Luftfeuchtigkeit aufnehmen. Diese Menge fällt bei 10 °C auf etwa 7,5 g/kg ab. Die überschüssige Menge wird je nach Wetterlage als Niederschlag in Form von Regen, Schnee, Hagel, Nebel, Tau, Reif oder Raureif aus der Luft ausgeschieden.
Wolken senden die ankommende Sonnenstrahlung teilweise zurück ins All und verringern auf diese Weise die am Boden ankommende Energiemenge. Das gleiche tun sie mit der von unten kommenden Wärmestrahlung und erhöhen damit die atmosphärische Gegenstrahlung. Ob Wolken die Erdoberfläche wärmen oder kühlen hängt davon ab, in welcher Höhe sie sich befinden: Niedrig stehende Wolken kühlen die Erde, hoch stehende Wolken wirken wärmend.[5]
In der Stratosphäre vorhandene Spuren von Wasserdampf gelten als besonders klimarelevant. Die Klimaforscher beobachteten in den letzten 40 Jahren ein Anwachsen des Wasserdampfs in der Stratosphäre um 75 % (siehe polare Stratosphärenwolken) und machen diesen für die Erhöhung der mittleren Erdtemperatur mitverantwortlich.[6] Die Herkunft des Wasserdampfs in diesen Höhen ist noch unklar, man vermutet jedoch einen Zusammenhang mit der in den letzten Jahrzehnten stark gestiegenen Methanausbringung durch die industrielle Landwirtschaft. Methan wird in diesen großen Höhen zu Kohlendioxid und Wasserdampf oxidiert, womit allerdings nur die Hälfte des Zuwachses zu erklären ist.
In der Erdatmosphäre vorhandener Wasserdampf ist mit um 36 % bis zu 70 % Anteil die Hauptquelle der atmosphärischen Gegenstrahlung und Träger des „natürlichen“ Treibhauseffektes. Die große Bandbreite (36 % bis 70 %) kommt nicht dadurch zustande, dass man den Effekt nicht genau messen könnte, sondern dadurch, dass die atmosphärische Luftfeuchtigkeit zeitlich und örtlich starken natürlichen Schwankungen unterliegt.[7] Der Treibhauseffekt ist für den Strahlungshaushalt der Erde ein wichtiger Effekt und hat eine Erhöhung der globalen Durchschnittstemperatur auf ein Niveau von 15 °C zur Folge. Das Leben auf der Erde wurde dadurch überhaupt erst möglich. Als Durchschnittstemperatur ohne Treibhauseffekt wird meist eine Temperatur von etwa −18 °C angegeben.
Wasserdampf-Rückkopplung
[Bearbeiten | Quelltext bearbeiten]Eine steigende Durchschnittstemperatur der Erde führt zu einem steigenden mittleren Wasserdampfgehalt der Atmosphäre.[8] Gemäß der Clausius-Clapeyron-Gleichung kann die Atmosphäre mit jedem Grad Temperaturanstieg 7 % mehr Wasserdampf enthalten.
Im Kontext der globalen Erwärmung ist die so genannte „Wasserdampf-Rückkopplung“ neben der Eis-Albedo-Rückkopplung die stärkste bisher bekannte positive Rückkopplung:[9][10] Bei einer angenommenen Klimasensitivität von 2,8 °C bei einer Verdoppelung der atmosphärischen Kohlenstoffdioxidkonzentration ist 1,2 °C auf die direkte wärmende Wirkung des CO2 zurückzuführen, ein Grad entfällt auf die Wasserdampf-Rückkopplung und der Rest auf die übrigen Rückkopplungen.[11] Während der letzten 35 Jahre ist die Luftfeuchtigkeit am oberen Rand der Wetterschicht um durchschnittlich ca. zehn Prozent gestiegen.[10]
Wissenschaftler halten es für möglich, dass eine Wasserdampf-Rückkopplung auch auf anderen Planeten stattfindet; so könnte die Venus kurz nach ihrer Entstehung vor viereinhalb Milliarden Jahren für längere Zeit einen Ozean besessen haben,[12] und im Laufe ihrer Entwicklungsgeschichte soll auch eine Wasserdampf-Rückkopplung aufgetreten sein.[13]
Natürliches Vorkommen
[Bearbeiten | Quelltext bearbeiten]
Reiner Wasserdampf entsteht in der Natur auf der Erde in Vulkanen, Fumarolen und bei Geysiren. Es ist der wichtigste Parameter bei vulkanischen Eruptionen und bestimmt deren Charakter mit. Es ist dabei maßgebend, dass viele Minerale bzw. Gesteine Wasser oder andere flüchtige Stoffe in ihr Kristallgitter einbinden, besonders unter der Wirkung hoher Drücke. Da Magma beim Aufsteigen in der Kruste eine Druckentlastung erfährt, treibt der Wasserdampf zusammen mit anderen Fluiden aus dem Magma aus und bildet Blasen, welche durch den Druck zunächst jedoch nicht frei expandieren. Unterschreitet der Druck einen bestimmten Wert, so verbinden sich diese Fluidblasen und führen zu einer Art enormen Siedeverzugs, werden also explosionsartig frei. Dabei reißen sie auch größere Mengen Magma mit und verursachen die vergleichsweise seltenen explosiven Vulkanausbrüche. Da der Anteil an Fluiden in den Gesteinen bei konvergierenden Plattengrenzen besonders groß ist, zeigt sich bei diesen auch die deutlichste Tendenz für diesen Vulkantyp.
Menschlicher Wasserdampf
[Bearbeiten | Quelltext bearbeiten]Wasserdampf ist ein wichtiges Hilfsmittel für den menschlichen Wärmehaushalt. Bei hohen Umgebungstemperaturen wird zur Thermoregulation durch Schwitzen die überschüssige Körperwärme (Verdunstungskälte) an die Umgebung abgegeben. Die dabei umgesetzten Wärmemengen sind erheblich, zur Verdunstung von einem Gramm Schweiß werden 2,43 kJ Wärme benötigt. Der gesunde Mensch erzeugt bei normalen Umgebungstemperaturen täglich etwa 500 g Wasserdampf durch Schwitzen, hinzu kommt noch einmal die doppelte Menge mit der ausgeatmeten Luft. Auch dadurch wird die Körpertemperatur auf 37 °C geregelt.
Wasserdampfeintrag
[Bearbeiten | Quelltext bearbeiten]

Bei der Verbrennung von Erdölprodukten werden die Kohlenwasserstoffe der Erdölfraktionen im Wesentlichen in Kohlenstoffdioxid und Wasserdampf umgesetzt. Im Autoverkehr sind die Quellen Benzin und Diesel, im Luftverkehr Kerosin, in der Hausheizung Heizöl und in der Industrie Schweröle. Der im Abgas enthaltene kondensierende Wasserdampf macht sich beim Flugzeug durch Kondensstreifen am Himmel bemerkbar. Bei der Verbrennung von Erdgas, das mittlerweile zur Heizung von Gebäuden verwendet wird, fällt wegen der vier Wasserstoffatome je Kohlenstoffatom im Methanmolekül doppelt so viel Wasserdampf wie Kohlenstoffdioxid an. Dies ist der Grund dafür, dass Brennwertgeräte für Erdgas effektiver arbeiten als für Heizöl. Wasserdampf wird bei vielen großtechnischen Prozessen als Abfallprodukt in die Atmosphäre eingetragen.
Wasserdampf in der Klimatechnik
[Bearbeiten | Quelltext bearbeiten]Eine Klimaanlage ist eine Gebäudeausstattung, die einen definierten Wasserdampfgehalt der Luft garantiert. Um Fertigprodukte aus Eisen- und Stahlwerkstoffen vor Korrosion, Lagerbestände wie Bücher vor Verwitterung und Lebensmittel vor Austrocknung zu schützen, werden Lagerhallen klimatisiert. In der Wohnraumklimatisierung trägt der Wasserdampfgehalt in erheblichem Maße zum Wohlbefinden des Menschen bei. Bei der Beurteilung der Raumluft spielt der Begriff der Behaglichkeit eine zentrale Rolle; ein Aspekt ist der als angenehm empfundene Zusammenhang zwischen Raumlufttemperatur und relativer Luftfeuchtigkeit. Dieser wird von einer Klimaanlage sichergestellt und liegt in der Regel zwischen 30 % und 70 % relativer Luftfeuchte.
Quantifizierung von Wasserdampf
[Bearbeiten | Quelltext bearbeiten]Da der Wasserdampf bei verschiedensten Gegebenheiten und Prozessen eine große Rolle spielt, wird er mit unterschiedlichsten Messmethoden und -geräten erfasst und in einer Vielzahl von Größen angegeben.
Für meteorologische Zwecke in Bezug auf die feuchte Luft wird oft die relative Luftfeuchte φ verwendet. Diese kann man unter anderem mit einem Haarhygrometer messen. In der Technik wird in der Regel die absolute Feuchte x verwendet. Diese misst man mit einem LiCl-Geber oder Coulometrischem Feuchtesensor, bei welchen (ausgehend von stark hygroskopischem Diphosphorpentoxid) auf den Wasserdampfgehalt der Luft geschlossen wird. Eine weitere Möglichkeit zur Bestimmung des Wasserdampfgehaltes der Luft ist die Messung ihrer Temperatur an je einem trockenen und angefeuchteten Thermometer, wobei die Messstelle des zweiten Thermometers mit einem wassergetränkten Gewebe umwickelt und zur Förderung der Verdunstung mit einem kleinen Lüfter angeblasen wird. Mithilfe der beiden abgelesenen Werte lässt sich aus dem Mollier-h-x-Diagramm sofort die zugehörige Luftfeuchtigkeit ablesen. Das Psychrometer ist das praktische Ergebnis der Weiterentwicklung dieser Messmethode.
In Dampferzeugern dienen neben Thermometer auch Manometer zur einfachen Messung der Dampfparameter.
Wasserdampf in der Geschichte
[Bearbeiten | Quelltext bearbeiten]Der Anblick von Wasserdampf ist den Menschen seit der Nutzbarmachung des Feuers bekannt; er entstand mehr oder weniger unbeabsichtigt beim Kochen oder beim Löschen der Feuerstelle mit Wasser. Erste Überlegungen zur technischen Nutzung von Wasserdampf werden Archimedes zugeschrieben, der eine Dampfkanone konstruierte. Leonardo da Vinci stellte zu diesem Thema erste Berechnungen an, wonach eine acht Kilogramm schwere Kugel aus einer solchen Kanone verschossen etwa 1250 Meter weit fliegen würde.
Heron von Alexandria erfand den Heronsball, eine erste Dampfmaschine. Seine Erfindung hatte in der Antike keinen praktischen Nutzwert, sie zeigte aber die technische Möglichkeit der Nutzung von Wasserdampf auf.
Auf Denis Papin geht die praktische Ausführung des Schnellkochtopfes zurück. Dieser erste Druckbehälter wurde von Anfang an mit einem Sicherheitsventil ausgerüstet, nachdem es mit einem Prototyp bei den ersten Versuchen zu einem Zerknall gekommen war.
Die Erfindung und Nutzung der Dampfmaschine machten es notwendig, das Arbeitsmittel Wasserdampf theoretisch und praktisch zu untersuchen. Zu den Praktikern gehören James Watt und Carl Gustav Patrik de Laval, die durch die Vermarktung ihrer Maschinen zu wohlhabenden Männern wurden. Zu den Theoretikern gehörte dagegen Nicolas Léonard Sadi Carnot, der Überlegungen zu Wasserdampf und der Dampfmaschine anstellte. In die Reihe der Forscher, die sich eingehend mit den Eigenschaften von Wasserdampf beschäftigten, gehören auch Rudolf Julius Emanuel Clausius und Ludwig Boltzmann.
Nutzung in der Technik
[Bearbeiten | Quelltext bearbeiten]| Dampferzeuger Dampf | |||||||||
| Dampfturbine Dampf | |||||||||
| Kondensator Wasser | |||||||||
| Speisepumpe Wasser | |||||||||
Wasserdampf wird in der Technik in Dampfkesseln erzeugt und beispielsweise zu folgenden Zwecken verwendet:
- als Arbeitsmittel in Dampfmaschinen, Dampflokomotiven und Dampfturbinen,
- bei der Förderung von Erdöl und als Hilfsmittel beim Steamcracken für die Herstellung von Benzin,
- als Zwischenprodukt bei der Meerwasserentsalzung,
- als ein Rohstoff für die Herstellung von Wasser- und Generatorgas durch das Steam-Reforming,
- in Dampfheizungen, Autoklaven und bei der Siedekühlung als Träger der Wärmeenergie,
- zur Dampfbefeuchtung trockener Luft in Lüftungsanlagen,
- zum Fördern von flüssigem Wasser mit einer Dampfstrahlpumpe,
- bei der Wasserdampfdestillation als Schleppmittel,
- Erzeugen eines Vakuums durch Verdrängung der Luft aus einem geschlossenen Druckbehälter mit anschließender Kondensation.
Die derzeit größten Kraftwerksdampferzeuger haben eine Leistung von bis zu 3600 Tonnen Dampf pro Stunde. Derartige Mengen werden beispielsweise mit einem Wasserrohrkessel bereitgestellt.
Beim technischen Einsatz von Wasserdampf ist zu beachten, dass Nassdampf im Unterschied zu den meisten anderen Flüssigkeiten und Gasen nicht gepumpt werden kann. Die beim Verdichten des Dampfes auftretenden Wasserschläge würden die Fördermaschine innerhalb kürzester Zeit zerstören.
Weitere Anwendungen
[Bearbeiten | Quelltext bearbeiten]- zur Bodensterilisation und Bodenhygienisierung durch Dämpfen (Bodendesinfektion) mit Heißdampf
- zur Reinigung mittels Dampfreinigern,
- in der Küche zur schonenden Zubereitung von Lebensmitteln durch Dämpfen,
- in der Mehlerzeugung, vor allem bei Vollkornmehl, zur Stabilisierung des Getreidekeimlings,
- zum Bearbeiten von Holz im Boots-, Möbel- und Instrumentenbau,
- zum Erzeugen eines Vakuums in geschlossenen Druckbehältern durch Verdrängung der Luft und anschließende Kondensation,
- zur Sterilisation von medizinischen und mikrobiologischen Instrumenten durch sogenanntes autoklavieren,
- zum Bügeln von Wäsche.
- In der Medizin und Therapeutik wird Wasserdampf für die Wärmeübertragung und als Träger therapeutischer Stoffe verwendet:
- Inhalation zur Heilung, etwa von Husten, oder zur Linderung von Erkältungen, mit Inhalatoren oder einer Gesichtssauna,
- im Wellnessbereich in Dampfbädern.
Gefahren durch Wasserdampf
[Bearbeiten | Quelltext bearbeiten]Geringe Mengen Wasserdampf können große Mengen Wärme und damit Energie transportieren. Aus diesem Grund ist das zerstörerische Potenzial von dampfführenden Apparaturen wie Dampferzeuger und Rohrleitungen erheblich. Kesselzerknalle von Dampfkesseln gehörten zu den schwersten Unfällen in der Technikgeschichte; derartige Ereignisse haben in der Vergangenheit mit einem Schlag Industriebetriebe zerstört.
Diese Ereignisse lösten die Gründung von Dampfkessel-Überwachungsvereinen aus, aus denen sich später die Technischen Überwachungsvereine, heute bekannt unter der Abkürzung TÜV, entwickelten.
Die Gefahr entsteht durch den „unsichtbaren“ Wasserdampf, der mit hoher Temperatur und hohem Druck in einem Strahl von erheblicher Länge aus einem defekten Dampfkessel frei austritt. Der austretende Freistrahl vermischt sich erst nach einer gewissen Strecke mit der Umgebungsluft und kühlt dabei langsam ab. Erst bei Unterschreitung von 100 °C (= Sattdampftemperatur bei Umgebungsdruck) beginnt der Dampf zu kondensieren und sichtbar zu werden.
Eine Gefahr bei großen Dampfaustritten ist andererseits die Bildung von Nebel, der für Flüchtende die Orientierung erschwert. Und schließlich kann ausströmender überhitzter Wasserdampf sogar Brände und zündwirksame Explosionen auslösen. Der Abriss der Tröpfchen von der Ausströmöffnung ist ein Trennprozess, der oft hohe Aufladungen zur Folge hat. Die dabei auftretenden elektrostatischen Entladungen sind in der Regel zündwirksam für explosionsfähige Gas- oder Dampf-Luft-Gemische. Das Nachverdampfen von flüssigem Wasser geschieht durch die in der Umgebung der defekten Stelle eintretende Druckverringerung.[14]
Ein großflächiger Kontakt mit einem Strahl Wasserdampf oder heißem Wasser ist wegen der augenblicklich eintretenden Verbrühungen tödlich. In der letzten Zeit sind im Zusammenhang mit Wasserdampf weniger Unfälle geschehen, weil sich der Stand der Technik auf diesem Gebiet permanent zu größeren Sicherheiten hin entwickelt hat.
Bei einem Metallbrand und den auftretenden hohen Temperaturen von über 2000 °C zersetzt sich Wasser in Wasserstoff und Sauerstoff. Infolgedessen besteht die Gefahr von Knallgasexplosionen, weshalb Wasser als Löschmittel nicht verwendet werden darf. Aufgrund des großen Volumenunterschiedes zwischen Wasser und Wasserdampf (1:1700) ist es gefährlich, bestimmte Brände mit Wasser zu löschen. Bei einem Kaminbrand kann das Löschwasser zu einem Zerreißen des Kamins führen und somit die Löschkräfte gefährden und Sachschaden anrichten. Aus dem gleichen Grund darf ein Fettbrand nicht mit Wasser gelöscht werden, da Wasser wegen der höheren Dichte unter das brennende Fett gelangt, an der heißen Fläche verdampft und sich dabei explosionsartig ausdehnt und brennendes Fett mitreißt, so kommt es zur Fettexplosion.
Begriffe und Stoffwerte
[Bearbeiten | Quelltext bearbeiten]
- Name
- Wasserdampf
- weitere Namen
- dazu das nebenstehende Diagramm
- Summenformel
- H2O
- Dichte
- 0,598 kg/m³ (bei 100 °C und 1,01325 bar)
- Spezifische Wärmekapazität
- 2,08 kJ/(kg K) (bei 100 °C und 1,01325 bar)
- Wärmeleitfähigkeit
- 0,0248 W/(m·K)
- Tripelpunkt
- 273,160 K entspricht 0,01 °C bei 0,00612 bar
- kritischer Punkt
- 374,150 °C bei: 221,20 bar
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Literatur
[Bearbeiten | Quelltext bearbeiten]- Dubbel Kapitel D. 17. Auflage. Springer, Berlin 1990, ISBN 3-540-52381-2.
- Mollier h,s-Diagram for Water and Steam. Springer, Berlin 1998, ISBN 3-540-64375-3.
- Walter Wagner: Wasser und Wasserdampf im Anlagenbau. Kamprath-Reihe. Vogel, Würzburg 2003, ISBN 3-8023-1938-9.
- Properties of Water and Steam in SI-Units. Thermodynamische Eigenschaften von Wasser und Wasserdampf, 0–800 °C, 0–1000 bar. Springer, Berlin 1981, ISBN 3-540-09601-9, ISBN 0-387-09601-9.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Ein leeres TS-Diagramm für Wasser und Wasserdampf auf Commons
- Ein leeres Mollier-hs-Diagramm für Wasserdampf in hoher Auflösung auf Commons
- Website der International Association for the Properties of Water and Steam (engl.)
- Wasserdampftafel für flüssiges Wasser und Sattdampf
- Wasserdampfkalkulation ( vom 7. Oktober 2007 im Internet Archive) – Freeware in MS-Excel, OpenDocument und anderen Formaten
- Stefanie Lorenz, Hilke Stümpel: Lernmodul „Kondensation und Feuchtemaße“. Wasser in der Atmosphäre. In: WEBGEO. Institut für Physische Geographie (IPG) der Universität Freiburg, 1. Oktober 2001, abgerufen am 14. Dezember 2010.
- Programmdownload (Win) „Air Humid Handling“ zum Berechnen mithilfe des Mollier h-x-Diagramms
- www.unitica.de: Wasserdampftafel. (Excel-Tabelle; 156 kB) mit den spezifischen Zustandsgrössen Volumen v, Enthalpie h, innere Energie u, Entropie s und isobare Wärmekapazität cp von 0.05 bis 500 bar und 0 bis 800 °C. Archiviert vom am 28. September 2007; abgerufen am 14. Dezember 2010.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Wasserdampftafel.
- ↑ Tropopause iacweb.Ethz.ch, Figure 26
- ↑ Solarkonstante und Strahlstärke LeifiPhysik.de, abgerufen am 25. November 21
- ↑ Direkte Sonnenseinstrahlung HLNuG.de, abgerufen am 25. November 21
- ↑ NASA Facts (1999): Clouds and the Energy Cycle ( vom 26. Februar 2007 im Internet Archive) (PDF-Datei; 85 kB).
- ↑ Wasserdampf ist Treibhausgas Nr. 1 • Studie unter Jülicher Leitung ( vom 5. April 2008 im Internet Archive), Forschungszentrums Jülich, Pressemitteilung vom 31. Mai 2001.
- ↑ Stefan Rahmstorf: Klimawandel – einige Fakten. In: Aus Politik und Zeitgeschichte (APuZ 47/2007).
- ↑ A. Raval, Veerabhadran Ramanathan: Observational determination of the greenhouse effect. In: Nature. 342. Jahrgang, Nr. 6251, 1989, S. 758–761, doi:10.1038/342758a0 (nature.com).
- ↑ S. Rahmstorf, H.J. Schellnhuber: Der Klimawandel. C.H. Beck, 6. Auflage 2007
- ↑ a b Brian Soden. In: Volker Mrasek: Wasserdampf-Zunahme in der Atmosphäre, Deutschlandfunk, Forschung Aktuell, 29. Juli 2014.
- ↑ J. Hansen, D. Johnson, A. Lacis, S. Lebedeff, P. Lee, D. Rind, G. Russell: Climate Impact of Increasing Atmospheric Carbon Dioxide. In: Science. 213. Jahrgang, Nr. 4511, 28. August 1981, S. 957, doi:10.1126/science.213.4511.957 (atmos.washington.edu ( des vom 3. Januar 2017 im Internet Archive) [abgerufen am 18. August 2016]).
- ↑ M. J. Way, Anthony D. Del Genio: Venusian Habitable Climate Scenarios: Modeling Venus Through Time and Applications to Slowly Rotating Venus‐Like Exoplanets. In: JGR Planets. 125. Jahrgang, Nr. 5, Mai 2020, doi:10.1029/2019JE006276 (englisch, arxiv.org [PDF]).
- ↑ Paul Sutter: How Venus Turned Into Hell, and How the Earth Is Next. In: space.com. 2019, abgerufen am 31. August 2019 (englisch).
- ↑ ist ausströmender heißer Wasserdampf bei Entspannung von 16 bar eine wirksame Zündquelle für brennbare Dampf-Luft-Gemische? Berufsgenossenschaft Rohstoffe und chemische Industrie (BG RCI), abgerufen am 28. Januar 2024.


















![{\displaystyle {\theta }={\sqrt[{4}]{p}}\cdot 100}](https://wikimedia.org/api/rest_v1/media/math/render/svg/62146acb77ddf951bc0e882e8d11b623f8592b6d)

