2,2,3-Trimethylbutan
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 2,2,3-Trimethylbutan | |||||||||||||||
| Andere Namen |
Triptan | |||||||||||||||
| Summenformel | C7H16 | |||||||||||||||
| Kurzbeschreibung |
farblose, leichtentzündbare Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 100,21 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,69 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
81 °C[1] | |||||||||||||||
| Dampfdruck |
385 mbar (50 °C)[1] | |||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (5,7 mg·l−1 bei 25 °C)[1] | |||||||||||||||
| Brechungsindex |
1,3864 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
2,2,3-Trimethylbutan ist eine chemische Verbindung aus der Gruppe der aliphatischen gesättigten Kohlenwasserstoffe. Es ist eines der neun Konstitutionsisomere des Heptans.
Gewinnung und Darstellung
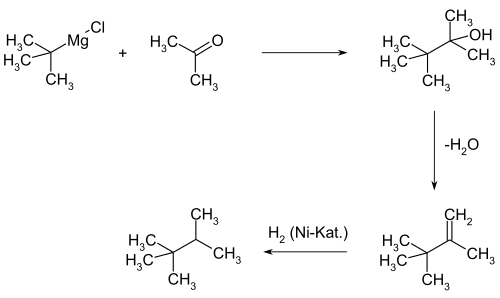
[Bearbeiten | Quelltext bearbeiten]2,2,3-Trimethylbutan kommt im Erdöl vor.[4] Die Verbindung kann aus Crackgasen[5] oder durch Hydrodesalkylierung von Isooctan[5] sowie in geringen Anteilen durch die Isomerisierung von n-Heptan[6][7] hergestellt werden. Schon 1927 wurde eine Laborsynthese beschrieben, bei der die Grignardverbindung aus tert.-Butylchlorid mit Aceton umgesetzt wird. Das resultierende 2,2,3-Trimethylbutan-3-ol wird zum 2,3,3-Trimethylbut-1-en dehydratisiert und anschließend mittels Nickelkatalysator zum 2,2,3-Trimethylbutan hydriert.[8]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]2,2,3-Trimethylbutan ist ein leichtentzündliche und farblose Flüssigkeit.[1] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 3,9222, B = 1203,362 und C = −46,776 im Temperaturbereich von 286 bis 355 K[9] Die Temperaturabhängigkeit der Verdampfungsenthalpie lässt sich entsprechend der Gleichung ΔVH0=Aexp(−βTr)(1−Tr)β (ΔVH0 in kJ/mol, Tr =(T/Tc) reduzierte Temperatur) mit A = 46,76 kJ/mol, β = 0,2726 und Tc = 531,1 K im Temperaturbereich zwischen 298 K und 353 K beschreiben.[10] In fester Phase können zwei polymorphen Kristallformen auftreten. Unterhalb von −151,75 °C existiert die Kristallform II, oberhalb dieser Temperatur die Kristallform I.[11] Die Umwandlungsenthalpie des Festphasenübergangs beträgt 2,242 kJ·mol−1.[11] Die Kristallform I schmilzt bei −25,45 °C.[2]
Die wichtigsten thermodynamischen Eigenschaften sind in der folgenden Tabelle aufgelistet:
| Eigenschaft | Typ | Wert [Einheit] |
|---|---|---|
| Standardbildungsenthalpie | ΔfH0gas ΔfH0liquid |
−205,9 kJ·mol−1[12] −238 kJ·mol−1[12] |
| Verbrennungsenthalpie | ΔcH0liquid | −4803 kJ·mol−1[12] |
| Wärmekapazität | cp | 213,51 J·mol−1·K−1 (25 °C)[11] als Flüssigkeit |
| Schmelzenthalpie | ΔfH0 | 2,2 kJ·mol−1[2] beim Schmelzpunkt |
| Schmelzentropie | ΔfS0 | 8,88 kJ·mol−1[2] beim Schmelzpunkt |
| Verdampfungsenthalpie | ΔVH0 | 28,9 kJ·mol−1[10] beim Normaldrucksiedepunkt 32,19 kJ·mol−1[10] bei 25 °C |
| Kritische Temperatur | TC | 257,9 °C[13] |
| Kritischer Druck | PC | 29,5 bar[13] |
| Kritisches Volumen | VC | 0,398 l·mol−1[13] |
| Kritische Dichte | ρC | 2,51 mol·l−1[13] |
Sicherheitstechnische Kenngrößen
[Bearbeiten | Quelltext bearbeiten]2,2,3-Trimethylbutan bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von −19 °C.[1] Die Zündtemperatur beträgt 450 °C.[1] Der Stoff fällt somit in die Temperaturklasse T2.
Verwendung
[Bearbeiten | Quelltext bearbeiten]2,2,3-Trimethylbutan wird als hochwertiger, sehr klopffester Flugzeugkraftstoff mit der Octanzahl 112 verwendet.[5] Zudem dient die Substanz als Bezugssubstanz in der Gaschromatographie.[5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j Eintrag zu 2,2,3-Trimethylbutan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- ↑ a b c d Domalski, E.S.; Hearing, E.D.: Heat Capacities and Entropies of Organic Compounds in the Condensed Phase. Volume III. In: J. Phys. Chem. Ref. Data 25 (1996) 1–525. doi:10.1063/1.555985.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-506.
- ↑ Lindeman, L.P.; Annis, J.L.: Use of a conventional mass spectrometer as a detector for gas chromatography in Anal. Chem. 32 (1960) 1742–1747, doi:10.1021/ac50153a011.
- ↑ a b c d Eintrag zu 2,2,3-Trimethylbutan. In: Römpp Online. Georg Thieme Verlag, abgerufen am 14. Juni 2014.
- ↑ Haensel, V.; Donaldson, G.R.: Platforming of Pure Hydrocarbons in Ind. Eng. Chem. 43 (1951) 2102–2104, doi:10.1021/ie50501a036.
- ↑ Blomsma, E.; Martens, J.A.; Jacobs, P.A.: Reaction Mechanisms of Isomerization and Cracking of Heptane on Pd/H-Beta Zeolite in J. Catal. 155 (1995) 141–147, doi:10.1006/jcat.1995.1195.
- ↑ Edgar, G.; Calingaert, G.; Marker, R.E.: The preparation and properties of the isomeric heptanes. Part I. Preparation in J. Am. Chem. Soc. 51 (1929) 1483–1491, doi:10.1021/ja01380a027.
- ↑ Forziati, A.F.; Norris, W.R.; Rossini, F.D.: Vapor Pressures and Boiling Points of Sixty API-NBS Hydrocarbons in J. Res. Natl. Bur. Stand. (U.S.) 43 (1949) 555–567.
- ↑ a b c Majer, V.; Svoboda, V.: Enthalpies of Vaporization of Organic Compounds: A Critical Review and Data Compilation, Blackwell Scientific Publications, Oxford, 1985, S. 300.
- ↑ a b c Huffman, H.M.; Gross, M.E.; Scott, D.W.; McCullough, I.P.: Low temperature thermodynamic properties of six isomeric heptanes in J. Phys. Chem. 65 (1961) 495-503, doi:10.1021/j100821a026.
- ↑ a b c Davies, G.F.; Gilbert, E.C.: Heats of combustion and formation of the nine isomeric heptanes in the liquid state in J. Am. Chem. Soc. 63 (1941) 2730–2732, doi:10.1021/ja01855a064.
- ↑ a b c d Daubert, T. E.: Vapor-Liquid Critical Properties of Elements and Compounds. 5. Branched Alkanes and Cycloalkanes in J. Chem. Eng. Data 41 (1996) 365–372, doi:10.1021/je9501548.