2-Fluornaphthalin
Zur Navigation springen
Zur Suche springen
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 2-Fluornaphthalin | |||||||||||||||
| Andere Namen |
β-Fluornaphthalin | |||||||||||||||
| Summenformel | C10H7F | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 146,16 g·mol−1 | |||||||||||||||
| Schmelzpunkt |
58 °C[1] | |||||||||||||||
| Siedepunkt |
212 °C[1] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
2-Fluornaphthalin (β-Fluornaphthalin) ist eine chemische Verbindung des Fluors aus der Gruppe der Naphthalinderivate und zählt zu den Fluoraromaten. 2-Fluornaphthalin ist isomer zu 1-Fluornaphthalin.
Gewinnung und Darstellung
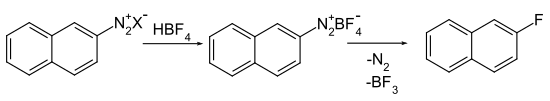
[Bearbeiten | Quelltext bearbeiten]Arylfluoride werden in einer Schiemann-Reaktion aus Diazoniumfluoroboraten dargestellt.[4][5]
Auch die Fluorierung mit N-Fluorobis(phenylsulfonyl)amin ist möglich.[6]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Es handelt sich um einen weißen Feststoff.
Verwendung und Reaktionen
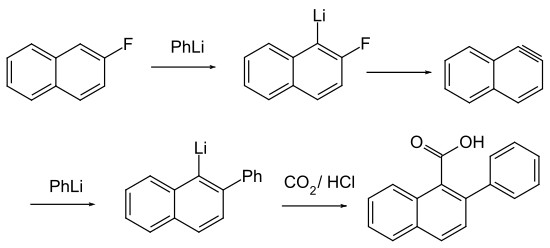
[Bearbeiten | Quelltext bearbeiten]Die fluorierten Aromaten werden für Kupplungsreaktionen von Arylen verwendet.[7]
Literatur
[Bearbeiten | Quelltext bearbeiten]- Nobuo Nakata: Versuche zur Frage des Naphthalin-Modells. In: Berichte der deutschen chemischen Gesellschaft. Band 64, Nr. 8, 1931, S. 2059–2069, doi:10.1002/cber.19310640829.
- Günther Schiemann, Werner Gueffroy, Wolfgang Winkelmüller: Fluorverbindungen des Naphtalins. In: Liebigs Annalen. Band 487, Nr. 1, 1931, S. 270–287, doi:10.1002/jlac.19314870118.
- F. W. McLafferty: Mass Spectrometric Analysis. Aromatic Halogenated Compounds. In: Analytical Chemistry. Band 34, Nr. 1, 1962, S. 16–25, doi:10.1021/ac60181a004.
- Haget Bouillard, Y. et al. Acta Cryst. 1972, 28, 3400. in A. I. Kitaigorodsk: Mixed Crystals, 33, Springer Series in Solid-State Sciences, 377. ISBN 978-3-642-81672-7.
- David Doddrell, Michael Barfield, William Adcock, Mohammad Aurangzeb, David Jordan: 13C nuclear magnetic resonance studies of some fluorinated and trifluoromethylated aromatic compounds. Studies on 13C–19F coupling constants. In: J. Chem. Soc., Perkin Trans. 2. Band 0, Nr. 4, 1976, S. 402–412, doi:10.1039/P29760000402.
- Jason R. Loader, Stefano Libri, Anthony J. H. M. Meijer, Robin N. Perutz, Lee Brammer: Highly fluorinated naphthalenes and bifurcated C–H⋯F–C hydrogen bonding. In: CrystEngComm. Band 16, Nr. 41, 2014, S. 9711–9720, doi:10.1039/c4ce01322k.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d William M. Haynes: CRC Handbook of Chemistry and Physics, 93rd edition. CRC Press, 2012, ISBN 978-1-4398-8049-4, S. 276 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Datenblatt 2-Fluoronaphthalene solution, 2000 μg/mL in methylene chloride bei Sigma-Aldrich, abgerufen am 3. Dezember 2017 (PDF).
- ↑ Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von 2-fluoronaphthalene im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 3. Dezember 2017.
- ↑ H. Meislich, H. Nechamkin, J. Sharefkin: Organische Chemie. Schaum, Mc Graw Hill Book Company 1980, ISBN 007-092028-2, 404.
- ↑ Jerry March: Advanced Organic Chemistry, S. 1929–1985, 602, ISBN 0-471-85472-7.
- ↑ G. I. Borodkin, I. R. Elanov, and V. G. Shubin: Fluorination of Bi- and Polycyclic Aromatic Hydrocarbons with N-Fluorobis(phenylsulfonyl)amine in the Absence of Solvent. In: Zhurnal Organicheskoi Khimii, 2010, Vol. 46, No. 9, S. 1318–1323.
- ↑ R. Huisgen et al.: Die Reaktion aromatischer Fluorverbindungen mit Phenyl-lithium; ein Beitrag zum Chemismus der Umlagerungen bei nucleophilen aromatischen Substitutionen, 1955, doi:10.1002/jlac.19555940204.