2-Imidazolidinon
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
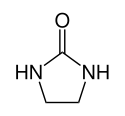
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2-Imidazolidinon | ||||||||||||||||||
| Andere Namen |
Ethylenharnstoff | ||||||||||||||||||
| Summenformel | C3H6N2O | ||||||||||||||||||
| Kurzbeschreibung |
farbloser bis gelblicher Feststoff mit schwachem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 86,05 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[2] | ||||||||||||||||||
| Dichte |
1,44 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
335,5 °C[1] | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
2-Imidazolidinon (Trivialname: Ethylenharnstoff) ist eine chemische Verbindung und eines der zwei möglichen Imidazolidinone.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Die früheste Synthese von 2-Imidazolidinon wurde 1886 von Emil Fischer und H. Koch publiziert. Die Autoren berichten von der Reaktion von Ethylendiamin mit Ethylencarbonat. Bei dieser Reaktion wechselt die Carbonylgruppe aus dem Ethylencarbonat zum Diamin und es bleibt eine stöchiometrische Menge Ethylenglycol zurück. Damit die Reaktion abläuft muss ein lösungsmittelfreies Gemisch der beiden Edukte auf 180 °C erhitzt werden.[4]
Im Jahr 1901 beschrieben Julius Tafel und Ludwig Reindl die elektrochemische Reduktion von Parabansäure, bei der 2-Imidazolidinon als Nebenprodukt entstand. Es ist schwer aus dem Produktgemisch zu isolieren. Es entsteht stattdessen hauptsächlich Hydantoin.[6]
Theodor Curtius und Wilhelm Hechtenberg gewannen 1922 das 2-Imidazolidinon aus Ethylendiisocyanat[7] durch Reaktion mit Wasser unter Eliminierung von Kohlenstoffdioxid über eine Cyclokondensation.[5]
1946 setzten Duschinsky und Dolan 2-Hydroxyimidazol[8] durch Reduktion mit Wasserstoff am Platin(II)-oxid zum Produkt um.[3]
Durch Umkristallisation aus Chloroform lässt sich 2-Imidazolidinon aufreinigen.[4][5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]2-Imidazolidon ist ein brennbarer, schwer entzündbarer, farbloser bis gelblicher Feststoff mit schwachem Geruch, der leicht löslich in Wasser ist. Seine wässrige Lösung reagiert alkalisch.[1] Er kristallisiert in farblosen Prismen.[5]
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Eintrag zu 2-Imidazolidon in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Januar 2024. (JavaScript erforderlich)
- ↑ a b Datenblatt 2-Imidazolidon bei Sigma-Aldrich, abgerufen am 4. September 2022 (PDF).
- ↑ a b R. Duschinsky, L. A. Dolan: Studies in the Imidazolone Series. The Synthesis of a Lower and a Higher Homolog of Desthiobiotin and of Related Substances1. In: Journal of the American Chemical Society. Band 68, Nr. 11, 1946, S. 2350–2355, doi:10.1021/ja01215a064.
- ↑ a b c d e Fischer, Emil and Koch, H: III. Ueber einige Derivate des Trimethylen-und Aethylendiamins. In: Justus Liebigs Annalen der Chemie. Band 232, Nr. 2, 1886, S. 222–228, doi:10.1002/jlac.18862320211.
- ↑ a b c d Curtius, Theodor and Hechtenberg, Wilhelm: Synthese des β-Alanin aus Succinylglycinester. In: Journal für Praktische Chemie. Band 105, Nr. 1, 1922, S. 289–318, doi:10.1002/prac.19231050125.
- ↑ J. Tafel, L. Reindl: Elektrolytische Reduction einiger cyclischer Ureïde. In: Berichte der deutschen chemischen Gesellschaft. Band 34, Nr. 3, 1901, S. 3286–3291, doi:10.1002/cber.19010340310.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Ethylendiisocyanat: CAS-Nr.: 929-26-0, PubChem: 11521073, ChemSpider: 9695860, Wikidata: Q82295024.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 2-Hydroxyimidazol: CAS-Nr.: 5918-93-4, EG-Nr.: 852-506-3, ECHA-InfoCard: 100.302.640, PubChem: 22208, ChemSpider: 20850, Wikidata: Q27122279.

