2-Octanol
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
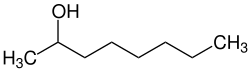
| ||||||||||
| Vereinfachte Strukturformel ohne Stereochemie | ||||||||||
| Allgemeines | ||||||||||
| Name | 2-Octanol | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C8H18O | |||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit aromatischem Geruch[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 130,23 g·mol−1 | |||||||||
| Aggregatzustand |
flüssig[1] | |||||||||
| Dichte |
0,82 g·cm−3[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
180 °C[1] | |||||||||
| Dampfdruck | ||||||||||
| Löslichkeit | ||||||||||
| Brechungsindex |
1,4260 (20 °C)[3] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Toxikologische Daten | ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||
2-Octanol ist eine chemische Verbindung aus der Gruppe der Alkohole. Es ist zugleich ein chiraler sekundärer Alkohol.
Isomere
[Bearbeiten | Quelltext bearbeiten]Wenn in diesem Artikel oder in der wissenschaftlichen Literatur „2-Octanol“ ohne Präfix erwähnt wird, ist das Racemat (±)-2-Octanol [Synonym: (RS)-2-Octanol] gemeint, ein 1:1-Gemisch von (R)-2-Octanol und (S)-2-Octanol.
Neben dem 2-Octanol existieren Strukturisomere von Octanol, und zwar 1-Octanol, 3-Octanol und 4-Octanol.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]2-Octanol kommt natürlich in Geranienöl,[4] Minze[4], Lavendel,[4] Garten-Senfrauke (Eruca sativa),[5] Rooibos (Aspalathus linearis),[6] Buchweizen (Fagopyrum esculentum),[6] Ingwer (Zingiber officinale),[6] Mais (Zea mays)[6] und Frucht-Salbei (Salvia dorisiana)[5] vor.
-
Geranie
-
Grüne Minze
-
Lavendel
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]2-Octanol kann durch alkalische Hydrolyse von Rizinusöl zu Natriumrizinolat und anschließende Pyrolyse gewonnen werden, wobei auch 2-Octanon und Wasserstoff entstehen. Dadurch enthält das technische Produkt etwa 15 % 2-Octanon.[4]
Es kann auch durch eine Grignard-Reaktion von Ethylmagnesiumbromid und Hexanal oder Hexylmagnesiumbromid mit Acetaldehyd hergestellt werden.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]2-Octanol ist eine brennbare, schwer entzündbare, wenig flüchtige, farblose Flüssigkeit mit aromatischem Geruch, die schwer löslich in Wasser ist.[1] Sie kann mit Säuren und einem geeigneten Katalysator verestert, zu Ketonen oxidiert und zu Olefinen dehydratisiert werden.[4]
Biologische Bedeutung
[Bearbeiten | Quelltext bearbeiten]Neben 1-Octanol und Isoamylacetat (Essigsäureisopentylester) ist 2-Octanol ein Alarmpheromon der Honigbiene.[7][8]
Verwendung
[Bearbeiten | Quelltext bearbeiten]2-Octanol wird in Aromen, Farben und Beschichtungen, Antischaummitteln, als schwerflüchtiges Lösungsmittel, in Schmierstoffen, Kraftstoffen, Farben und Lacken verwendet. Es wird als Entschäumer in Benetzungsmitteln eingesetzt und ist ein Zwischenprodukt bei der Herstellung von Tensiden, kosmetischen Emolliens und Weichmachern. Ferner wird es auch als Edukt in der Synthese von pharmazeutischen Verbindungen und Piperin-Derivate eingesetzt. Zusätzlich wird es als Alternative von 2-Ethylhexanol eingeschätzt.[3]
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Die Dämpfe von 2-Octanol können mit Luft ein explosionsfähiges Gemisch (Flammpunkt 71 °C, Zündtemperatur 265 °C) bilden.[1]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j k Eintrag zu 2-Octanol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ Shmuel Yannai: Dictionary of Food Compounds with CD-ROM, Second Edition. CRC Press, 2012, ISBN 978-1-4200-8351-4, S. 1440 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c d Datenblatt (±)-2-Octanol, 98% bei Alfa Aesar, abgerufen am 9. Juli 2016 (Seite nicht mehr abrufbar).
- ↑ a b c d e Philip H. Howard: Handbook of Environmental Fate and Exposure Data for Organic Chemicals. CRC Press, 1993, ISBN 978-0-87371-413-6, S. 469 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b 2-OCTANOL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 25. Juli 2021.
- ↑ a b c d OCTAN-2-OL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 25. Juli 2021.
- ↑ W.M. Getz, R.P. Akers: Olfactory response characteristics and tuning structure of placodes in the honey bee Apis mellifera L. In: Apidologie, 1993 Vol 24 S. 195–217.
- ↑ D. A. Shearer, R. Boch: 2-Heptanone in the Mandibular Gland Secretion of the Honey-bee. In: Nature. Band 206, 1965, S. 530, doi:10.1038/206530a0.



