Dichloraniline
Die Dichloraniline bilden eine Stoffgruppe von aromatischen Verbindungen, die sich sowohl vom Anilin als auch von Chlorbenzol ableiten. Die Struktur besteht aus einem Benzolring mit angefügter Aminogruppe (–NH2) und zwei Chlor (–Cl) als Substituenten. Durch deren unterschiedliche Anordnung ergeben sich sechs Konstitutionsisomere mit der Summenformel C6H5Cl2N. Alle Stoffe sind in Wasser schwer löslich und giftig.
| Dichloraniline | |||||||||||||||
| Name | 2,3-Dichloranilin | 2,4-Dichloranilin | 2,5-Dichloranilin | 2,6-Dichloranilin | 3,4-Dichloranilin | 3,5-Dichloranilin | |||||||||
| Andere Namen | 1-Amino- 2,3-dichlorbenzol, 2,3-Dichlorphenylamin, 2,3-Dichlorbenzolamin, 2,3-DCA |
1-Amino- 2,4-dichlorbenzol, 2,4-Dichlorphenylamin, 2,4-Dichlorbenzolamin, 2,4-DCA |
1-Amino- 2,5-dichlorbenzol, 2,5-Dichlorphenylamin, 2,5-Dichlorbenzolamin, 2,5-DCA, Echtscharlach GG Base |
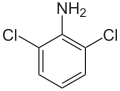
1-Amino- 2,6-dichlorbenzol, 2,6-Dichlorphenylamin, 2,6-Dichlorbenzolamin, 2,6-DCA |
1-Amino- 3,4-dichlorbenzol, 3,4-Dichlorphenylamin, 3,4-Dichlorbenzolamin, 3,4-DCA |
1-Amino- 3,5-dichlorbenzol, 3,5-Dichlorphenylamin, 3,5-Dichlorbenzolamin, 3,5-DCA | |||||||||
| Strukturformel | 
|

|

|
|

|

| |||||||||
| CAS-Nummer | 608-27-5 | 554-00-7 | 95-82-9 | 608-31-1 | 95-76-1 | 626-43-7 | |||||||||
| PubChem | 11844 | 11123 | 7262 | 11846 | 7257 | 12281 | |||||||||
| ECHA-InfoCard | 100.009.235 | 100.008.235 | 100.002.233 | 100.009.237 | 100.002.227 | 100.009.954 | |||||||||
| Summenformel | C6H5Cl2N | ||||||||||||||
| Molare Masse | 162,02 g·mol−1 | ||||||||||||||
| Aggregatzustand | fest | ||||||||||||||
| Kurzbeschreibung | brennbare, kristalline Feststoffe | ||||||||||||||
| Schmelzpunkt | 23–24 °C[1] | 62 °C[2] | 50 °C[3] | 36–38 °C[4] | 70–72 °C[5] | 51–53 °C[6] | |||||||||
| Siedepunkt | 252 °C[1] | 242 °C[2] | 251 °C[3] | 228 °C[4] | 272 °C[5] | 259–260 °C[6] | |||||||||
| Dichte | 1,38 g·cm−3 (bei 20 °C)[1] | 1,56 g·cm−3 (bei 20 °C)[2] | 1,54 g·cm−3 (bei 20 °C)[3] | 1,28 g·cm−3 (bei 20 °C)[4] | 1,57 g·cm−3 (bei 20 °C)[5] | 1,58 g·cm−3 (bei 20 °C)[6] | |||||||||
| Löslichkeit | 0,75–1 g·l−1 (bei 20 °C)[1] | 0,45 g·l−1 (bei 20 °C)[2] | 0,56 g·l−1 (bei 20 °C)[3] | 1,6 g·l−1 (bei 20 °C)[4] | 0,58 g·l−1 (bei 20 °C)[5] | 0,78 g·l−1 (bei 20 °C)[6] | |||||||||
| Flammpunkt | 115 °C[1] | 115 °C[2] | 139 °C[3] | 118 °C[4] | 135 °C[5] | 133 °C[6] | |||||||||
| Zündtemperatur | >600 °C[2] | >540 °C[3] | >600 °C[4] | >600 °C[5] | 620 °C[6] | ||||||||||
| GHS- Kennzeichnung |
|
|
| ||||||||||||
| H- und P-Sätze | 301‐311‐331‐373‐410[1][2][3][4] | 301‐311‐331‐317‐318‐410[5] | 301‐311‐331‐373‐410[6] | ||||||||||||
| keine EUH-Sätze | |||||||||||||||
| 261‐273‐280- 301+310‐501[1] |
273‐280‐301+310+330- 302+352+312‐304+340+311‐314[2] |
261‐273‐280- 301+310‐311‐501[3] |
261‐273‐280- 301+310‐311‐501[4] |
261‐273‐280‐301+310- 305+351+338‐311[5] |
261‐273‐280- 301+310‐311‐501[6] | ||||||||||
| Tox-Daten | 1600 mg·kg−1 (LD50, Ratte, oral)[2] | 1600 mg·kg−1 (LD50, Ratte, oral)[3] | 545 mg·kg−1 (LD50, Ratte, oral)[5] | ||||||||||||
Darstellung
[Bearbeiten | Quelltext bearbeiten]Dichloraniline können durch Hydrierung von Dichlornitrobenzolen mit Wasserstoff mit Hilfe eines Edelmetallkatalysators bei Temperaturen von 80 bis 180 °C und Drücken von 0,3 bis 15 MPa gewonnen werden.[7]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Alle Dichloraniline werden als Zwischenprodukte zur Herstellung von Arzneistoffen, Farbstoffen, Schädlingsbekämpfungsmitteln und Pflanzenschutzmitteln, aber auch Flammschutzmitteln und Polymeren verwendet. So wird z. B. 3,4-Dichloranilin zu Diethofencarb und – über 3,4-Dichlorphenylisocyanat – zu Diuron sowie 3,5-Dichloranilin zu Vinclozolin verarbeitet. Weltweit werden etwa 45.000 t 3,4-Dichloranilin pro Jahr produziert (Stand 1997).[8]
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h Eintrag zu 2,3-Dichloranilin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Dezember 2019. (JavaScript erforderlich)
- ↑ a b c d e f g h i j Eintrag zu 2,4-Dichloranilin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ a b c d e f g h i j Eintrag zu 2,5-Dichloranilin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Dezember 2019. (JavaScript erforderlich)
- ↑ a b c d e f g h i Eintrag zu 2,6-Dichloranilin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Dezember 2019. (JavaScript erforderlich)
- ↑ a b c d e f g h i j Eintrag zu 3,4-Dichloranilin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Dezember 2019. (JavaScript erforderlich)
- ↑ a b c d e f g h i Eintrag zu 3,5-Dichloranilin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Dezember 2019. (JavaScript erforderlich)
- ↑ Toxikologische Bewertung von 3,4-Dichloranilin und 2,5-Dichloranilin (PDF) bei der Berufsgenossenschaft Rohstoffe und chemische Industrie (BG RCI), abgerufen am 22. August 2012.
- ↑ Gefahren durch hormonell wirksame Pestizide und Biozide. ( vom 9. November 2012 im Internet Archive) (PDF; 1,1 MB)



