Ammoniumchlorat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 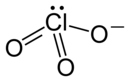
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Ammoniumchlorat | |||||||||||||||
| Summenformel | NH4ClO3 | |||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 101,49 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
1,91 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
leicht löslich in Wasser[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Ammoniumchlorat ist eine chemische Verbindung aus der Gruppe der Ammoniumverbindungen und Chlorate.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Ammoniumchlorat kann durch Reaktion von Kaliumchlorat mit Ammoniumsulfat gewonnen werden.[2]
Es kann ebenfalls durch Reaktion einer Chlorsäurelösung mit der stöchiometrisch notwendigen Menge an Ammoniak oder Ammoniumcarbonat[2]
oder durch Reaktion von Bariumchlorat mit Ammoniumsulfat dargestellt werden.[2]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Ammoniumchlorat ist ein unbeständiger farbloser Feststoff, der sehr leicht löslich in Wasser ist und in Form kleiner nadelförmiger Kristalle vorliegt. Beim Umgang mit der Verbindung ist Vorsicht geboten, da die Substanz bisweilen ohne erkennbaren Anlass, bestimmt aber bei Temperaturen über 100 °C, explodiert. In dünner Schicht offen ausgebreitet, ist die Substanz ungefährlich zu handhaben.[2] Er besitzt eine trigonale Kristallstruktur mit der Raumgruppe R3m (Raumgruppen-Nr. 160).[1]
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e Jean d’Ans, Ellen Lax, Roger Blachnik: Taschenbuch für Chemiker und Physiker. Springer DE, 1998, ISBN 3-642-58842-5, S. 588 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c d e Georg Brauer, unter Mitarbeit von Marianne Baudler u. a. (Hrsg.): Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band 1. Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 324.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.



