Bariumpropionat
Zur Navigation springen
Zur Suche springen
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
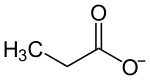 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Bariumpropionat | |||||||||||||||
| Andere Namen |
Bariumpropanoat | |||||||||||||||
| Summenformel | C6H10BaO4 | |||||||||||||||
| Kurzbeschreibung |
farblose voluminöse Prismen[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 283,47 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Siedepunkt |
300 °C (Zersetzung)[1] | |||||||||||||||
| pKS-Wert |
4,88[2] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Bariumpropionat ist das Bariumsalz der Propionsäure.
Herstellung
[Bearbeiten | Quelltext bearbeiten]Bariumpropionat kann durch Reaktion von Bariumhydroxid mit Propionsäure dargestellt werden.[5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Bariumpropionat bildet verschiedene Hydrate: ein Monohydrat, das bei 110 °C sein Kristallwasser abgibt, ein Tri- und ein Hexahydrat.[1]
Beim trockenen Erhitzen auf 460 °C zersetzt sich Bariumpropionat in 3-Pentanon und Bariumcarbonat.[6]
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Eintrag zu Barium propionate (IR Spectrum). In: P. J. Linstrom, W. G. Mallard (Hrsg.): NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e A. Renard: "Sur les propionates métalliques" in Comptes rend. hebd. 1887, 104, S. 913–917. Volltext
- ↑ W. L. F. Armarego, Christina Li Lin Chai: "Purification of laboratory chemicals", Verlag Butterworth-Heinemann, 2003, ISBN 9780750675710, S. 399. (eingeschränkte Vorschau in der Google-Buchsuche)
- ↑ H. J. Wing, T. J. Thompson: "The solubility of Barium propionate" in J. Am. Chem. Soc 1926, 48(1), S. 104–106, doi:10.1021/ja01412a014.
- ↑ Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von Barium dipropionate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 28. Dezember 2019.
- ↑ U. Hasenkox, S. Hoffmann, R. Waser: "Influence of Precursor Chemistry on the Formation of MTiO3 (M = Ba, Sr) Ceramic Thin Films" in Journal of Sol-Gel Science and Technology 1998, 12(2), S. 67–79. doi:10.1023/A:1026480027046
- ↑ A. T. Johns: "The Mechanism of Propionic Acid Formation by Veillonella gazogenes" in J. gen. Microbiol. 1951, 5, S. 326–336. doi:10.1099/00221287-5-2-326, PMID 14832421.

