Paracetamol
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Paracetamol | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C8H9NO2 | |||||||||||||||||||||
| Kurzbeschreibung | ||||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus |
Hemmung der Cyclooxygenase-2 (COX-2) im Rückenmark[4] | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 151,16 g·mol−1 | |||||||||||||||||||||
| Dichte |
1,29 g·cm−3 (21 °C)[2] | |||||||||||||||||||||
| Schmelzpunkt |
| |||||||||||||||||||||
| pKS-Wert |
9,38[7] | |||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
10 mg·m−3[2] | |||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Paracetamol (auch Acetaminophen, als Kontraktionen des chemischen Namens para-(Acetylamino)phenol) ist ein schmerzlindernder und fiebersenkender Arzneistoff aus der Gruppe der Nichtopioid-Analgetika. In Nordamerika, Südamerika (außer im portugiesischsprachigen Brasilien) und in Iran ist die übliche Bezeichnung der Substanz Acetaminophen.
Paracetamol ist ein Derivat der Essigsäure und des Aminophenols p-Hydroxyanilin. Es wurde erstmals 1878 von Harmon Northrop Morse aus p-Nitrophenol in Eisessig hergestellt. Seit den 1950er Jahren wird Paracetamol mit der Einführung von Fertigarzneimitteln auch im Rahmen der Selbstmedikation als Monopräparat oder Bestandteil verschiedener Kombinationspräparate eingesetzt. Neben Acetylsalicylsäure, Ibuprofen oder Diclofenac ist Paracetamol einer der häufigsten Wirkstoffe in Präparaten, die gegen Fieber und Schmerzen eingesetzt werden. Paracetamol wirkt im Gegensatz zu diesen nicht entzündungshemmend. Seit 1977 steht Paracetamol auf der Liste der unentbehrlichen Arzneimittel der WHO.
Geschichte
[Bearbeiten | Quelltext bearbeiten]Die Herstellung von Paracetamol als Produkt der Reduktion von p-Nitrophenol mit Zink in Eisessig wurde erstmals 1878 von Harmon Northrop Morse beschrieben.[9] Josef von Mering verwendete 1887 Paracetamol erstmals heilkundlich, jedoch erweckte die Anwendung wenig Aufsehen.[10] Vorerst therapeutisch bedeutender waren die verwandten Substanzen Acetanilid und Phenacetin.[11]
1893 wurde Paracetamol erstmals im Urin einer Person nachgewiesen, die Phenacetin eingenommen hatte. 1899 wurde das Paracetamol außerdem als Stoffwechselprodukt (Metabolit) des Acetanilids erkannt. Dennoch kam es zu keiner nennenswerten Anwendung des Stoffes.

Erst nach dem Zweiten Weltkrieg wurde das Paracetamol bekannter, als es 1948 von Bernard B. Brodie und Julius Axelrod am New York City Department of Health ein zweites Mal als Metabolit von Phenacetin identifiziert wurde. Diese forschten im Regierungsauftrag nach neuen Schmerzmitteln und zeigten in ihrer Arbeit auf, dass der schmerzstillende Effekt des Acetanilids und des Phenacetins vollständig auf das Abbauprodukt dieser Stoffe, das Paracetamol, zurückzuführen ist. Sie regten an, diesen Stoff in seiner Reinform zu nutzen, um die toxischen Nebenwirkungen der Ursprungsstoffe zu vermeiden.
Seinen ersten Einsatz in einem Fertigarzneimittel fand Paracetamol 1955 in den USA in Tylenol Children’s Elixir der Firma McNeil Laboratories.[12] Seit 1956 ist Paracetamol in Tablettenform mit 500 mg Wirkstoff erhältlich und wurde in Großbritannien unter dem Markennamen Panadol verkauft, hergestellt von der Firma Frederick Stearns & Co, die ein Ableger der Sterling Drug Inc. war. Es war ausschließlich auf Rezept zu bekommen und wurde als schmerzstillendes und fiebersenkendes Mittel beworben, welches zugleich den Magen schone. Die damals bereits bekannte Acetylsalicylsäure ist weniger magenfreundlich. 1958 kam zusätzlich eine Kinderversion des Präparates mit dem Namen Panadol Elixir auf den Markt. 1959 wurde Paracetamol vom Münchener Unternehmen bene-Arzneimittel als erstes Monopräparat unter dem Markennamen ben-u-ron auf dem deutschen Markt eingeführt.[13][14]
Seit 1963 wird Paracetamol im britischen Arzneibuch, der „British Pharmacopoeia“, monographiert. Kurz danach wurde es auch in Arzneibücher anderer europäischer Staaten aufgenommen.
1982 kam es in den USA zu einem Fall von Produktsabotage,[15][16] durch dessen Folgen sich die zuständige Staatsbehörde Food and Drug Administration veranlasst sah, strengere Schutzvorschriften zu erlassen. Durch vergiftete Paracetamolpräparate waren sieben Patienten gestorben. Zurückgerufen wurden Präparate im Marktwert von 100 Millionen US-Dollar.
Anwendung
[Bearbeiten | Quelltext bearbeiten]Anwendungsgebiete (Indikationen)
[Bearbeiten | Quelltext bearbeiten]Paracetamol ist als Fertigarzneimittel zur Behandlung von leichten bis mäßig starken Schmerzen und Fieber zugelassen.[17] Verwendung findet es vor allem bei leichten Kopfschmerzen, leichten Zahnschmerzen, Regelschmerzen,[17] Sonnenbrand und arthrosebedingten Gelenkschmerzen sowie bei Migräne. Bei isolierten Extremitätenschmerzen wurde bei intravenöser Gabe eine dem Morphin vergleichbare Wirkung beschrieben.[18][19]
Ebenfalls zur Behandlung leichter bis mäßiger Schmerzen ist Paracetamol in fixer Kombination mit Coffein (400 mg Paracetamol, 50 mg Coffein) zugelassen. Diese Kombination soll eine um das 1,3- bis 1,7-fach höhere Wirkstärke als Paracetamol allein haben und ermöglicht die Reduktion der Paracetamoldosis. Coffein verkürzt zudem die Zeit bis zum Wirkungseintritt von Paracetamol.[20] Auch die Dreifachkombination von Paracetamol mit Acetylsalicylsäure und Coffein führt zu einer gesteigerten Wirksamkeit[21][22] und wird daher von der Deutschen Migräne- und Kopfschmerz-Gesellschaft als Mittel der ersten Wahl zur Behandlung der Migräne und des Spannungskopfschmerzes empfohlen.[23][24]
In fixer Kombination mit Codein (Co-Codamol) oder Tramadol ist Paracetamol zur Behandlung mäßig starker bis starker Schmerzen zugelassen.[25]
Da Erkältungskrankheiten mit Fieber, Glieder- und Kopfschmerzen einhergehen können, ist Paracetamol in Kombination mit weiteren Arzneistoffen wie Antihistaminika, Hustenlöser, Hustenblockern oder Vitamin C als analgetisch und antipyretisch wirksamer Bestandteil vieler sogenannter „Grippemittel“ bzw. „Erkältungsmittel“ zugelassen.
Gegenanzeigen (Kontraindikationen) und Warnhinweise
[Bearbeiten | Quelltext bearbeiten]Bei einer bekannten Überempfindlichkeit gegen Paracetamol oder bei einer schweren Beeinträchtigung der Leberfunktion auf Grund eines Leberversagens mit einem Child-Pugh-Score von 9 oder höher darf Paracetamol nicht angewendet werden. Bei Patienten mit Leberversagen mit einem Child-Pugh-Score von < 9, einem Gilbert-Meulengracht-Syndrom, chronischem Nierenversagen mit einer Kreatinin-Clearance von unter 10 ml/min oder einem chronischen Alkoholmissbrauch darf Paracetamol nur mit besonderer Vorsicht unter ärztlicher Kontrolle und gegebenenfalls einer angepassten Dosierung angewendet werden.[17]
Bei längerer hochdosierter, nicht bestimmungsgemäßer Anwendung von Paracetamol ist die Entstehung eines medikamenteninduzierten Kopfschmerzes möglich. Nach abruptem Absetzen verschlimmern sich die Kopfschmerz- und Begleitsymptome.[17]
Schwangerschaft und Stillzeit
[Bearbeiten | Quelltext bearbeiten]Zumeist ältere Reproduktionsstudien und epidemiologische Daten gaben keinen Hinweis auf eine schädigende Wirkung von Paracetamol auf die Gesundheit des Fetus bzw. des Neugeborenen. Zahlreiche Untersuchungen legen einen möglichen Zusammenhang zwischen der Einnahme von Paracetamol während der Schwangerschaft und einem gehäuften Auftreten von Asthma beim Kind nahe.[26][27][28] Als möglicher Pathomechanismus wird der Einfluss von Paracetamol auf die hämatopoetische Stammzellentwicklung im Nabelschnurblut diskutiert, welcher zu einer Differenzierung von Immunzellen führen kann.[29] Für eine Langzeitanwendung während der Schwangerschaft liegen keine ausreichenden Daten zur Abschätzung der Sicherheit vor.[17] Eine aktuelle Studie der Universität Oslo legt jedoch sehr deutlich nahe, dass die Einnahme von Paracetamol während Schwangerschaft und Stillzeit, insbesondere über einen längeren Zeitraum, zu einer späteren Entwicklungsverzögerung des ungeborenen Kindes führen kann. Untersucht wurden über einen Zeitraum von neun Jahren über 48.000 Kinder, darunter fast 3000 Geschwisterpaare.[30]
Der Verdacht, dass Kinder, die im Mutterleib dem Wirkstoff Paracetamol ausgesetzt waren, später verhaltensauffällig werden können, wurde durch eine Studie von Forschern der University of Bristol mit insgesamt 14.500 Müttern und ihren Kindern bestätigt. Bei sieben Jahre alten Kindern, deren Mütter zwischen der 19. und der 32. Schwangerschaftswoche Paracetamol eingenommen hatten, stieg das Risiko für Verhaltensprobleme um 46 Prozent.[31]
Forscher der Icahn School of Medicine at Mount Sinai berichteten im Januar 2018 davon, dass der Paracetamolkonsum während der Schwangerschaft im Zusammenhang mit einer erhöhten Rate der Sprachverzögerung bei Mädchen steht. In einer Erststudie dieser Art fanden die Forscher eine erhöhte Rate von Sprachverzögerungen bei Mädchen im Alter von 30 Monaten, die von Müttern geboren wurden, die zu Beginn der Schwangerschaft häufig Paracetamol verwendeten. Diese Ergebnisse stimmen mit Studien überein, die über einen verminderten IQ und erhöhte Kommunikationsprobleme bei Kindern von Müttern berichten, die während der Schwangerschaft mehr Paracetamol verwendet haben. Sich die Sprachentwicklung anzusehen ist wichtig, weil sie sich als prädiktiv für andere neurologische Entwicklungsstörungen bei Kindern erwiesen hat. Die schwedische „Environmental Longitudinal, Mother and Child, Asthma and Allergy Study“ (SELMA) lieferte Daten für diese Forschung. Informationen wurden von 754 Frauen gesammelt, die in den Wochen 8–13 ihrer Schwangerschaft in die Studie aufgenommen wurden.[32][33]
Wenngleich Paracetamol in geringen Mengen in die Muttermilch übergeht, sind bei Einnahme von Paracetamol während der Stillzeit keine unerwünschten Wirkungen für den Säugling bekannt geworden.[17]
Art der Anwendung und Dosierung
[Bearbeiten | Quelltext bearbeiten]Paracetamol kann oral, rektal oder intravenös verabreicht werden. Paracetamol wird in Abhängigkeit von Alter und Körpergewicht dosiert. Bei einer oralen Anwendung werden in der Regel 10 bis 15 mg Paracetamol pro kg Körpergewicht als Einzeldosis und bis 60 mg/kg Körpergewicht als Tagesgesamtdosis verwendet. Die maximale Tagesdosis für Jugendliche ab 12 Jahren und Erwachsene ist mit 4000 mg angegeben,[17] verteilt auf drei bis vier Einzeldosen mit einem Abstand von mindestens 6 Stunden. Bei Patienten mit Funktionsstörungen der Nieren oder der Leber werden Dosisabsenkungen vorgenommen.[17]
Wechselwirkungen
[Bearbeiten | Quelltext bearbeiten]Probenecid hemmt die Glucuronidierung von Paracetamol und somit seine Ausscheidung. Eine Hemmung der Ausscheidung von Paracetamol kann ebenfalls nach gleichzeitiger Einnahme von Salicylamid beobachtet werden. Alkohol und Arzneimittel, die als Induktoren des Cytochrom-P450-Enzymsystems wirken, wie beispielsweise Carbamazepin und Barbiturate, führen zu einer verstärkten Bildung von leberschädlichen Stoffwechselprodukten (Metaboliten) des Paracetamols. Ionenaustauscher, wie beispielsweise Colestyramin, reduzieren die Aufnahme von Paracetamol. Der Eintritt der Wirkung von Paracetamol kann durch Arzneimittel, die die Magen-Darm-Tätigkeit beeinflussen, wie beispielsweise Metoclopramid, verlangsamt oder beschleunigt werden.
Paracetamol selbst beeinflusst nur in seltenen Fällen die Wirkung anderer Arzneimittel. Bei regelmäßiger Einnahme verstärkt Paracetamol die Wirkung von Gerinnungshemmern wie Phenprocoumon und Warfarin. Auch die blutbildschädigenden Nebenwirkungen von Zidovudin können bei gleichzeitiger Einnahme von Paracetamol verstärkt werden.[17] Weiterhin mehren sich in letzter Zeit die Hinweise, dass Paracetamol und bestimmte andere Schmerzmittel aus der Gruppe der nichtsteroidalen Antiphlogistika bzw. nichtsteroidalen Antirheumatika (NSAIDs), wie z. B. Acetylsalicylsäure (Aspirin), die Wirksamkeit von Impfstoffen herabsetzen können, indem der Körper nach einer Impfung weniger der schützenden Antikörper bildet.[34][35][36][37][38] Letzteres wird darauf zurückgeführt, dass durch Medikamente wie Paracetamol die terminale Differenzierung der B-Zellen zu Antikörper-produzierenden Plasmazellen beeinträchtigt wird.[39] Forscher und Ärzte raten daher, einige Zeit vor und nach der Impfung auf entsprechende Medikamente zu verzichten.[40][41][42]
Nebenwirkungen
[Bearbeiten | Quelltext bearbeiten]Paracetamol zeigt bei bestimmungsgemäßem Gebrauch nur selten bis sehr selten unerwünschte Wirkungen. Keine der auf eine Einnahme von Paracetamol zurückzuführenden Nebenwirkungen tritt häufiger als bei einem unter 1000 Patienten auf. Dazu gehören der Anstieg bestimmter Leberenzyme (Transaminasen) im Serum (Häufigkeit: 0,01–0,1 %). Sehr selten (Häufigkeit: < 0,01 %) bzw. in Einzelfällen konnten schwerwiegende Veränderungen des Blutbildes wie Thrombozytopenie (verringerte Anzahl von Blutplättchen) und Agranulozytose beobachtet werden. Ebenso selten kann es zu allergischen Reaktionen in Form von einfachem Hautausschlag oder Nesselausschlag bis hin zu einer Schockreaktion kommen. Ebenfalls mit einer Häufigkeit von unter 0,01 % kam es bei empfindlichen Personen zu einer Verkrampfung der Atemmuskulatur (Analgetika-Asthma).[17] Bei bestimmungsgemäßer Anwendung von Paracetamol ist das Risiko einer Analgetika-Nephropathie sehr gering. Ob dieses Risiko durch eine kombinierte Anwendung mit Acetylsalicylsäure und Coffein erhöht ist, wird kontrovers diskutiert.[43]
Epidemiologische Studien bringen den Paracetamolkonsum in der Kindheit dosisabhängig mit einem langfristig erhöhten Asthmarisiko und einem erhöhten Risiko für das Auftreten von Entzündungen der Nasenschleimhaut und der Augenbindehaut (Allergische Rhinitis) sowie Hautentzündungen (Ekzem) in Verbindung.[44][45] Andere Studien widersprechen der These, dass Paracetamol Asthma fördert.[46]
Der Abbau von Paracetamol verbraucht Glutathion und kann bei älteren Patienten zu einem Mangel an schwefelhaltigen Aminosäuren führen, was generell auf Dauer über den Glutathionmangel zu kardiovaskulärer Anfälligkeit (Anfälligkeit des Blutkreislaufes) führen kann.[47]
Der längerfristige Gebrauch von Paracetamol steht im Verdacht, das Risiko für eine Reihe von Blutkrebserkrankungen zu erhöhen.[48]
Angesichts der in den vorangegangenen Jahren beobachteten schweren und lebensbedrohlichen Hautreaktionen unter der Anwendung von Paracetamol riet die FDA 2013 den Anwendern, beim Auftreten von Hautreaktionen ihren Arzt aufzusuchen und die weitere Einnahme des Präparats einzustellen. Ein entsprechender Warnhinweis sollte künftig in den USA auf den Arzneimittelpackungen von paracetamolhaltigen Präparaten abgedruckt werden.[49]
Der Pharmakovigilanzausschuss für Risikobewertung (PRAC) der Europäischen Arzneimittel-Agentur (EMA) hat im September 2017 empfohlen, Paracetamol-Präparate mit verlängerter Freisetzung vom Markt zu nehmen. Das Risiko infolge einer Überdosierung überwiege gegenüber dem Vorteil eines länger wirkenden Präparates. Eine endgültige Entscheidung der EMA dazu steht noch aus. Die betroffenen Herstellerfirmen haben noch Gelegenheit, eine weitere Überprüfung durch das PRAC zu fordern.[50]
Neue Studien deuten darauf hin, dass Paracetamol Einfluss auf Mitgefühl und Einfühlungsvermögen hat und die Risikobereitschaft erhöht.[51][52]
Die PATH-BP-Studie untersuchte den Einfluss einer regelmäßigen Paracetamol-Einnahme auf den Blutdruck bei Personen mit arterieller Hypertonie ohne chronische Schmerzen. Die 110 Teilnehmenden erhielten in einem Cross-over-Design zunächst 14 Tage lang entweder Placebo oder 4 g Paracetamol täglich. Nach einer zweiwöchigen Karenzphase wechselten sie dann in das jeweils andere Therapieschema. Jeweils zu Beginn und am Ende der Behandlungszeiträume erfolgten 24-h-Blutdruckmessungen. Unter Paracetamol-Einnahme stieg der systolische Blutdruck in den Tagesstunden im Mittel signifikant von 132,8 (±10,5) auf 136,5 (±10,1) mmHg an, unter Placebo-Einnahme fiel er hingegen von 133,9 (±10,3) auf 132,5 (±9,9) mmHg ab. Nach statistischer Bereinigung ergab sich unter Paracetamol-Einnahme im Vergleich zu Placebo ein mittlerer Blutdruckanstieg um 4,7 mmHg (95 % KI: 2,6–6,6) systolisch und 1,6 mmHg (95 % KI: 0,5–2,7) diastolisch. Die Ergebnisse zeigen, dass eine regelmäßige Paracetamol-Einnahme bei bestehender arterieller Hypertonie den Blutdruck erhöht.[53]
Schädlicher Gebrauch und Überdosierung
[Bearbeiten | Quelltext bearbeiten]Paracetamolüberdosierungen als Folge der Unkenntnis der maximalen Tagesdosis, Nichtbeachtung von Gegenanzeigen und Anwendungsbeschränkungen sowie in selbstschädigender, meist suizidaler Absicht sind häufig mit schweren Beeinträchtigungen der Leberfunktion verbunden.[54] Eine Überdosierung über 150 Milligramm pro Kilogramm Körpergewicht, entsprechend 10 Gramm für Erwachsene, kann zu einer irreversiblen Schädigung der Leberzellen oder gar zum Leberversagen führen. Alkoholiker oder Patienten mit einer verringerten Ausscheidung von Paracetamol können schon bei einer deutlich geringeren Dosis Leberschäden erleiden.[55][56] In England und Wales werden etwa 30.000 Patienten pro Jahr mit einer Paracetamolvergiftung als Folge suizidaler Absicht ins Krankenhaus eingeliefert, von denen etwa 150 der Vergiftung erliegen. Eine Beschränkung der Packungsgröße von Paracetamolpräparaten zeigte in Großbritannien erst nach ein paar Jahren eine Reduktion der Suizide.[57][58] Wie in Großbritannien[59] ist Paracetamol auch in den USA die häufigste Ursache für akutes Leberversagen, wobei etwa die Hälfte der Intoxikationen unbeabsichtigt geschehen.[54] 2011 ersuchte die US-amerikanische Zulassungsbehörde FDA die Hersteller von solchen Arzneimitteln, in denen Paracetamol mit einem Opioid kombiniert ist, die Paracetamoldosis auf 325 mg pro Dosierungseinheit zu limitieren, um das Risiko für lebertoxische Effekte zu reduzieren. Für OTC-Arzneimittel will die FDA ebenfalls Maßnahmen erarbeiten.[60]
Erste Symptome einer akuten Paracetamolvergiftung, die innerhalb der ersten 48 Stunden eintreten und nach etwa vier bis sechs Tagen ihren Höhepunkt erreichen, sind Übelkeit, Erbrechen, Appetitlosigkeit, Blässe und anhaltende Unterleibsschmerzen als Zeichen einer Leberschädigung. Gleichzeitig können klinische Werte, wie Lebertransaminasen, Laktatdehydrogenase, Bilirubinwert und Prothrombinzeit, erhöht sein. Folgt keine umgehende Behandlung, so erleiden etwa 10 % der Patienten mit einer akuten Paracetamolvergiftung eine dauerhafte, schwere Leberschädigung. Etwa 10 bis 20 % dieser Patienten wiederum sterben an den Folgen eines Leberversagens. Seltener tritt akutes Nierenversagen auf.[55] In einer Studie wurde bei Niereninsuffizienz-vorgeschädigten Patienten bei einer gleichzeitigen Einnahme von Naproxen und Paracetamol (kumulativ 0,4 und 1,0 kg über Jahre) eine Nephropathie beobachtet. Dies deutet auf einen kombinierten negativen Effekt von Naproxen und Paracetamol.[61] Andere leberunabhängige Symptome, die nach einer Paracetamolvergiftung beobachtet wurden, sind Herzmuskelanomalien und Pankreatitis.[17]
Als Ursache für die Lebertoxizität von Paracetamol gilt sein Stoffwechselprodukt N-Acetyl-p-benzochinonimin (NAPQI). Die Bildung dieses leberschädigenden Metaboliten wird durch regelmäßigen Konsum von Alkohol und Arzneimitteln mit einer enzyminduzierenden Wirkung, wie beispielsweise Carbamazepin, noch verstärkt. Ein geeignetes Gegenmittel bei einer Paracetamolvergiftung ist N-Acetylcystein, das toxische Paracetamolmetaboliten, wie N-Acetyl-p-benzochinonimid, unter Bildung ungiftiger Konjugate abfängt. Hierdurch kann eine Progression zur irreversiblen Leberschädigung oder zum Leberversagen verhindert werden, vorausgesetzt das Antidot wird rechtzeitig verabreicht.[59] N-Acetylcystein gilt als wirksam, falls es innerhalb von zehn Stunden verabreicht wird. Verschiedene Behandlungsschemata empfehlen die Anwendung von etwa 150 mg/kg Körpergewicht als Einzeldosis und eine Gesamtdosis von 300 bis 1330 mg/kg Körpergewicht verteilt über 20 bis 68 Stunden. Zu diesem Zweck steht N-Acetylcystein zur intravenösen Verabreichung als auch zur oralen Anwendung (Brausetabletten) zur Verfügung. Unmittelbar bis etwa eine Stunde nach Einnahme einer Überdosis Paracetamol kann auch Aktivkohle angewendet werden.[62] Bei einem fortgeschrittenen akuten Leberversagen ist jedoch die Lebertransplantation die einzige verbleibende Therapieoption, welche dem Patienten noch eine Überlebenschance eröffnet.[59]
Anwendung in der Tierheilkunde
[Bearbeiten | Quelltext bearbeiten]Aufgrund der potenziell leberschädigenden Wirkung sollte Paracetamol in der Tierheilkunde mit Vorsicht eingesetzt werden. Bei Katzen und Jungtieren führt die Gabe von Paracetamol sehr schnell zu Vergiftungen mit Methämoglobinbildung, Anämie, Hämoglobinurie, Leberschädigung, Gelbsucht, Atemnot und Herzrasen, da diese den Wirkstoff nur unzureichend glucuronidieren können. Hunde vertragen den Wirkstoff zwar gut,[63] aber die Wirkungsdauer ist sehr kurz (etwa zwei Stunden), so dass der Wirkstoff praktisch ohne sinnvolle Anwendung ist. Unter den Nutztieren ist die Anwendung von Paracetamol bei Schweinen erlaubt, wobei eine Rückstandmengenbegrenzung nicht notwendig ist (Anhang II der Verordnung 2377/90).[64] Auf Schlangen haben bereits geringe Mengen von Paracetamol eine tödliche Wirkung. Beispielsweise wird die invasive Braune Nachtbaumnatter auf der Pazifikinsel Guam mit Paracetamol-versehenen Ködern, die in Massen aus der Luft abgeworfen werden und sich in den Baumkronen verfangen, bekämpft.[65][66]
Pharmakologie
[Bearbeiten | Quelltext bearbeiten]Wirkungsweise (Pharmakodynamik)
[Bearbeiten | Quelltext bearbeiten]Anders als Schmerzmittel wie Acetylsalicylsäure und Ibuprofen besitzt Paracetamol nur unter Laborbedingungen eine feststellbare entzündungshemmende Wirkung. Dementsprechend wird es nicht in die Gruppe der klassischen „nicht-steroidalen Entzündungshemmer“ (auch: nicht-steroidale Antirheumatika, NSAR; englisch non-steroidal anti-inflammatory drugs, NSAID) eingeordnet. Im Gegensatz zu den klassischen NSAR hemmt Paracetamol kaum die periphere Cyclooxygenase. So treten deren typische Nebenwirkungen, wie Magengeschwüre, sehr selten auf. Paracetamol hat auch keinen Einfluss auf die Aggregation der Blutplättchen und somit keine blutgerinnungshemmende Wirkung.
Der genaue Wirkmechanismus von Paracetamol ist nicht bekannt. Bekannt ist, dass mehrere, kontrovers diskutierte Mechanismen zusammenspielen, und dass der schmerzstillende Effekt zu einem nicht unerheblichen Teil in Gehirn und Rückenmark zustande kommt.
Die Schmerzlinderung entspricht etwa der von Ibuprofen, tritt bei oraler Gabe jedoch schneller ein.[67]
Hemmung von Cyclooxygenasen
[Bearbeiten | Quelltext bearbeiten]Basierend auf den Entdeckungen John Vanes wurde lange Zeit angenommen, dass der schmerzstillende Effekt des Paracetamols auf eine Hemmung der Cyclooxygenasen, an Entzündungsreaktionen und der Schmerzentstehung beteiligte Enzyme, zurückzuführen ist.[68] Die Cyclooxygenasen sind über die Bildung von Schmerz- und Entzündungsmediatoren aus der Gruppe der Prostaglandine maßgeblich an der Schmerzweiterleitung ins Gehirn beteiligt.[69] Mit einer Hemmung der Cyclooxygenasen konnte zwar die vergleichbare analgetische Wirkstärke von Paracetamol und saurer Nicht-Opioidanalgetika, wie beispielsweise Acetylsalicylsäure und Ibuprofen, erklärt werden, aber nicht die weitgehend fehlende antiinflammatorische Wirksamkeit und die ebenso weitgehend fehlenden gastro-intestinalen Nebenwirkungen des Paracetamols. Als Ursache für diese Unterschiede wurde eine voneinander abweichende Verteilung von Paracetamol und saurer Nicht-Opioidanalgetika in Körpergewebe angenommen, wobei Paracetamol sich gleichmäßig im Körper verteilt und saure Nicht-Opioidanalgetika sich im Sinne eines Drug Targetings beispielsweise im Magen und im entzündeten Gewebe anreichern.[70] Eine weitere mögliche Erklärung wurde mit der Entdeckung des Cyclooxygenase-Isoenzyms COX-3, einer insbesondere in der Großhirnrinde vorkommenden Variante der COX-1, gefunden.[71] Diese These wurde allerdings einige Jahre später verworfen, da die COX-3 eigentlich nur eine andere splice-Variante der COX-1 darstellt und nicht ausreichend exprimiert wird, um einen biologischen Effekt hervorzurufen.[72] Neueren Untersuchungen zufolge soll eine schwach dämpfende Wirkung auf das Cyclooxygenase-Isoenzym COX-1 und eine starke auf COX-2 in vivo für die Wirkungen von Paracetamol verantwortlich sein.[4] Dies passt zu seiner schwachen Wirkung auf Thrombozyten (Blutplättchen).[73]
Wechselwirkungen mit dem Serotoninsystem
[Bearbeiten | Quelltext bearbeiten]Weitere experimentelle Daten lassen vermuten, dass Paracetamol seine Effekte über eine Aktivierung serotoninerger schmerzhemmender Mechanismen vermittelt. Insbesondere Serotonin-Rezeptoren vom Typ 5-HT3 sollen dabei eine wichtige Rolle spielen.[74] Der schmerzhemmende Effekt wird dabei auf eine Projektion serotoninerger Neurone bis in das Rückenmark zurückgeführt. Diese Hypothese über den Mechanismus des Paracetamols zeigt Analogien zur Wirkweise von Opioiden, wie Morphin.[75] Alternativ dazu kann ein schmerzstillender serotoninerger Effekt des Paracetamols auch als eine Folge der Hemmung der Prostaglandinfunktion interpretiert werden, da die meisten serotoninergen Neurone auch Prostanoidrezeptoren exprimieren.[76]
Wechselwirkungen mit dem Endocannabinoidsystem
[Bearbeiten | Quelltext bearbeiten]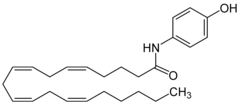
Eine Wechselwirkung von Paracetamol mit dem körpereigenen Cannabinoidsystem (Endocannabinoid-System) wurde auf Grund einer zusätzlich zur analgetischen Wirkung existierenden schwachen euphorisierenden, entspannenden und beruhigenden Wirkung von Analgetika vom Anilin-Typ vermutet.[75] In der Tat konnte eine Wechselwirkung von Paracetamol mit dem Endocannabinoidsystem in vivo nachgewiesen werden. So zeigt ein Metabolit des Paracetamols, das N-Arachidonoylphenolamin, welches insbesondere im Gehirn gebildet wird, eine antipyretische und analgetische Wirkung über eine indirekte Wirkung auf Cannabinoid-Rezeptoren. N-Arachidonoylphenolamin interagiert mit dem Vanilloid-Rezeptor TRPV1, der auf vielen, als Nozizeptoren fungierenden freien Nervenendigungen vorkommt und zusätzlich an der Regulation der Körpertemperatur beteiligt ist. Darüber hinaus hemmt dieser Paracetamolmetabolit die zelluläre Wiederaufnahme des Anandamid und führt somit zu einer Konzentrationserhöhung dieses endogenen Cannabinoids.[77][78]
Sonstige Wirkmechanismen
[Bearbeiten | Quelltext bearbeiten]Neben einer Interaktion von Paracetamol mit Cyclooxygenasen, dem Serotonin-System und dem Endocannabinoidsystem wird ein hemmender Einfluss des Paracetamols auf eine durch Glutamat oder Substanz P verursachte Hyperalgesie als Ursache für seine analgetische Wirkung diskutiert. Zusätzlich ist Paracetamol an der Hemmung der Freisetzung des Botenstoffs Stickstoffmonoxid (NO) beteiligt.[77]
Darüber hinaus gibt es Hinweise, dass Paracetamol nicht nur physischen Schmerz, sondern auch durch soziale Ausgrenzung oder eine Zurückweisung hervorgerufenes psychisches Leiden (sog. sozialer Schmerz, social pain) zu lindern vermag.[79][80] Dies ist nach Ansicht der Autoren ein Hinweis darauf, dass es hinsichtlich der betroffenen Hirnregionen eine substantielle Überlappung zwischen physischem und psychischem Schmerz gibt.
Pharmakokinetik
[Bearbeiten | Quelltext bearbeiten]
Eine Wirkung tritt bei intravenöser Gabe nach 10 bis 15 Minuten ein und hält 4 bis 6 Stunden an.[81] Bei oraler Gabe wird die maximale Wirkkonzentration von Paracetamol nach etwa 30 bis 60 Minuten erreicht. Bei rektaler Anwendung, bei der eine Bioverfügbarkeit von 68 bis 88 % erreicht wird, werden maximale Plasmakonzentrationen nach circa 3 bis 4 Stunden erreicht.[17] Die Plasmahalbwertszeit liegt bei 1 bis 4 Stunden.[82] Bei Frühgeborenen kann sie auf Grund eines noch nicht voll entwickelten Stoffwechselsystems deutlich darüber liegen.[83]

Der Abbau von Paracetamol erfolgt vor allem in der Leber, wo der größte Teil des Stoffes im Rahmen einer Phase-II-Reaktion durch Verbindung mit Sulfat oder Glucuronsäure inaktiviert (Glucuronidierung) und dann über die Nieren ausgeschieden wird.
Die toxische Wirkung lässt sich auf ein in kleinen Mengen entstehendes Produkt zurückführen, das insbesondere über den Abbau über das Cytochrom-P450-Enzymsystem entsteht, das N-Acetyl-p-benzochinonimin. An der Bildung dieses sehr reaktionsfähigen Metaboliten ist insbesondere das Cytochrom-P450-Isoenzym CYP 2E1, ferner aber auch CYP 1A2 und CYP 3A4 beteiligt. Normalerweise wird N-Acetyl-p-benzochinonimin sofort über die Reaktion mit Glutathion (GSH) abgefangen und das entstandene Produkt über die Niere ausgeschieden. Glutathion steht jedoch nur in begrenztem Umfang in der Leber zur Verfügung und seine Nachbildung kann nicht genügend gesteigert werden. Daher erschöpft sich bei der akuten Überdosierung von Paracetamol der Glutathion-Anteil. Das N-Acetyl-p-benzochinonimin reagiert nun mit Struktur- und Funktionsproteinen der Leberzellen, was zur Leberzellnekrose und klinischem Leberversagen führen kann. Ein chronischer Alkoholkonsum und enzyminduzierende Arzneistoffe verstärken die Verstoffwechselung von Paracetamol über das Cytochrom-P450-Enzymsystem zu N-Acetyl-p-benzochinonimin und verstärken somit die Toxizität von Paracetamol.[55]
Ein alternativer Abbauweg des Paracetamols unter Beteiligung der Cytochrom-P450-Isoenzyme CYP 2A6 und CYP 2B1 führt zu 3-Hydroxyparacetamol. Dieser Metabolit, der nach Glucuronidierung ausgeschieden wird, zeigt eine deutlich niedrigere Toxizität als N-Acetyl-p-benzochinonimin.
Struktur
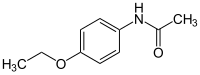
[Bearbeiten | Quelltext bearbeiten]Paracetamol ist ein Derivat des para-Aminophenols, also zugleich ein Phenol (N-Acetyl-p-aminophenol) und ein Derivat des Anilins (p-Hydroxyacetanilid). Daneben lässt sich Paracetamol auch als Acetamid, also als Amid der Essigsäure auffassen, woraus sich der nach IUPAC-Regularien vergebene Name N-(4-Hydroxyphenyl)acetamid ergibt.
Auf Grund der enthaltenen Anilinstruktur wird Paracetamol wie auch Acetanilid, Phenacetin und Propacetamol der Schmerzmittelgruppe der Anilinderivate zugerechnet. Acetanilid, Phenacetin und Propacetamol können dabei als Vorstufen (Prodrugs) angesehen werden, die im Organismus zu Paracetamol umgewandelt werden.

|

|
|

|
| Acetanilid | Paracetamol | Phenacetin | Propacetamol |

Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Paracetamol ist ein weißer, kristalliner Feststoff, der in mindestens zwei verschiedenen Modifikationen vorkommt. Diese Polymorphie ist von pharmazeutischer Bedeutung und hat Auswirkungen auf die Verpressbarkeit des Arzneistoffs. Orthorhombisches Paracetamol zeigt dabei eine der thermodynamisch stabileren monoklinen[84] Modifikation überlegene Verpressbarkeit.[85] Paracetamol ist in beiden Modifikationen in Alkoholen gut löslich, in kaltem Wasser dagegen nur mäßig (14 g/l bei 25 °C[7]), wohl aber in kochendem Wasser. Paracetamol hat eine Dichte von 1,293 Gramm pro Kubikzentimeter.[2] Es ist als Phenol schwach sauer. Der pH-Wert einer gesättigten, wässrigen Lösung liegt bei etwa sechs. Paracetamol hat einen charakteristischen, leicht bitteren Geschmack.[86]
Herstellung
[Bearbeiten | Quelltext bearbeiten]
Für die Herstellung von Paracetamol wurden verschiedene Synthesewege beschrieben. Das klassische Verfahren bedient sich der N-Acetylierung von p-Aminophenol.[87] Dieser Grundstoff ist herstellbar durch Nitrierung und nachfolgender Reduktion von Phenol oder alternativ ausgehend von Anilin oder p-Chlorphenol. Zur Acetylierung des Aminophenols lässt man es mit überschüssigem Essigsäureanhydrid reagieren, wobei unter Abspaltung von Essigsäure das Endprodukt wie auch N,O-diacetyliertes Nebenprodukt entsteht. Letzteres hydrolysiert im wässrigen Medium oder im schwach alkalisierten Milieu aufgrund der höheren Hydrolyseempfindlichkeit der Ester- gegenüber der Amidbindung selektiv zu Paracetamol.
Ein Verfahren der industriellen Großproduktion geht von Phenol aus und umfasst drei Schritte. Phenol wird mit Acetanhydrid in Gegenwart von Flusssäure in para-Stellung zu p-Hydroxyacetophenon acetyliert. Alternativ lässt sich p-Hydroxyacetophenon auch aus Phenylacetat bei niedriger Temperatur und mit Aluminiumchlorid als Lewis-Säure gewinnen (Fries-Umlagerung). Das p-Hydroxyacetophenon kondensiert man anschließend mit Hydroxylamin zum Oxim. Dieses lagert sich in Gegenwart von Thionylchlorid gemäß Beckmann zu Paracetamol um.[87]
Eine jüngere Variante ist die reduzierende Amidierung von p-Nitrophenol mit Thioessigsäure.[88]
Analytik
[Bearbeiten | Quelltext bearbeiten]
Nach dem Europäischen Arzneibuch kann Paracetamol mit Hilfe chemischer und instrumenteller analytischer Verfahren identifiziert werden. So kann Paracetamol durch Oxidation mit Kaliumdichromat unter Bildung eines blauen Farbstoffs nachgewiesen werden. Die Acetylgruppe lässt sich nach Hydrolyse mit Hilfe von Lanthannitrat und Iod nachweisen.[89] Alternativ dazu lässt sich Paracetamol nach Hydrolyse mit Hilfe von Formaldehyd durch eine positive Marquis-Reaktion nachweisen. Das Hydrolyseprodukt gibt auch einen positiven Nachweis auf primäre aromatische Amine. Die Phenolstruktur kann auch mit Eisen(III)-chlorid identifiziert werden, wobei sich ein blauer, säurelabiler Komplex bildet.
Die Gehaltsbestimmung von Paracetamol erfolgt nach dem Europäischen Arzneibuch nach hydrolytischer Spaltung des Paracetamols zu p-Aminophenol klassisch als oxidimetrische Titration mit Hilfe der Cerimetrie.[89] Alternative Gehaltsbestimmungsmethoden schließen instrumentelle Verfahren – wie HPLC – ein. Für die quantitative Bestimmung von Paracetamol im Urin, Blutplasma oder im Serum stehen neben HPLC- und Gaschromatographie-Verfahren[90][91] auch colorimetrische Assays und Immunassays zur Verfügung.
Angesichts der häufigen Verwendung kann Paracetamol neben Ibuprofen inzwischen auch in Flüssen nachgewiesen werden.[92]
Handelspräparate
[Bearbeiten | Quelltext bearbeiten]Wirtschaftsdaten, Abgaberegelung
[Bearbeiten | Quelltext bearbeiten]Paracetamol zählt weltweit zu den meistverkauften Arzneimitteln. Das Monopräparat Paracetamol-ratiopharm war mit über 20 Millionen Packungseinheiten im Jahr 2008 das in Deutschland am zweithäufigsten gekaufte Arzneimittel. Auch das Kombinationspräparat Thomapyrin (12,4 Millionen Packungseinheiten im Jahr 2008) findet sich in den Top 10 der meistgekauften Arzneimittel wieder.[93] Der jährliche Gesamtumsatz von Paracetamol in Deutschland wird auf etwa 31 Millionen Packungen mit einem Marktwert von etwa 60 Millionen Euro geschätzt.[94]
Paracetamol-Präparate für die orale Gabe zur Behandlung leichter bis mäßig starker Schmerzen und/oder von Fieber in einer Gesamtwirkstoffmenge von bis zu 10 g je Packung sowie für die rektale Anwendung unterliegen in Deutschland nicht der Verschreibungspflicht. Die Unterstellung oraler Mengen von mehr als 10 g unter die Verschreibungspflicht erfolgte im April 2009 mit dem Ziel, die Häufigkeit durch missbräuchliche Anwendung entstandener Paracetamolvergiftungen zu reduzieren.[95] Ähnliche Beschränkungen in Großbritannien führten zu einem geringfügigen Rückgang paracetamolbedingter Todesfälle.[57] Ein Antrag auf eine generelle Verschreibungspflicht für Paracetamol in Deutschland wurde 2012 abgelehnt.[96] In Deutschland ist Paracetamol ausschließlich in schnell freisetzenden Darreichungsformen zu haben – für Länder wie Belgien, Dänemark, Finnland, Luxemburg, Portugal, Rumänien und Schweden, in denen auch Retard-Varianten erhältlich sind,[97] bestätigte der Pharmakovigilanzausschuss der europäischen Arzneimittelagentur im Dezember 2017 seine Empfehlung, die Zulassung dieser Darreichungsformen ruhen zu lassen; die Koordinierungsgruppe des Zusammenschlusses der nationalen Zulassungsbehörden schloss sich dem an.[98]
Für paracetamolhaltige Infusionslösungen oder die Anwendung in der Tiermedizin benötigt man eine Verschreibung, ebenso für perorale Kombinationspräparate mit verschreibungspflichtigen Stoffen wie Codein, Metoclopramid und Tramadol.
Monopräparate
[Bearbeiten | Quelltext bearbeiten]Acetalgin (CH), ben-u-ron (D, A, CH), Captin (D), Contac (D), Contra-Schmerz P (CH)[99], Dafalgan (CH, BE, FR), Doliprane (F), Dolprone (CH), Enelfa Dr. Henk (D), GRIPPEX (D), Mexalen (A), Panadol (CH), Parapaed (D), Perfalgan (A, D, CH), RubieMol (A), Tachipirina (I), Tylenol (USA, CH) sowie zahlreiche Generika.
Kombinationspräparate
[Bearbeiten | Quelltext bearbeiten]- mit Acetylsalicylsäure: Fibrex (D), Thomapyrin 300 mg/200 mg (D, A)
- mit Butylscopolamin: Buscopan Plus (A,D)
- mit Coffein: Azur (D), COPYRKAL (D), Neopyrin (D), Octadon (D), Panadol Extra (CH), Prontopyrin (D), Vivimed (D)
- mit Codein: Contraneural (D), Gelonida (D), Nedolon (D), Optipyrin (D), Paracetamol comp. STADA (D), talvosilen (D), Titretta (D), Co–Dafalgan (CH)
- mit Diphenhydramin: Panadol PM (USA)
- mit Ibuprofen: Duoval (D), Synofen (D)
- mit Metoclopramid: Migraeflux MCP (D), Migräne-Neuridal (D), Migränerton (D), Migralave + MCP (D)
- mit Phenylephrin: Doregrippin (D)
- mit Tramadol: DOLEVAR (D), Zaldiar (CH, D)
- mit Ascorbinsäure (Vitamin C): Mexa-Vit C (A)
Mehrfachkombinationen:
- mit Acetylsalicylsäure und Coffein: Chephapyrin (D), dolomo (D), Dolopyrin (D), HA-Tabletten N (D), Melabon (D), Neuralgin (D), Novo Petrin (D), ratiopyrin (D), Thomapyrin CLASSIC (D), Thomapyrin INTENSIV (D), TITRALGAN (D), Thomapyrin (A), InfluASS (A), Irocophan (A)
- mit Ascorbinsäure, Coffein und Chlorphenamin: Grippostad (D)
- mit Coffein und Codein: Azur compositum (D)
- mit Acetylsalicylsäure und Ascorbinsäure: Grippal + C (D)
- mit Guaifenesin, Phenylephrin und Ascorbinsäure: WICK DayMed Erkältungs-Getränk für den Tag (D)
- mit Phenylpropanolamin und Dextromethorphan: Basoplex Erkältungs-Kapseln (D), WICK DayMed Erkältungs-Kapseln (D)
- mit Doxylamin, Ephedrin, Dextromethorphan: WICK MediNait Erkältungssirup (D)
- mit Doxylamin und Dextromethorphan: WICK MediNait Erkältungssirup mit Honig- und Kamillenaroma (D, CH)
- mit Phenylephrin und Dextromethorphan: Contac Erkältungs-Trunk Forte (D)
- mit Pheniramin, Phenylephrin, Ascorbinsäure: NeoCitran (A, CH)
Literatur
[Bearbeiten | Quelltext bearbeiten]- A. Bertolini, A. Ferrari, A. Ottani, S. Guerzoni, R. Tacchi, S. Leone: Paracetamol: new vistas of an old drug. In: CNS Drug Reviews. Band 12, Nr. 3–4, 2006, S. 250–275, doi:10.1111/j.1527-3458.2006.00250.x, PMID 17227290.
- Ernst Mutschler u. a.: Mutschler – Arzneimittelwirkungen Lehrbuch der Pharmakologie und Toxikologie. 9. Auflage. Wissenschaftl. Verlagsgesellschaft, Stuttgart 2008, ISBN 978-3-8047-1952-1.
- R. E. Brandlistuen, E. Ystrom, I. Nulman, G. Koren, H. Nordeng: Prenatal paracetamol exposure and child neurodevelopment: a sibling-controlled cohort study. In: International Journal of Epidemiology. Band 42, Nr. 6, 10. Januar 2014, S. 1702–1713, doi:10.1093/ije/dyt183.
- Kay Brune: Paracetamol: Eine Geschichte voller Fehleinschätzungen. In: Journal Club Schmerzmedizin. Band 4, Nr. 4, 1. Dezember 2015, S. 230–232, doi:10.1055/s-0041-106457.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Paracetamol-Präparate. Arzneimittel-Kompendium der Schweiz
- Superbrands: Panadol. (PDF; englisch)
- Eintrag zu Paracetamol bei Vetpharm, abgerufen am 28. März 2012.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu ACETAMINOPHEN in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2020.
- ↑ a b c d e f g Eintrag zu Paracetamol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2017. (JavaScript erforderlich)
- ↑ a b Eintrag zu Acetylaminophenole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 25. Dezember 2014.
- ↑ a b B. Hinz, O. Cheremina, K. Brune: Acetaminophen (paracetamol) is a selective cyclooxygenase-2 inhibitor in man. In: FASEB J. 2008 Feb;22(2) S. 383–390. PMID 17884974.
- ↑ R. Picciochi, H. P. Diogo, M. E. Minas da Piedade: Thermochemistry of paracetamol. In: J. Therm. Anal. Calorim. 100, 2010, S. 391–401. doi:10.1007/s10973-009-0634-y
- ↑ P. Di Martino, P. Conflant, M. Drache, J. P. Huvenne, A. M. Guyot-Hermann: Preparation and physical characterization of forms II and III of paracetamol. In: J. Therm. Anal. 48, 1997, S. 447–458.
- ↑ a b c d Eintrag zu Acetaminophen in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ Yumpu.com: SICHERHEITSDATENBLATT - Euro OTC Pharma Gmbh. Abgerufen am 11. Juli 2023.
- ↑ H. N. Morse: Ueber eine neue Darstellungsmethode der Acetylamidophenole. In: Berichte der deutschen chemischen Gesellschaft. Band 11, Nr. 1, 1878, S. 232–233, doi:10.1002/cber.18780110151 (bnf.fr [abgerufen am 3. Januar 2016]).
- ↑ J. Von Mering: Beiträge zur Kenntnis der Antipyretica. In: Ther. Monatsch. 7, 1893, S. 577–587.
- ↑ K. Brune: Paracetamol: gefährlicher als man denkt! 150 Jahre Anilinanalgetika Chemie in unserer Zeit 49(6), 2015, S. 402–409
- ↑ A Festival of Analgesics. Chemical Heritage Foundation, 2001.
- ↑ Über Bene. Abgerufen am 6. Januar 2016.
- ↑ U. S. Mantzke, A. M. Brambrink: Paracetamol im Kindesalter. Aktueller Wissensstand und Hinweise für einen rationalen Einsatz zur postoperativen Analgesie. In: Der Anaesthesist. Volume 51, Issue 9, September 2002, S. 735–746, doi:10.1007/s00101-002-0359-9.
- ↑ G. Dunea: Death over the counter. In: Br Med J. 1983, 286, S. 211–212. PMID 6401533; PMC 1546319 (freier Volltext).
- ↑ K. A. Wolnik, F. L. Fricke, E. Bonnin, C. M. Gaston, R. D. Satzger: The Tylenol tampering incident – tracing the source. In: Anal. Chem. 56, 1984, S. 466A–470A, 474A. PMID 6711821.
- ↑ a b c d e f g h i j k l Mustertext Nr. 8000443: Fachinformation Paracetamol. (PDF) Stand 1. Februar 2022; von der Website: BfArM – Muster- und Referenztexte. In: bfarm.de. 30. Oktober 2009, abgerufen am 29. November 2023.
- ↑ M. Craig, R. Jeavons, J. Probert, J. Benger: Randomised comparison of intravenous paracetamol and intravenous morphine for acute traumatic limb pain in the emergency department. In: Emergency Medicine Journal. Band 29, Nr. 1, 2012, S. 37–39. (doi:10.1136/emj.2010.104687).
- ↑ T. Luiz, G. Scherer und andere: Prähospitale Analgesie durch Rettungsassistenten in Rheinland-Pfalz. Praktikabilität, analgetische Wirkung und Sicherheit bei i.v.-verabreichtem Paracetamol. In: Der Anaesthesist. (doi:10.1007/s00101-015-0089-4).
- ↑ Fachinformation: Fixe Arzneistoffkombination Paracetamol 400 mg/Coffein 50 mg Tabletten Bundesinstitut für Arzneimittel und Medizinprodukte. Stand April 2012.
- ↑ H. C. Diener, V. Pfaffenrath, L. Pageler, H. Peil, B. Aicher: The fixed combination of acetylsalicylic acid, paracetamol and caffeine is more effective than single substances and dual combination for the treatment of headache: a multicentre, randomized, double-blind, single-dose, placebo-controlled parallel group study. In: Cephalalgia. Band 25, Nr. 10, Oktober 2005, S. 776–787, doi:10.1111/j.1468-2982.2005.00948.x, PMID 16162254.
- ↑ G. Geisslinger, S. Menzel, T. Gundermann, B. Hinz, P. Roth (Hrsg.): Mutschler Arzneimittelwirkungen. 11. Auflage. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2020, S. 272.
- ↑ S. Evers, A. May, G. Fritsche, P. Kropp, C. Lampl, V. Limmroth, V. Malzacher, S. Sandor, A. Straube, H. C. Diener: Akuttherapie und Prophylaxe der Migräne – Leitlinie der Deutschen Migräne- und Kopfschmerzgesellschaft und der Deutschen Gesellschaft für Neurologie. In: Nervenheilkunde. Band 27, Nr. 10, 2008, S. 933–949 (dmkg.de [PDF]).
- ↑ Deutsche Migräne- und Kopfschmerz-Gesellschaft: Spannungskopfschmerz selbst behandeln – Selbstmedikation für Patienten (PDF; 349 kB).
- ↑ Fachinformation: Fixe Arzneistoffkombination Paracetamol 500 mg/Codeinphosphat-Hemihydrat 30 mg Bundesinstitut für Arzneimittel und Medizinprodukte. Stand 5. September 2008.
- ↑ V. Persky, J. Piorkowski, E. Hernandez u. a.: Prenatal exposure to acetaminophen and respiratory symptoms in the first year of life. In: Ann Allergy Asthma Immunol. Band 101, Nr. 3, September 2008, S. 271–278, doi:10.1016/S1081-1206(10)60492-9, PMID 18814450, PMC 2578844 (freier Volltext).
- ↑ H. Allmers, C. Skudlik, S. M. John: Acetaminophen use: a risk for asthma? In: Curr Allergy Asthma Rep. Band 9, Nr. 2, März 2009, S. 164–167, PMID 19210907.
- ↑ H. Farquhar, A. Stewart, E. Mitchell u. a.: The role of paracetamol in the pathogenesis of asthma. In: Clin Exp Allergy. Band 40, Nr. 1, Januar 2010, S. 32–41, doi:10.1111/j.1365-2222.2009.03378.x, PMID 20205695.
- ↑ Bremer L.: Paracetamol Medication During Pregnancy: Insights on Intake Frequencies, Dosages and Effects on Hematopoietic Stem Cell Populations in Cord Blood From a Longitudinal Prospective Pregnancy Cohort; EBioMedicine, Oktober 2017
- ↑ R. E. Brandlistuen, E. Ystrom, I. Nulman, G. Koren, H. Nordeng: Prenatal paracetamol exposure and child neurodevelopment: a sibling-controlled cohort study. In: Int J Epidemiol. Band 42, S. 1702–1713, PMID 24163279.
- ↑ Paracetamol könnte Verhaltensprobleme bei Kindern auslösen. Nebenwirkungen von Paracetamol. In: Der Spiegel, Nr. 43/2016.
- ↑ C.-G. Bornehag et al.: Prenatal exposure to acetaminophen and children’s language development at 30 months. In: European Psychiatry. 1. Juni 2018, ehemals im (nicht mehr online verfügbar); abgerufen am 16. Juni 2019 (englisch). (Seite nicht mehr abrufbar. Suche in Webarchiven)
- ↑ Acetaminophen Use During Pregnancy Associated With Elevated Rate of Language Delay in Girls, Mount Sinai Researchers Find. Mount Sinai, 10. Januar 2018, abgerufen am 16. Juni 2019 (englisch, Press Release).
- ↑ S. Bancos, M. P. Bernard, D. J. Topham, R. P. Phipps: Ibuprofen and other widely used non-steroidal anti-inflammatory drugs inhibit antibody production in human cells. In: Cell Immunol. Band 258, Nr. 1, 2009, S. 18–28, PMID 19345936.
- ↑ V. A. Blaho u. a.: Cyclooxygenase-1 orchestrates germinal center formation and antibody class-switch via regulation of IL-17. In: J Immunol. Band 183, Nr. 9, 2009, S. 5644–5653, PMID 19843949.
- ↑ Roman Prymula u. a.: Effect of prophylactic paracetamol administration at time of vaccination on febrile reactions and antibody responses in children: two open-label, randomised controlled trials. In: The Lancet. Band 374, Nr. 9698, 2009, S. 1339–1350, PMID 19837254 (soniped.org [PDF]).
- ↑ Common Pain Relievers May Dilute Power of Flu Shots. University of Rochester Medical Center (URMC), abgerufen am 27. Juli 2011.
- ↑ Schmerzmittel schwächen Impfschutz. In: Spiegel online. Abgerufen am 4. Dezember 2009.
- ↑ M. P. Bernard, R. P. Phipp: Inhibition of cyclooxygenase-2 impairs the expression of essential plasma cell transcription factors and human B-lymphocyte differentiation. In: Immunology. Band 129, Nr. 1, 2010, S. 87–96, PMID 20050331.
- ↑ Over-the-Counter Pain Drugs May Affect Vaccine Strength. WXXI, archiviert vom (nicht mehr online verfügbar) am 11. Dezember 2013; abgerufen am 27. Juli 2011.
- ↑ Impfeffekt kann durch manche Medikamente deutlich abgeschwächt werden. Lungenärzte im Netz, abgerufen am 17. April 2019.
- ↑ Effect of Prophylactic Paracetamol Administration at Time of Vaccination on Febrile Reactions and Antibody Responses in Children F1000 Ranking: „Exceptional“ and Changes Clinical Practice. Medscape, abgerufen am 26. Juli 2011.
- ↑ A. R. Feinstein, L. A. Heinemann, G. C. Curhan u. a.: Relationship between nonphenacetin combined analgesics and nephropathy: a review. Ad Hoc Committee of the International Study Group on Analgesics and Nephropathy. In: Kidney Int. Band 58, Nr. 6, Dezember 2000, S. 2259–2264, doi:10.1046/j.1523-1755.2000.00410.x, PMID 11115060.
- ↑ R. Beasley: Association between paracetamol use in infancy and childhood, and risk of asthma, rhinoconjunctivitis, and eczema in children aged 6–7 years: analysis from Phase Three of the ISAAC programme. In: The Lancet. 372 (9643), 20. September 2008, S. 1039–1048. PMID 18805332.
- ↑ R. W. Beasley u. a.: Acetaminophen Use and Risk of Asthma, Rhinoconjunctivitis and Eczema in Adolescents: ISAAC Phase Three. In: Am. J. Respir. Crit. Care Med. 2010, doi:10.1164/rccm.201005-0757OC, PMID 20709817.
- ↑ A. J. Lowe, J. B. Carlin, C. M. Bennett, C. S. Hosking, K. J. Allen, C. F. Robertson, C. Axelrad, M. J. Abramson, D. J. Hill, S. C. Dharmage: Paracetamol use in early life and asthma: prospective birth cohort study. In: BMJ (Clinical research ed.). Band 341, 2010, S. c4616. PMID 20843914, PMC 2939956 (freier Volltext).
- ↑ G. Pickering, E. Schneider u. a.: Acetaminophen metabolism after major surgery: a greater challenge with increasing age. In: Clinical pharmacology and therapeutics. Band 90, Nummer 5, November 2011, S. 707–711, doi:10.1038/clpt.2011.176. PMID 21975347.
- ↑ Roland B. Walter, Filippo Milano, Theodore M. Brasky, Emily White: Long-Term Use of Acetaminophen, Aspirin, and Other Nonsteroidal Anti-Inflammatory Drugs and Risk of Hematologic Malignancies: Results From the Prospective Vitamins and Lifestyle (VITAL) Study. In: Journal of Clinical Oncology. 2011, doi:10.1200/JCO.2011.34.6346.
- ↑ FDA Warns of Rare Acetaminophen Risk. In: fda.gov. 1. August 2013, archiviert vom (nicht mehr online verfügbar) am 22. Juli 2017; abgerufen am 23. Januar 2024 (englisch).
- ↑ PRAC recommends modified-release paracetamol be removed from market. EMA, Summary, 1. September 2017; abgerufen am 6. September 2017.
- ↑ Dominik Mischkowski, Jennifer Crocker, Baldwin M. Way: From Painkiller to Empathy Killer: Acetaminophen (Paracetamol) Reduces Empathy for Pain. In: Social Cognitive and Affective Neuroscience. 2016, S. nsw057, doi:10.1093/scan/nsw057 (oxfordjournals.org [abgerufen am 21. Mai 2016]).
- ↑ Alexis Keaveney, Ellen Peters, Baldwin Way: Effects of acetaminophen on risk taking. In: Social Cognitive and Affective Neuroscience. Band 15, Nr. 7, Juli 2020, S. 725–732, doi:10.1093/scan/nsaa108.
- ↑ Iain M. MacIntyre, Emma J. Turtle, Tariq E. Farrah, Catriona Graham, James W. Dear: Regular Acetaminophen Use and Blood Pressure in People With Hypertension: The PATH-BP Trial. In: Circulation. Band 145, Nr. 6, 8. Februar 2022, S. 416–423, doi:10.1161/CIRCULATIONAHA.121.056015, PMID 35130054, PMC 7612370 (freier Volltext).
- ↑ a b A. M. Larson u. a.: Acetaminophen-induced acute liver failure: results of a United States multicenter, prospective study. In: Hepatology. Band 42, Nr. 6, 2005, S. 1364–1372, PMID 16317692.
- ↑ a b c L. Jackson Roberts, Jason D. Morrow: Goodman & Gilman’s the pharmacological basis of therapeutics. Hrsg.: Alfred Gilman, Louis Sanford Goodman, Joel G. Hardman, Lee E. Limbird. McGraw-Hill, New York 2001, ISBN 0-07-112432-2, Analgesic-antipyretic and antiinflammatory agents and drugs employed in the treatment of gout, S. 687–732.
- ↑ Williams, Roger Lawrence; Jean-Pierre Benhamou; Lee, William Thomas: Acute liver failure. Cambridge University Press, Cambridge, UK 1997, ISBN 0-521-55381-4.
- ↑ a b O. W. Morgan, C. Griffiths, A. Majeed: Interrupted time-series analysis of regulations to reduce paracetamol (acetaminophen) poisoning. In: PLoS Med. Band 4, Nr. 4, April 2007, S. e105, doi:10.1371/journal.pmed.0040105, PMID 17407385, PMC 1845154 (freier Volltext).
- ↑ K. Hawton, H. Bergen, S. Simkin, S. Dodd, P. Pocock, W. Bernal, D. Gunnell, N. Kapur: Long term effect of reduced pack sizes of paracetamol on poisoning deaths and liver transplant activity in England and Wales: interrupted time series analyses. In: BMJ. 346, 2013. doi:10.1136/bmj.f403
- ↑ a b c L. J. Chun u. a.: Acetaminophen hepatotoxicity and acute liver failure. In: J Clin Gastroenterol. Band 43, Nr. 4, 2009, S. 342–349, PMID 19169150.
- ↑ Pressemitteilung der FDA verfügbar als html, zuletzt abgerufen am 14. Januar 2011.
- ↑ J. Granese, K. Brightbill, P. Osborne, C. E. Cox, L. W. Gaber: Analgesic nephropathy selectively affecting a unilateral non-functioning hypoplastic kidney. In: Clin. Nephrol. Band 68, Nr. 2, August 2007, S. 115–120, PMID 17722712.
- ↑ H. Kupferschmidt: Therapie der Paracetamolvergiftung Schweizerisches Toxikologisches Informationszentrum (PDF; 72 kB)
- ↑ Julia Nakagawa u. a.: Nebenwirkungen durch nicht zugelassene nichtsteroidale Entzündungshemmer (NSAID) bei 21 Hunden. In: Kleintierpraxis. 55, 2010, S. 364–370.
- ↑ Wolfgang Löscher, Fritz Rupert Ungemach: Pharmakotherapie bei Haus- und Nutztieren. 7. Auflage. Paul Parey, 2006, ISBN 3-8304-4160-6, S. 106–107.
- ↑ Stille Killer im Dienst des Umweltschutzes. US Army setzt mit Paracetamol vergiftete Schlangenköder ein.
- ↑ Zaria Gorvett: The US island ruled by alien snakes and spiders. In: BBC News. 31. Oktober 2024, abgerufen am 3. November 2024 (englisch).
- ↑ J. H. Friday und andere: Ibuprofen provides analgesie equivalent to acetaminophen-codeine in the treatmeant of acute pain in children with extremity injuries: a randomized clinical trial. In: Acad Emerg Med. Band 16, Nr. 8, 2009, S. 711–716 (doi:10.111/j.1553-2712.2009.00471.x).
- ↑ R. J. Flower, J. R. Vane: Inhibition of prostaglandin synthetase in brain explains the anti-pyretic activity of paracetamol (4-acetamidophenol). In: Nature. Band 240, Nr. 5381, Dezember 1972, S. 410–411, PMID 4564318.
- ↑ Olivier Boutaud, David M. Aronoff, Jacob H. Richardson, Lawrence J. Marnett, John A. Oates: Determinants of the cellular specificity of acetaminophen as an inhibitor of prostaglandin H2 synthases, In: Proc. Natl. Acad. Sci. USA. 2002, 99, S. 7130–7135. PMID 12011469; PMC 124540 (freier Volltext).
- ↑ K. Brune, K. D. Rainsford, A. Schweitzer: Biodistribution of mild analgesics. In: British Journal of Clinical Pharmacology. 10 Suppl 2, Oktober 1980, S. 279S–284S, PMID 6969084, PMC 1430188 (freier Volltext).
- ↑ N. V. Chandrasekharan, H. Dai, K. L. Roos u. a.: COX-3, a cyclooxygenase-1 variant inhibited by acetaminophen and other analgesic/antipyretic drugs: cloning, structure, and expression. In: Proc. Natl. Acad. Sci. U.S.A. Band 99, Nr. 21, Oktober 2002, S. 13926–13931, doi:10.1073/pnas.162468699, PMID 12242329, PMC 129799 (freier Volltext).
- ↑ Bela Kis, James A. Snipes, David W. Busija: Acetaminophen and the Cyclooxygenase-3 Puzzle: Sorting out Facts, Fictions, and Uncertainties. In: Journal of Pharmacology and Experimental Therapeutics. Band 315, Nr. 1, 19. September 2005, S. 1–7, doi:10.1124/jpet.105.085431.
- ↑ C. Frölich: Selektive Cyclooxygenasehemmer: Eine neue Generation von Antirheumatika. In: Deutsches Ärzteblatt. 93 (47), 1996, S. A-3100 / B-2632 / C-2438 Medizinreport.
- ↑ G. Pickering, V. Estève, M. A. Loriot, A. Eschalier, C. Dubray: Acetaminophen reinforces descending inhibitory pain pathways. In: Clin. Pharmacol. Ther. Band 84, Nr. 1, Juli 2008, S. 47–51, doi:10.1038/sj.clpt.6100403, PMID 17957182.
- ↑ a b B. J. Anderson: Paracetamol (Acetaminophen): mechanisms of action. In: Paediatr Anaesth. Band 18, Nr. 10, Oktober 2008, S. 915–921, doi:10.1111/j.1460-9592.2008.02764.x, PMID 18811827.
- ↑ Mechanism of action of paracetamol. PMID 15662292
- ↑ a b Alfio Bertolini, Anna Ferrari, Alessandra Ottani, Simona Guerzoni, Raffaella Tacchi, Sheila Leone: Paracetamol: New vistas of an old drug. In: CNS Drug Reviews. 12, 2006, S. 250–275. PMID 17227290; doi:10.1111/j.1527-3458.2006.00250.x.
- ↑ E. D. Högestätt, B. A. Jönsson, A. Ermund, D. A. Andersson, H. Björk, J. P. Alexander, B. F. Cravatt, A. I. Basbaum, P. M. Zygmunt: Conversion of acetaminophen to the bioactive N-acylphenolamine AM404 via fatty acid amide hydrolase-dependent arachidonic acid conjugation in the nervous system, In: J. Biol. Chem. 280 (36), 2005, S. 31405–31412. PMID 15987694.
- ↑ C. N. Dewall, G. Macdonald, G. D. Webster, C. L. Masten, R. F. Baumeister, C. Powell, D. Combs, D. R. Schurtz, T. F. Stillman, D. M. Tice, N. I. Eisenberger: Acetaminophen reduces social pain: behavioral and neural evidence. In: Psychol Sci. Band 21, Nr. 7, 2010, S. 931–937, PMID 20548058.
- ↑ C. N. Dewall: Hurt feelings? You could take a pain reliever... In: Harv Bus Rev. Band 89, Nr. 4, 2011, S. 28–29, PMID 21510517.
- ↑ D. Häske und andere: Analgesie bei Traumapatienten in der Notfallmedizin. In: Der Anaesthesist, Band 69, Nr. 2, Februar 2020, S. 137–148, hier: S. 140 f.
- ↑ Rote Liste 2009. Rote Liste Service. ISBN 3-939192-30-9.
- ↑ R. A. van Lingen, J. T. Deinum, J. M. Quak u. a.: Pharmacokinetics and metabolism of rectally administered paracetamol in preterm neonates. In: Arch. Dis. Child. Fetal Neonatal Ed. Band 80, Nr. 1, Januar 1999, S. F59–F63, PMID 10325815, PMC 1720876 (freier Volltext).
- ↑ Charge density and electrostatic potential analyses in paracetamol. In: Acta Cryst. B65, 2009, S. 363–374.
- ↑ Stephen P. F. Miller, Andre S. Raw, Lawrence X. Yu: Polymorphism: in the Pharmaceutical Industry. Hrsg.: Rolf Hilfiker. John Wiley & Sons, Chichester 2006, ISBN 3-527-31146-7, Scientific considerations of pharmaceutical solid polymorphism in regulatory applications, S. 385–404.
- ↑ Lewis, R.J. Sr.; Hawley's Condensed Chemical Dictionary, 15. Ausgabe. John Wiley & Sons, Inc. New York, NY 2007., S. 11.
- ↑ a b Thomas Christoph, Helmut Buschmann: Analgesics: From Chemistry and Pharmacology to Clinical Application. Hrsg.: Bernd Sundermann, Helmut Buschmann, Thomas Christoph, Elmar Friderichs, Corinna Maul. Wiley-VCH, Weinheim 2002, ISBN 3-527-30403-7, Cyclogenase inhibition: From NSAIDs to selective COX-2 inhibitors, S. 13–126.
- ↑ A. Bhattacharya u. a.: Eco-friendly reductive acetamidation of arylnitro compounds by thioacetate anion through in situ catalytic regeneration: application in the synthesis of Acetaminophen. In: Tetrahedron Letters. Band 47, Nr. 19, 2006, S. 3221–3223, doi:10.1016/j.tetlet.2006.03.057.
- ↑ a b Europäisches Arzneibuch. 6. Ausgabe. Grundwerk 2008. Monographie Paracetamol. Deutscher Apotheker Verlag, Stuttgart, ISBN 978-3-7692-3962-1.
- ↑ J Lee, J Park, A Go, H Moon, S Kim, S Jung, W Jeong, H Chung: Urine Multi-drug Screening with GC-MS or LC-MS-MS Using SALLE-hybrid PPT/SPE. In: J Anal Toxicol., 1. November 2018, 42(9), S. 617–624, PMID 29762685
- ↑ W Lu, S Zhao, M Gong, L Sun, L Ding: Simultaneous determination of acetaminophen and oxycodone in human plasma by LC-MS/MS and its application to a pharmacokinetic study. In: J Pharm Anal. Juni 2018, 8(3), S. 160–167, PMID 29922484
- ↑ J Borrull, A Colom, J Fabregas, E Pocurull, F Borrull: A simple, fast method for the analysis of 20 contaminants of emerging concern in river water using large-volume direct injection liquid chromatography-tandem mass spectrometry. In: Anal Bioanal Chem., 2019 Mar, 411(8), S. 1601–1610, PMID 30680425
- ↑ G. Glaeske, C. Schicktanz, K. Janhsen: GEK-Arzneimittelreport 2009. Asgard Verlag, 2009, ISBN 978-3-537-44068-6.
- ↑ Ibuprofen dreimal so oft wie ASS In: Apotheke Adhoc, 28. September 2014.
- ↑ Schmerzmittel mit Paracetamol ab April teilweise rezeptpflichtig. ( vom 2. Januar 2016 im Internet Archive) ABDA, Pressemitteilung, 10. März 2009.
- ↑ Paracetamol bleibt OTC-Produkt. In: Apotheke Adhoc. 27. Juni 2012, archiviert vom (nicht mehr online verfügbar) am 23. September 2015; abgerufen am 10. November 2014.
- ↑ Julia Borsch: EMA empfiehlt Aus für retardiertes Paracetamol. In: DAZ.online. 4. September 2017 (deutsche-apotheker-zeitung.de [abgerufen am 4. September 2017]).
- ↑ Paracetamolhaltige Arzneimittel mit modifizierter Freisetzung: Maßnahmen zur Risikominimierung und Schadensreduktion bei Überdosierung. BfArM, 15. Dezember 2017.
- ↑ Contra-Schmerz® P. In: compendium.ch. 23. April 2018, archiviert vom (nicht mehr online verfügbar) am 3. September 2014; abgerufen am 27. Juli 2018.