Benutzer:Holger87/Spielwiese/geminal
In der Chemie spricht man von geminal (von lat. gemini „Zwillinge“), wenn zwei gleiche funktionelle Gruppen (z. B. Halogene wie Fluor, Chlor oder Brom) an dasselbe Kohlenstoff-Atom innerhalb einer Kette oder eines Ringsystems gebunden sind.[1] Abweichende Definitionen schließen unterschiedliche Substituenten nicht aus, wobei auch hier darauf hingewiesen wird, dass es sich in der Regel um gleichartige Substituenten handelt.[2]
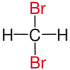
| Vergleich von geminalen mit vicinalen und isolierten Substitutionsmustern. | ||||
| Alkan | geminal | vicinal | isoliert | |
| Methan | 
|
|
existiert nicht | existiert nicht |
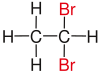
| Ethan | 
|
|

|
existiert nicht |
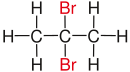
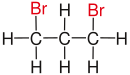
| Propan | 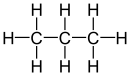
|
|

|
|
| Rot markierte Substituenten an ausgewählten Dibromalkanen. | ||||
Weitere, die relative Anordnung zweier funktioneller Gruppen beschreibende Begriffe sind vicinal, isoliert sowie α- und β-ständig.
1H-NMR-Spektroskopie
[Bearbeiten | Quelltext bearbeiten]In der 1H-NMR-Spektroskopie wird die Kopplung zweier Wasserstoffatome, die sich am selben Kohlenstoffatom befinden, als geminale Kopplung bezeichnet. Sie tritt nur auf, wenn sich zwei Wasserstoffatome an einer Methylengruppe stereochemisch voneinander unterscheiden. Die geminale Kopplungskonstante wird als 2J bezeichnet, da die Wasserstoffatome über zwei Bindungen hinweg miteinander koppeln. In Abhängigkeit von den anderen Substituenten nimmt die geminale Kopplungskonstante Werte zwischen −23 und +42 Hz ein.[3][4]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, S. 462.
- ↑ Thieme Römpp-Online, Georg Thieme Verlag, Stuttgart KG 2012, Suchbegriff „geminal“.
- ↑ H. Günther: NMR-Spektroskopie; Grundlagen,Konzepte und Anwendungen der Protonen- und Kohlenstoff-13-Kernresonanzspektroskopie in der Chemie, 3. neubearbeitete und erweiterte Auflage, Georg Thieme Verlag, Stuttgart 1992, S. 103.
- ↑ D. H. Williams, I. Fleming: Strukturaufklärung in der organischen Chemie; Eine Einführung in die spektroskopischen Methoden, 6. überarbeitete Auflage, Georg Thieme Verlag, Stuttgart 1991, S. 109.
[[Kategorie:Chemische Bindung]]