Prednisolon
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
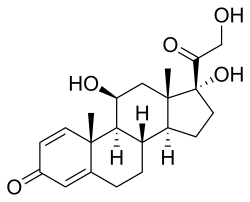
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Prednisolon | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C21H28O5 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
A07EA01, C05AA04, D07AA03, D07XA02, H02AB06, R01AD02, S01BA04, S01CB02, S02BA03, S03BA02 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 360,44 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
löslich in Ethanol, sehr schlecht in Wasser (223 mg·l−1 bei 25 °C)[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Prednisolon ist ein synthetisches Glucocorticoid. Seine Struktur ähnelt stark dem körpereigenen Steroidhormon der Nebennierenrinde, dem Cortisol, indem eine weitere C=C-Doppelbindung in den A-Ring eingefügt wurde. Die chemische Verbindung wird daher auch 1,2-Dehydrocortisol genannt. Frühere Bezeichnungen waren Metacortandralon oder Deltahydrocortison. Neben den beiden C=C-Doppelbindungen enthält das Molekül zwei Carbonylgruppen und drei Hydroxygruppen, ist also ein Hydroxyketon (11β,17α,21-Trihydroxy-1,4-pregnadien-3,20-dion).
Geschichte
[Bearbeiten | Quelltext bearbeiten]Das Hydroxyketon wurde von Wissenschaftlern der Chemical Research and Development Division der Schering Corporation in den USA (späterer Firmenname Schering-Plough) durch Reduktion von Prednison gewonnen, zunächst durch Reduktion des Bis-3,20-Semicarbazons mit Kaliumborhydrid, dann durch eine enzymatisch-mikrobiologische Reaktion.[4][5][6] Der Mikrobiologe Arthur Nobile verwendete dafür Kulturen von Corynebacterium simplex und anderen Mikroorganismen, was für die industrielle Produktion entscheidend war.[7]

Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Prednisolon ist eine feste kristalline Substanz, die in zwei polymorphen Formen und einer Hydratform auftritt.[1] Das kommerzielle Produkt schmilzt bei 239 °C mit einer Schmelzenthalpie von 33,1 kJ·mol−1.[1] Das zweite Polymorph zeigt einen Schmelzpunkt bei 243 °C mit einer Schmelzenthalpie von 23,7 kJ·mol−1.[1] Beide Kristallformen stehen somit enantiotrop zueinander, wobei das tiefer schmelzende Polymorph die bei Raumtemperatur thermodynamisch stabilere Form darstellt. Die Hydratform besitzt eine 1,5-Stöchiometrie und kann aus Methanol-Wasser-Gemischen kristallisiert werden.[1] Die Hydratwasserabgabe erfolgt bereits ab 30 °C unter Bildung der höher schmelzenden Kristallform.[1] Alle drei Kristallformen zeigen eine unterschiedliche Löslichkeit.[8]
Wirkung
[Bearbeiten | Quelltext bearbeiten]Prednisolon besitzt eine ausgeprägte immunsuppressive und darüber entzündungshemmende, antiallergische Wirkung. Es ist ein aktiver Metabolit des Prednisons. Die Substanz galt als Wirkstoff der Wahl für systemische antiinflammatorische und immunsuppressive Effekte.[9] Prednisolon kann sich in die Membran von Zellen einlagern und diese so stabilisieren, was eine geringere Beweglichkeit von Immunzellen zur Folge hat.
Anwendungsgebiete
[Bearbeiten | Quelltext bearbeiten]Seit 1957 wird Prednisolon als „Solu-Decortin H“ von Merck in Deutschland vermarktet.[10] Der Wirkstoff wird sowohl in freier Form als auch als Prednisolonacetat überall dort eingesetzt, wo es gilt, akute Entzündungsreaktionen zu unterdrücken. Dazu gehören unter anderem: Schock/anaphylaktischer Schock, schwere Verlaufsformen allergischer Reaktionen, beispielsweise nach Wespenstich, Hirnödem, Meningitis, nach neurochirurgischen Operationen, Transplantationen (bei Gefahr der Organabstoßung), Inhalation toxischer Substanzen wie z. B. Chlorgas, Pseudokrupp, schweren Infektionskrankheiten oder bei akuten Verschlechterungen der chronisch obstruktiven Lungenerkrankung (COPD) und bei schwerem Asthma Stufe 4, bei rheumatoiden Erkrankungen, entzündlichen Augenerkrankungen, chronisch-entzündlichen Darmerkrankungen, Multipler Sklerose und Autoimmunerkrankungen, Hautkrankheiten (insbesondere Neurodermitis).
Bei durch Immunkrankheiten ausgelösten Herzbeutelentzündungen können Wirkstoffe auf der Basis von Glucocorticoiden verabreicht werden.
Ein weiteres Anwendungsgebiet von Prednisolon ist die vorbeugende Behandlung bei Cluster-Kopfschmerz.[11]
Nebenwirkungen
[Bearbeiten | Quelltext bearbeiten]Prednisolon hat zahlreiche Nebenwirkungen, die auch gefährlich sein können (siehe hierzu auch Glucocorticoide#Nebenwirkungen). So resultiert aus der immunsuppressiven Wirkung eine erhöhte Infektanfälligkeit des betroffenen Patienten. Bei längerer Einnahme führt ein kataboler Effekt zu Schäden am Knochenbau (Osteopenie bzw. Osteoporose) und einem iatrogenen (durch ärztliche Therapie verursachten) Cushing-Syndrom. Es kann auch zur Entstehung eines Diabetes mellitus kommen.
Bei Beendigung einer länger dauernden Therapie mit Prednisolon oder anderen Steroiden kann es erforderlich sein, die tägliche Dosis langsam zu reduzieren, was als „Ausschleichen“ bezeichnet wird. Erfolgt dies nicht, kann es zum akuten Steroid-Entzugssyndrom kommen, welches einer Nebennierenrindeninsuffizienz ähnlich ist. Blutspiegelbestimmungen des spontanen morgendlichen Kortisolwerts (der über 500 nmol/l betragen sollte) sofort nach Ende der Prednisolontherapie können helfen, das zu vermeiden.[12]
Äquivalenzdosen
[Bearbeiten | Quelltext bearbeiten]Die relative entzündungshemmende Äquivalenzdosis anderer Präparate, welche beachtet werden muss, wenn Prednisolon die Einnahme eines anderen Glukokortikoids ersetzen soll, lässt sich aus der folgenden Gleichung ablesen:
5 mg Prednisolon = 5 mg Prednison = 0,7 mg Dexamethason = 4 mg Triamcinolon = 4 mg Methylprednisolon = 20 mg Hydrocortison = 25 mg Cortison.
Handelsnamen
[Bearbeiten | Quelltext bearbeiten]- Monopräparate: Aprednislon (A), Decortin H (D), Dermosolon (D), Dontisolon (D), Hefasolon (D), Hexacorton (CH), Infectocortikrupp (D), Inflanefran (D), Klismacort (D), Kuehlprednon (A), Linola H (D), Lygal Tinktur (D), Prednisolon (D), Prednisolut (D), Premandol (CH), Solu-Decortin H (D), Solu-Dacortin (A), Spiricort (CH), Ultracortenol (D, A, CH), Prednison 5 léčiva (CZ, SK), zahlreiche Generika (D, A, CH)
- Kombinationspräparate: Alpicort (D, A, CH), Aquapred (D), Bismolan-H Corti (D), Blephamide (D, CH), Imacort (CH), Imazol comp (D), Inflanegent (D), Leioderm P (D), Linoladiol H (D), Locaseptil (CH), Mycinopred (CH), Oxytetracyclin-Prednisolon (D), Scheriproct (A, CH)
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Maria D. Veiga, Rafael Cadorniga: Thermal Study of Prednisolone Polymorphs, in: Thermochim. Acta, 1985, 96, S. 111–115, doi:10.1016/0040-6031(85)80012-5.
- ↑ a b Eintrag zu Prednisolone in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ a b Datenblatt Prednisolone bei Sigma-Aldrich, abgerufen am 22. April 2011 (PDF).
- ↑ Hershel L. Herzog, Constance C. Payne, Margaret A. Jevnik, David Gould, Elliot L. Shapiro, Eugene P. Oliveto, E. B. Hershberg: 11-Oxygenated Steroids. XIII. Synthesis and Proof of Structure of △1,4-Pregnadiene-17α,21-diol-3,11,20-trione and △1,4-Pregnadiene-11β,17α,21-triol-3,20-dione, In: Journal of the American Chemical Society Jg. 1955 Bd. 77, Heft 18, S. 4781–4784 DOI:10.1021/ja01623a027
- ↑ Arthur Nobile, William Charney, Preston L. Perlman, Hershel L. Herzog, Constance C. Payne, Maryann E. Tully, Margaret A. Jevnik, Emanuel B. Hershberg: Microbiological Transformation of Steroids. I. Δ1,4-Diene-3-ketosteroids. In: Journal of the American Chemical Society, Jg. 1955, Bd. 77, S. 4184–4184.
- ↑ Arthur Nobile, US-Patente 2837464 und 3134718 (1958 und 1964).
- ↑ Arthur Nobile, US-Patente 2837464 und 3134718 (1958 und 1964).
- ↑ Maria D. Veiga, Rafael Cadorniga: Estudio de coeficientes de solubilidad y velocidad de disolucion de diversos polimorfos de la prednisolona. in: Cien. Ind. Farm., 1988, 7, S. 201–205.
- ↑ Pharmacology/H. P. Rang et al. – Churchill Livingstone, Edinburgh 2003, S. 412.
- ↑ Horst Finger: Der Einfluß von Avil und Solu-Decortin H auf die experimentelle „allergische“ Encephalomyelitis des Meerschweinchens und Kaninchens. Research in Experimental Medicine, Springer, Berlin/Heidelberg 1961, 135 (3), S. 276–280, doi:10.1007/BF02045076.
- ↑ S1-Leitlinie Clusterkopfschmerz und trigeminoautonome Kopfschmerzen der Deutschen Gesellschaft für Neurologie (DGN). In: AWMF online (Stand 2015).
- ↑ B. Kreutzkamp, in Medical Tribune 49, 11. Juli 2014, S. 4.