Brom(I)-fluorosulfonat
(Weitergeleitet von Bromfluorosulfat)
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
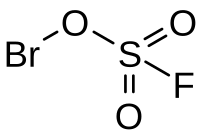
| |||||||
| Allgemeines | |||||||
| Name | Brom(I)-fluorosulfonat | ||||||
| Andere Namen |
| ||||||
| Summenformel | BrSO3F | ||||||
| Kurzbeschreibung |
schwarzrote Flüssigkeit[1] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 178,97 g·mol−1 | ||||||
| Aggregatzustand |
flüssig | ||||||
| Dichte |
2,60 g·cm−3 (25 °C)[2] | ||||||
| Siedepunkt |
120,5 °C[1] | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||
Brom(I)-fluorosulfonat, BrSO3F ist die einwertige chemische Verbindung des Broms aus der Gruppe der Fluorosulfonaten.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Analog zu den anderen Halogenfluorosulfonaten lässt die Reaktion von Brom mit Peroxydisulfuryldifluorid lässt die Verbindung entstehen.[1][4]
Die Reduktion von Brom(III)-fluorosulfonat lässt auch Brom(I)-fluorosulfonat gewinnen.[5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Brom(I)-fluorosulfonat ist eine schwarzrote, viskose, hydrolyseempfindliche Flüssigkeit, die mit Wasser sehr heftig reagiert. Beim Abkühlen erstarrt sie glasig.[4]
Brom(I)-fluorosulfonat reagiert ab 50 °C mit Iod(I)-fluorosulfonat zu Dibromoiodfluorosulfonat.[6]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c F. Albert Cotton (Hrsg.): Progress in Inorganic Chemistry. Band 14. John Wiley & Sons, 2009, ISBN 0-470-16658-4, S. 65.
- ↑ J.H. Simons: Fluorine Chemistry. Band 5. Elsevier, 2012, ISBN 0-323-14724-0, S. 70.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 339.
- ↑ John E. Roberts, George H. Cady: Halogen Fluorosulfonates BrSO3F, Br(SO3F)3 and I(SO3F)3. J. Am. Chem. Soc., Januar 1960, S. 352–353, doi:10.1021/ja01487a023.
- ↑ Kurt Niedenzu, Hans Zimmer: Annual Reports in Inorganic and General Syntheses. Academic Press, 2013, ISBN 1-4832-1388-9, S. 109.


