Dysprosium(III)-chlorid
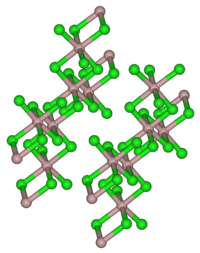
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| _ Dy3+ _ Cl− | ||||||||||
| Raumgruppe |
C2/m (Nr. 12) | |||||||||
| Allgemeines | ||||||||||
| Name | Dysprosium(III)-chlorid | |||||||||
| Andere Namen |
Dysprosiumtrichlorid | |||||||||
| Verhältnisformel | DyCl3 | |||||||||
| Kurzbeschreibung | ||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 268,86 g·mol−1 | |||||||||
| Aggregatzustand |
fest[3] | |||||||||
| Dichte |
3,67 g·cm−3 (25 °C)[3] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
1530 °C[1] | |||||||||
| Löslichkeit |
löslich in Wasser[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Toxikologische Daten | ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Dysprosium(III)-chlorid ist eine chemische Verbindung aus der Gruppe der Chloride.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Dysprosium(III)-chlorid kann direkt aus den Elementen Dysprosium und Chlor synthetisiert werden.[4]
Das Hexahydrat kann durch Reaktion von Dysprosium(III)-oxid, Dysprosium oder Dysprosium(III)-carbonat mit Salzsäure gewonnen werden.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
Dysprosium(III)-chlorid liegt als gelblichweiße perlmuttartige glänzende Schuppen vor. Es besitzt eine monokline Kristallstruktur mit der Raumgruppe C2/m (Raumgruppen-Nr. 12)[1] entsprechend der von Aluminium(III)-chlorid mit den Gitterparametern a = 691 pm, b = 1197 pm, c = 640 pm, β = 111,28° und Z = 2.[5] Das Hexahydrat ist ein hellgelber Feststoff.[2]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Dysprosium(III)-chlorid kann als Katalysator in organischen Synthesen verwendet werden.[6]
Literatur
[Bearbeiten | Quelltext bearbeiten]- Tomasz Mioduskia, Cezary Gumińskib, Dewen Zengc: IUPAC-NIST Solubility Data Series. 87. Rare Earth Metal Chlorides in Water and Aqueous Systems. Part 3. Heavy Lanthanides (Gd–Lu). In: Journal of Physical and Chemical Reference Data. Band 38, Nr. 4, 2009, S. 925–1011, doi:10.1063/1.3212962.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e Jean D’Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 2007, ISBN 978-3-540-60035-0, S. 442 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c Datenblatt Dysprosium(III) chloride hexahydrate, 99.9 % trace metals basis bei Sigma-Aldrich, abgerufen am 29. April 2012 (PDF).
- ↑ a b c d e f Datenblatt Dysprosium(III) chloride, anhydrous, powder, 99.99 % trace metals basis bei Sigma-Aldrich, abgerufen am 29. April 2012 (PDF).
- ↑ Webelements: Dysprosium
- ↑ S. Cahen, R. Vangelisti: Synthesis, structure and magnetic properties of lanthanide trichlorides‐GIC: Stage-2 DyCl3–GIC. In: Journal of Physics and Chemistry of Solids. 67, Nr. 5–6, 2006, S. 1223–1227, doi:10.1016/j.jpcs.2006.01.094.
- ↑ Gesine K. Veits, Javier Read de Alaniz: Dysprosium(III) catalysis in organic synthesis. In: Tetrahedron. 68, Nr. 8, 2012, S. 2015–2026, doi:10.1016/j.tet.2011.11.042.




