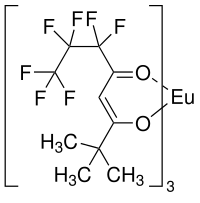
Eu(fod)3
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Eu(fod)3 | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C30H30EuF21O6 | ||||||||||||||||||
| Kurzbeschreibung |
hellgelber Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 1037,49 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
203–207 °C[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Eu(fod)3 (EuFOD) ist eine chemische Verbindung mit der Summenformel Eu(OCC(CH3)3CHCOC3F7)3. Diese Koordinationsverbindung wird primär in der NMR-Spektroskopie eingesetzt, um Signale zu verschieben (shiften). Es ist eines der bekanntesten Lanthanoid-Shift-Reagenzien und war vor allem in den 1970er- und 1980er-Jahren populär. Es wurde 1971 erstmals von Rondeau und Sievers verwendet und war das erste fluorierte Shift-Reagenzien.[2]
Struktur und Reaktivität
[Bearbeiten | Quelltext bearbeiten]Eu(fod)3 besteht aus drei zweizähnigen fod-Liganden, die an ein Eu(III)-Zentrum binden. Das 1,1,1,2,2,3,3-Heptafluor-7,7-dimethyl-4,6-octandionat (fod) leitet sich vom Acetylacetonat ab. Es trägt, wie das strukturell verwandte Eu(dmp)3, eine tert-Butyl-Gruppe und einen perfluorierten Propyl-Rest. Das Metallatom hat die Elektronenkonfiguration f6. Die sechs Elektronen sind ungepaart – jedes befindet sich in einem anderen einfach-besetzten f-Orbital – woraus ein ausgeprägter Paramagnetismus des Komplexes folgt. Der Komplex ist eine Lewis-Säure und kann seine Koordinationszahl von 6 auf 8 erhöhen. Die Verbindung besitzt eine hohe Affinität gegenüber harten Lewis-Basen, wie Sauerstoffatomen in Ethern und Stickstoffatomen in Aminen. Eu(fod)3 ist in unpolaren Lösungsmitteln löslich und zeigt im Vergleich mit Europium-Komplexen mit Acetylaceton und Hexafluoroacetylaceton eine erhöhte Löslichkeit.
Verwendung
[Bearbeiten | Quelltext bearbeiten]NMR-Shift-Reagenz
[Bearbeiten | Quelltext bearbeiten]Die ursprüngliche Anwendung von Eu(fod)3 bestand darin, diastereomere Verbindungen in der NMR-Spektroskopie zu untersuchen. Dabei induziert es eine für paramagnetische Verbindungen typische chemische Verschiebung. Für Protonen in der Nähe des Lewis-basischen Zentrums ist diese Verschiebung ausgeprägter. Diese Veränderung ermöglicht es, schlecht aufgelöste Signale aufzutrennen. Es werden nur geringe Mengen des Shift-Reagenz verwendet, da der Paramagnetismus der Verbindung ansonsten zu einer verkürzten Spin-Gitter-Relaxationszeit führt und die Signale so verbreitert werden und die Auflösung sinkt. Durch die Verfügbarkeit von Spektrometern mit höheren magnetischen Feldern und dem damit verbundenen erhöhten Auflösungsvermögen, ist der Bedarf an Shift-Reagenzien gesunken.
Lewis-Säure
[Bearbeiten | Quelltext bearbeiten]Eu(fod)3 kann als Lewis-acider Katalysator in organischen Synthesen wie stereoselektiven Diels-Alder and Aldoladditionen verwendet werden. Zum Beispiel kann Eu(fod)3 die Cyclocondensation von substituierten Dienen mit aromatischen und aliphatischen Aldehyden zu Dihydropyranen katalysieren und zeigt dabei eine hohe Selektivität für das endo-Produkt.[3]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d Datenblatt Resolve-Al™ EuFOD bei Sigma-Aldrich, abgerufen am 24. Januar 2020 (PDF).
- ↑ Robert E. Sievers, Roger E. Rondeau: New Superior Paramagnetic Shift Reagents for Nuclear Magnetic Resonance Spectral Clarification. In: Journal of the American Chemical Society. Band 93, Nr. 6, März 1971, S. 1522–1524, doi:10.1021/ja00735a049.
- ↑ Wenzel, T.J.; Ciak, J.M.; Europium, tris(6,6,7,7,8,8,8-heptafluoro-2,2-dimethyl-3,5-octanedianato), in: Encyclopedia of Reagents for Organic Synthesis, 2004. John Wiley & Sons, Ltd. (doi:10.1002/047084289X.rn00449).