Condylomata acuminata
| Klassifikation nach ICD-10 | |
|---|---|
| A63.0 | Anogenitale (venerische) Warzen |
| ICD-10 online (WHO-Version 2019) | |
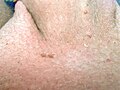
Bei Condylomata acuminata – auch unter dem Begriff Feigwarzen, Feigblattern, Feuchtwarzen und Genitalwarzen bekannte Warzen – oder kurz Kondylomen handelt es sich um eine Viruserkrankung. Feigwarzen sind kleine, weiche rosa Warzen (papillomatöse Fibroepitheliome), die am häufigsten an den Schamlippen, am Penisschaft und auf der Vorhaut vorkommen, sich aber auch um den Enddarm oder in der Mundhöhle befinden können. Sie sind neben Herpes genitalis und Chlamydiose eine der häufigsten sexuell übertragbaren Erkrankungen.

Erreger
[Bearbeiten | Quelltext bearbeiten]Feigwarzen werden zu 90 % durch Niedrigrisikotypen des humanen Papillomvirus (HPV) verursacht.[1] Die auch Kondyloma-Viren genannten Erreger sind kugelförmige, unbehüllte, doppelsträngige DNA-Viren (dsDNA), die zu den Papillomaviridae gehören, und von denen insgesamt 200 verschiedene (davon ca. 40 anogenitale) Typen bekannt sind. Die anogenitalen HPV-Typen werden in Niedrigrisikotypen (z. B. 6 und 11) und Hochrisikotypen (z. B. 16 und 18) unterschieden. Während eine persistierende Infektion mit Hochrisikotypen das Risiko für bestimmte Krebsformen (v. a. Gebärmutterhalskrebs, in seltenen Fällen aber auch für Peniskarzinom, Analkrebs und Krebs im Mund-Rachen-Raum) erhöht, besitzen Veränderungen durch Niedrigrisikotypen kaum Entartungspotenzial.
Übertragung und Verbreitung
[Bearbeiten | Quelltext bearbeiten]Grundsätzlich werden die Krankheitserreger durch Kontaktinfektion beziehungsweise Schmierinfektion übertragen.[2] Damit ist es theoretisch möglich, dass HP-Viren bei fast allen Haut-zu-Haut-Kontakten übertragen werden können, Hauptursache für eine Infektion ist aber der ungeschützte Geschlechtsverkehr. Eine Infektion auf anderen Wegen, z. B. in der Sauna, beim Baden oder sogar auf Türklinken, ist zwar möglich, aber höchst selten.[3]
Aufgrund des Infektionsweges von HPV bieten Kondome keinen völligen Schutz. Eine Studie zur Schutzwirkung von Kondomen vor HPV hat aber ergeben, dass sich durch konsequenten Kondomgebrauch im Laufe eines Jahres ca. 70 % aller HPV-Infektionen verhindern lassen.[4]
Global gesehen steigt die Anzahl an Neuinfektionen mit Feigwarzen kontinuierlich an.[5] Es existieren verschiedene Hypothesen über die Ursache dieser Entwicklung. Eine davon lautet, dass die bei Intimrasuren entstehenden kleinen Verletzungen das Risiko für Feigwarzen begünstigen und immer mehr Menschen sich im Intimbereich rasieren.[6] Die Haupt-Risikofaktoren bleiben dennoch:
- ungeschützter Geschlechtsverkehr, besonders wenn er mit mehreren Personen und in jungen Jahren ausgeführt wird[7]
- Faktoren, die die Immunabwehr des Körpers schwächen, wie Stress, Rauchen, Immunsuppressiva.[5]
Darüber hinaus wird auch empfohlen, Unterwäsche heiß zu waschen, da die HP-Viren bei 55 °C inaktiviert werden.[3]
Etwa 1 % bis 2 % der sexuell aktiven Bevölkerung haben sichtbare Feigwarzen.[8] Darüber hinaus weisen ca. 5 bis 10 % der Bevölkerung subklinische HPV-assoziierte Läsionen im Anogenitalbereich auf, die mit bloßem Auge nicht zu erkennen sind und in der Regel nicht diagnostiziert werden. Bei ca. 60 % der Bevölkerung lassen sich Antikörper gegen HPV im Blut finden, die eine frühere Infektion nachweisen.[9] Das Risiko, im Laufe des Lebens eine HPV-Infektion durchzumachen, wird folglich mit zwischen 75 % und 80 % beziffert.[10]
Aufgrund der hohen Infektiosität und Verbreitung ist eine HPV-Infektion eine fast zwangsläufige Konsequenz sexueller Kontakte. Fünf Jahre nach Beginn ihrer sexuellen Aktivität haben sich ca. 70 % aller Frauen mit mindestens einem anogenitalen HPV-Typ infiziert.[11] Zwischen 64 und 70 % der männlichen Beziehungspartner von Frauen, die unter einer zervikalen HPV-Erkrankung leiden, weisen wiederum – wie mehrere Studien zeigen – ihrerseits HPV-assoziierte Läsionen am Penis auf.[12]
Lokalisation
[Bearbeiten | Quelltext bearbeiten]Eine feuchte und warme Umgebung begünstigt die Entwicklung von Feigwarzen, daher finden sie gerade in Hautrissen im Genital- und Analbereich ideale Wachstumsbedingungen vor.[13] Feigwarzen bleiben auf Grund ihres Typus lokal beschränkt. Bei beiden Geschlechtern finden sich Feigwarzen somit im Analbereich, seltener im Enddarm. Bei der Frau sind vor allem die Schamlippen sowie die Scheide, seltener Gebärmutterhals betroffen. Beim Mann können die Eichel, die Vorhaut am Penis und auch der Hodensack befallen sein.[5]
Krankheitsverlauf und Symptome
[Bearbeiten | Quelltext bearbeiten]Zwischen der Infektion und dem ersten Auftreten der Feigwarzen liegt eine Ausbruchszeit von einigen Tagen oder Wochen bis zu mehreren Monaten – und in sehr seltenen Fällen auch Jahren.[14] Allerdings muss nicht jede Infektion zwingend zu einer Warze führen. Die HP-Viren persistieren in den Stachel- und Plattenepithelzellen der Epidermis. Somit sind die Betroffenen zwar Virusträger, aber die Krankheit bricht nicht aus. Man spricht in so einem Fall auch von einer stummen Infektion.[15]
Die Mehrzahl der Infektionen verläuft ohne klinische Symptome und ist nach einiger Zeit selbst mit aufwendigen Methoden nicht mehr nachweisbar. In etwa 30 % der Fälle heilen aufgetretene Feigwarzen von selbst wieder ab.
Die Krankheitserreger bilden in der Genitalregion oder am After meist kleine Warzen, die papillomatösen Fibroepitheliome,[16] die zur Beetbildung neigen und dann konfluierende (sich vereinigende) Warzen ausbilden. Kleinere Herde weisen dabei meist keine Symptome auf, größere können schmerzhafte Einrisse, Spannungsgefühl und ein Sekundärekzem verursachen.[17] Insgesamt ist die Erkrankung selbst unbehandelt nicht tödlich, kann jedoch erheblichen negativen Einfluss auf die (sexuelle) Lebensqualität des Patienten erlangen. Ein eventuell betroffener Partner sollte sich dabei unbedingt auch auf das HP-Virus untersuchen und gegebenenfalls behandeln lassen, damit es nicht zu einer wiederholten gegenseitigen Infektion kommt.
Condylomata acuminata werden nahezu immer durch Niedrigrisikotypen (in über 90 % der Fälle durch HPV 6 oder 11)[18] verursacht, die nicht als kanzerogen gelten. Bei einer jahrelangen Erkrankung und nicht ausreichender Behandlung können Feigwarzen trotzdem entarten, bei Frauen etwas häufiger als bei Männern. Deshalb wird zu einer Behandlung geraten.[3] Gelegentlich entstehen nämlich auch sehr große Tumoransammlungen, welche als Condylomata gigantea oder Buschke-Löwenstein-Tumoren bezeichnet werden. Sie zeichnen sich durch destruierendes Wachstum und benigne Entartung aus. Unbehandelt können sie auch aufbrechen und stark bluten.[17][19]
-
Feigwarzen im rasierten Schambereich an Peniswurzel, ca. 6 bis 10 Monate nach Infektion
-
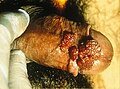
Stark ausgeprägter Feigwarzenbefall am Penis
-
Stark ausgeprägter Feigwarzenbefall in der Vulva
Diagnostik
[Bearbeiten | Quelltext bearbeiten]In der Regel erfolgt aufgrund des charakteristischen Erscheinungsbildes nur eine Blickdiagnose. Bei unklarem klinischen Bild stehen dem behandelnden Arzt weitere diagnostische Maßnahmen offen.
- Essigsäuretest: Eine drei- bzw. fünfprozentige Essigsäure färbt betroffene Areale weißlich. Hierbei können eher unauffällige Zellveränderungen sichtbar gemacht sowie die Ausbreitung besser eingeschätzt werden, falls die Kondylome chirurgisch entfernt werden sollen. Allerdings ist der Essigsäuretest unspezifisch und wenig sensitiv, d. h. sich verfärbende Areale sind nicht zwingend HPV-assoziiert. Falls sich verdächtige Areale nicht verfärben, bedeutet dies aber auch nicht zwingend, dass es sich nicht um Kondylome handelt. Daher kann der Test nur von einem erfahrenen Arzt richtig interpretiert werden.
- Histologische Untersuchung: Eine Gewebeprobe kann im Labor histologisch untersucht werden. Insbesondere Koilozyten gelten als Marker für HPV-assoziierte Hautveränderungen. Es finden sich aber auch zum Teil Hyper- und Parakeratosen.[20]
- Virusnachweis: Der Nachweis von HPV-DNA gehört nicht zu der Routinediagnostik bei Condylomata acuminata. Dennoch ist ein Test per Abstrich von einer verdächtigen Stelle möglich. Als Testmethoden sind Sondentests (weit verbreitet, günstig, differenziert zwischen High und Low Risk) von Tests durch eine Polymerase-Kettenreaktion (PCR) (teuer, sehr sensitiv, erlaubt die Bestimmung des exakten Virustyps) zu unterscheiden. Die PCR zeichnet sich im Vergleich durch eine deutlich höhere Sensitivität und Spezifität aus.[21]
- HPV-Serologie: HPV-Infektionen verlaufen ohne Virämie. Daher lassen sich die Viren nicht im Blut nachweisen. Der Nachweis von Antikörpern ist wissenschaftlichen Untersuchungen vorbehalten und aufgrund der hohen Durchseuchung ohne diagnostischen Nutzen.
- Durch eine Kolposkopie, Anoskopie, Proktoskopie und bzw. oder Urethroskopie können „innere“ Kondylome ausgeschlossen werden. Vor derartigen Untersuchungen sollten äußere Kondylome entfernt werden, weil ansonsten die Gefahr besteht, die Infektion durch die Untersuchung selbst zu verschleppen.[19]
Differentialdiagnosen
[Bearbeiten | Quelltext bearbeiten]Eine Infektion mit Niedrigrisikotypen wie HPV 6 oder HPV 11 ist von einer Infektion mit HPV 16 und HPV 18 abzugrenzen, da bei Frauen mit einer Infektion der letztgenannten Typen die Gefahr besteht, an Gebärmutterhalskrebs zu erkranken. Differenzialdiagnostisch sind Condylomata acuminata insbesondere von anderen gutartigen Tumoren (z. B. Fibromen), heterotopen Talgdrüsen, Hirsuties papillaris penis, Hirsuties vulvae, Hymenalresten, prämalignen und malignen Veränderungen sowie anderen Infektionen (z. B. Condylomata lata durch Lues), auch Fokale epitheliale Hyperplasie zu unterscheiden.[19] Die veralteten Bezeichnungen Feigwarzen (von mittelhochdeutsch vīcwarze) und Feigblattern bezogen sich vom Mittelalter bis in die Neuzeit sowohl auf die Condylomata acuminata als auch auf Hämorrhoidalknoten bzw. Hämorrhoiden (II. bis III. Grades mit blutigem Ausfluss) und Marisken.[22][23] Um die Diagnose abzusichern, kann eine histologische Untersuchung und/oder ein Virusnachweis durchgeführt werden.
Komplikationen
[Bearbeiten | Quelltext bearbeiten]Da HPV häufig in Zusammenhang mit einem erhöhten Krebsrisiko genannt wird, sei darauf hingewiesen, dass eine alleinige Infektion mit Niedrigrisikotypen, die Condylomata acuminata auslösen, das Krebsrisiko in der Regel nicht erhöht. Da Hochrisikotypen aber den identischen Infektionsweg wie Niedrigrisikotypen haben, ist bei Condylomata acuminata eine parallele Infektion mit einem Hochrisikotyp nicht ausgeschlossen. Erste Studien weisen darauf hin, dass Patienten mit Condylomata acuminata eine vergleichsweise hohe Gefahr haben, zusätzlich mit einem Hochrisikotyp infiziert zu sein, weswegen ein routinemäßiger HPV-Test auf Hochrisikotypen (per Abstrich vom Gebärmutterhals) durchaus gerechtfertigt scheint.[24] Falls Hochrisikotypen nachgewiesen werden, ist die Persistenz der Infektion zu überprüfen. In aller Regel kann das Immunsystem die Infektion erfolgreich bekämpfen, so dass sie nach zwei Jahren bei den meisten Frauen nicht mehr nachzuweisen ist. Falls die Infektion mit Hochrisikotypen aber persistiert, erhöht sich deutlich das Risiko, an Gebärmutterhalskrebs zu erkranken.
Größere Kondylome (insbesondere Condylomata gigantea) können den Geburtskanal behindern, was eine Geburt durch Kaiserschnitt notwendig erscheinen lassen kann. Generell kann ein Kaiserschnitt das Risiko einer Übertragung von HPV auf das Kind mindern, aber nicht zuverlässig verhindern.[25]
In seltenen Fällen kann es nach der Übertragung von Niedrigrisikotypen während der Geburt auf das Neugeborene zu einer Larynxpapillomatose kommen.
Behandlung
[Bearbeiten | Quelltext bearbeiten]Ärztliche Eingriffe
[Bearbeiten | Quelltext bearbeiten]Neben der chirurgischen Entfernung ist eine Warzenentfernung mit Laser, Elektrokoagulation, Kauterisierung (Verbrennung mit Kauter) oder Kryotherapie (Vereisung) möglich. Bei der Vereisung wird mit flüssigem Stickstoff oder anderen Vereisungssprays versucht, die Warzen zu entfernen.
Nach der Entfernung kann es zu Schwellungen und Narbenbildung kommen. Sollen Kondylome auch am After behandelt werden, besteht die Gefahr, dass der Schließmuskel verletzt wird, so dass er entweder nicht mehr schließen kann oder seine Dehnfunktion verliert, mit der möglichen Folge einer Inkontinenz.
Medikamentöse Behandlung
[Bearbeiten | Quelltext bearbeiten]- Bei einer Kauterisierung durch Verätzung erfolgt eine Behandlung mit den verschiedensten Mitteln wie Salicylsäurelotionen, Trichloressigsäure, Monochloressigsäure oder Silbernitrat. Viele gängige „begrenzt viruzide“ Desinfektionsmittel eignen sich nicht zur Desinfektion, da es sich bei HPV um ein unbehülltes Virus handelt.
- Bei einer äußerlichen zytostatischen Behandlung werden Medikamente wie Podophyllotoxin oder 5-Fluoruracil aufgetragen. Die Behandlung mit Podophyllin gilt mittlerweile als obsolet aufgrund von erhöhter Toxizität und des Verdachts karzinogener Effekte.[26] Als Ersatz dafür gibt es heute den aus Podophyllin isolierten und deutlich verträglicheren Hauptwirkstoff Podophyllotoxin in Form einer Salbe (Wartec) oder einer Lösung (Condylox) zur Heimanwendung.
- Isotretinoin hat sich in experimenteller Anwendung als effektiv in Fällen von Feigwarzen gezeigt, die durch andere Therapien nicht behandelt werden konnten. Aufgrund der starken Nebenwirkungen von Isotretinoin wird diese Therapie jedoch selten durchgeführt. Es gibt nur wenige Studien über die Anwendung von Isotretinoin bei Genitalwarzen, und diese Therapie ist off-label.[27][28]
- Stärkung der Immunabwehr zur Bekämpfung der warzenverursachenden Viren mit Medikamenten wie etwa Interferon, Sinecatechinen (Grünteeextrakte) (Veregen, VeregenRX) und Imiquimod (Aldara) provoziert eine lokal begrenzte Entzündung, regt die lokale Produktion von Antikörpern an und führt zu einer vermehrten Produktion von Interferonen, die tumorhemmend wirken. Im Schnitt ist eine konsequente Therapie mit Imiquimod-Salbe bei jedem zweiten Patienten erfolgreich. Nach einer erfolgreichen Therapie mit Imiquimod soll die Rezidivquote niedriger als bei den anderen verfügbaren Therapieformen sein. Daher wird die Creme teilweise auch zur postoperativen Rezidivprophylaxe verschrieben. Polyphenon E Salbe (Veregen) hat, ähnlich wie Imiquimod eine immunmodulierende Wirkung und erzielte in Zulassungsstudien ähnliche Erfolgsquoten mit einer niedrigen Rezidivquote.[29]
Alle genannten Behandlungsmethoden können aufgrund der exponierten Position der betroffenen Körperstellen mit mehr oder weniger schmerzhaften Irritationen einhergehen. Zudem ist die Therapie häufig langwierig und erfordert ein hohes Maß an Disziplin von den Patienten. Die Existenz eines Ping-Pong-Effekts ist umstritten. Konsequenter Kondomgebrauch scheint aber den Heilungsverlauf zu unterstützen.[10] An dieser Stelle sei allerdings nochmals darauf hingewiesen, dass Kondome generell die Infektionsgefahr durch HPV deutlich vermindern, aber keinen vollständigen Schutz garantieren.
Immunsuppression
[Bearbeiten | Quelltext bearbeiten]Personen, die mit Medikamenten behandelt werden, welche das Immunsystem unterdrücken sollen (Immunsuppression), wie beispielsweise bei Krebs, Organtransplantation oder Lupus erythematodes, sind ebenfalls für eine derartige Infektion anfällig.[30], da Immunsuppressiva eine aktivere Replikation der Papillomaviren in der ganzen Haut ermöglichen.[31]
Behandlungsmethoden ohne nachgewiesene Wirkung
[Bearbeiten | Quelltext bearbeiten]Neben den anerkannten Behandlungsmethoden werden auch alternative Medikamente angeboten. Insbesondere Thuja- oder Teebaumöl werden positive Effekte nachgesagt. Ebenso werden im Internet mehrere pflanzliche Salben und Lösungen angeboten, deren Wirksamkeit niemals in wissenschaftlichen Untersuchungen nachgewiesen wurde.
Ausblick
[Bearbeiten | Quelltext bearbeiten]- Mehrere therapeutische Impfungen gegen HPV befinden sich in frühen klinischen Testphasen. Dabei steht insbesondere die Therapie von Dysplasien, die durch Hochrisikotypen verursacht werden, im Mittelpunkt des Interesses. Allerdings wird auch an therapeutischen Impfstoffen gegen Niedrigrisikotypen, die Condylomata acuminata auslösen, geforscht.[32] Im Gegensatz zu dem einzigen verfügbaren Impfstoff gegen Feigwarzen (Gardasil), der die L1-Kapsid-Proteine der HPV-Typen 6, 11 (Low Risk) und 16, 18 (High Risk) enthält und nur prophylaktischen Schutz bietet, enthalten die therapeutischen Impfstoffe zumeist die tumorexprimierten Proteine E1, E2, E6 oder E7 und regen daher das Immunsystem dazu an, bereits infizierte Zellen abzustoßen. Einzige Ausnahme ist die experimentelle therapeutische Impfung gegen Genitalwarzen, welche in Australien und der Volksrepublik China erforscht wird (siehe nächster Punkt).
- In einer klinischen Phase-2-Studie an der University of Queensland (Australien) in Zusammenarbeit mit dem Wenzhou Medical College (China) sollte geklärt werden, ob eine Immunisierung mit L1 VLPs ohne Adjuvans einen therapeutischen Effekt auf HPV-Infektionen hat. In einer Pilotstudie aus dem Jahr 1999[33] führte die Immunisierung mit L1-VLPs zu einer kompletten Rückbildung der Warzen bei ca. 75 % der Studienteilnehmer innerhalb von 20 Wochen. Daraus schlossen die Wissenschaftler, dass eventuell auch das Protein L1 für eine therapeutische Impfung geeignet ist. Das in Gardasil® verwendete Adjuvans Aluminium scheint aber die für eine therapeutische Wirkung nötigen zytotoxischen Effekte zu verhindern.[34] Die Studie sollte im April 2008 enden, Ergebnisse sollten voraussichtlich gegen Ende desselben Jahres veröffentlicht werden. Eine Markteinführung wurde geschätzt wäre bei positiven Studienergebnissen frühestens 2012 zu erwarten.[35] Im Jahr 2018 waren therapeutische Impfungen noch immer in Entwicklung.[36]
- 2010 wurde eine Phase-III-Studie zur Wirksamkeit von niedrigdosiertem Cyclophosphamid (7 Tage 50 mg/d) nach erfolgter Laser-Therapie beendet. Es zeigte sich eine komplette Remission und ein Ausbleiben von Rezidiven.[37]
Vorbeugung
[Bearbeiten | Quelltext bearbeiten]Wirksamste Vorbeugung gegen eine Infektion sind Enthaltsamkeit und die Impfung. Safer Sex bietet keinen vollständigen Schutz, verringert die Gefahr einer Ansteckung jedoch deutlich.[38] Der prophylaktische HPV-Impfstoff Gardasil gegen die HPV-Typen 6, 11, 16 und 18 – von der amerikanischen Arzneimittelbehörde (FDA) in den USA im Juni 2006, von der europäischen Arzneimittelagentur im September 2006 in der EU zugelassen – schützt nach den bislang vorliegenden Untersuchungen zu 100 % vor einer Infektion mit den genannten Virentypen. Jungen im Alter von 9 bis 15 Jahren entwickelten nach Impfung eine Immunität. Der quadrivalente Impfstoff wurde in einer Studie mit 4.065 Jungen und Männern im Alter von 16 bis 26 Jahren als effektiv beurteilt.[39] Für homosexuelle Männer läuft eine weltweite klinische Studie zur Vorbeugung vor Geschlechtskrankheiten, insbesondere Feigwarzen, ferner Studien mit dem HPV-Impfstoff. Ziel ist eine Schutzimpfung zur Vorbeugung gegen Anal- und Peniskrebs, deren Entstehung ebenfalls mit Infektionen durch HPV in Verbindung gebracht wird. Aufgrund des Übertragungsweges besteht für homosexuelle Männer ein erhöhtes Risiko, ein Analkarzinom zu entwickeln.
Alle HPV-Impfstoffe wirken vorbeugend; eine bereits bestehende HPV-Infektion kann nicht behandelt oder gar beseitigt werden. Die Erstimmunisierung sollte daher vor dem ersten Geschlechtsverkehr abgeschlossen sein, da die Impfung offenbar keinen Einfluss auf bereits bestehende Infektionen hat.[40] Eine abschließende Beurteilung der Wirksamkeit sowie der Verträglichkeit ist wie bei allen neuen Medikamenten und Verfahren nicht möglich, Nebenwirkungen scheinen bislang allerdings keine Rolle zu spielen. Unklar ist, wie lange ein solcher Impfschutz anhalten wird. Bislang wird eine Grundimmunisierung mit drei Impfungen im Abstand von null, zwei und vier bis sechs Monaten empfohlen, Richtlinien zur Impfauffrischung gibt es nicht, da Langzeitstudien zum Verlauf der Schutzwirkung über die gesamte Lebensspanne gesehen zwangsläufig fehlen. Da die Impfung nicht gegen alle HPV-Typen wirkt, sollten aber auch geimpfte Frauen die Vorsorgeuntersuchungen gegen Gebärmutterhalskrebs (ab 20 Jahren) auf jeden Fall nutzen.
2011 wurden erste Daten nach Einführung eines flächendeckenden Impfprogramms mit einem quadrivalenten Impfstoff publiziert. Das Programm wurde 2007 in Australien etabliert. Die Impfquote liegt dort bei 80 bis 90 Prozent. Bereits drei Jahre nach Beginn der Impfkampagne sind die behandlungsbedürftigen Krebsvorstufen bei Mädchen unter 18 Jahren um 59 Prozent zurückgegangen.[41][42]
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Condylomata acuminata und andere HPV-assoziierte Krankheitsbilder von Genitale, Anus und Harnröhre, Leitlinien der Deutschen STD-Gesellschaft in Zusammenarbeit mit der Deutschen Dermatologischen Gesellschaft und der Paul-Ehrlich-Gesellschaft, Juli 2006.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Cloe Borton, Laurence Knott: Human Papillomavirus and Genital Warts, 19. Juli 2013; abgerufen am 24. April 2015
- ↑ Was sind Feigwarzen und wie häufig kommen sie vor?, Geschlechtskrankheiten.de – Das Informationsportal für sexuell übertragbare Krankheiten; abgerufen am 18. April 2015
- ↑ a b c Dr. med. Harald Bresser: Condylome, Feigwarzen, HP-Viren: Diagnose, Ursache, Behandlung der Genitalwarzen
- ↑ Condom Use and the Risk of Genital Human Papillomavirus Infection in Young Women. (PDF) In: The new england journal of medicine. 22. Juni 2006, (englisch).
- ↑ a b c Anale Feigwarzen. ( vom 5. April 2015 im Internet Archive; PDF) Leitlinien der deutschen Gesellschaft für Koloproktologie; abgerufen am 22. April 2015
- ↑ Intimrasur begünstigt Feigwarzen. In: www.schleswig-holstein.de. Der Ministerpräsident des Landes Schleswig-Holstein - Staatskanzlei, archiviert vom (nicht mehr online verfügbar) am 3. Mai 2015; abgerufen am 13. Juli 2017.
- ↑ What are genital warts? What causes genital warts? medicalnewstoday.com; abgerufen am 22. April 2015
- ↑ Susanne Krüger Kjær, Trung Nam Tran, Par Sparen, Laufey Tryggvadottir, Christian Munk, Erik Dasbach, Kai-Li Liaw, Jan Nygård, Mari Nygård: The Burden of Genital Warts: A Study of Nearly 70,000 Women from the General Female Population in the 4 Nordic Countries. In: The Journal of Infectious Diseases. 196, 2007, S. 1447, doi:10.1086/522863.
- ↑ arhp.org ( vom 19. Oktober 2007 im Internet Archive)
- ↑ a b Humane Papillomviren und Krebs: Antworten auf häufige Fragen – Ansteckungswege: Wie werden die Viren übertragen?, Krebsinformationsdienst des Deutschen Krebsforschungszentrums (DKFZ), Heidelberg. Vom 17. Februar 2014. Zuletzt abgerufen am 4. September 2014.
- ↑ Symposiumsbericht ( vom 8. Mai 2007 im Internet Archive)[ digene.de] (PDF)
- ↑ Häufige Fragen zu Humanen Papillomviren (HPV) und Gebärmutterhalskrebs. cervical cancer consortium europe
- ↑ Renate Huch, Klaus D. Jürgens (Hrsg.): Mensch, Körper, Krankheit. 6. Auflage. Elsevier / Urban & Fischer, München 2011, ISBN 978-3-437-26792-5, S. 138, 409.
- ↑ Dr. med. Nonnenmacher: Feigwarzen (HPV). 19. März 2014; abgerufen am 24. April 2015
- ↑ Risikofaktoren für die Ansteckung mit HPV und die Entstehung von Feigwarzen. geschlechtskrankheiten.de; abgerufen am 22. April 2015
- ↑ Günter W. Korting: Praxis der Dermatologie. Ein Lehrbuch für die Aus- und Weiterbildung. Stuttgart 1982, S. 149–150.
- ↑ a b Volker Schumpelick, Niels Bleese, Ulrich Mommsen et al.: Kurzlehrbuch Chirurgie S. 364, 8. Auflage, Georg Thieme Verlag, Stuttgart · New York, ISBN 978-3-13-127128-0
- ↑ Condylome. ( vom 20. Dezember 2010 im Internet Archive) Uni München, Patienteninfo.
- ↑ a b c HPV-assoziierte Läsionen der äußeren Genitalregion und des Anus – Genitalwarzen und Krebsvorstufen der Vulva, des Penis und der peri- und intraanalen Haut. ( vom 16. Juli 2020 im Internet Archive) (PDF) AWMF-Leitlinie 082-008, abgerufen am 14. August 2019
- ↑ Histologie und Zytologie gut- und bösartiger Veränderungen der Vulva. ( vom 21. März 2005 im Internet Archive) (PDF) aixcyto.de
- ↑ Papillomavirus (HPV)-Diagnostik. ( vom 10. Februar 2011 im Internet Archive) labor-bo.de
- ↑ Max Höfler: Deutsches Krankheitsnamen-Buch. München 1899, S. 781.
- ↑ Jürgen Martin: Die ‚Ulmer Wundarznei‘. Einleitung – Text – Glossar zu einem Denkmal deutscher Fachprosa des 15. Jahrhunderts. Königshausen & Neumann, Würzburg 1991 (= Würzburger medizinhistorische Forschungen. Band 52), ISBN 3-88479-801-4 (zugleich Medizinische Dissertation Würzburg 1990), S. 185.
- ↑ Stellungnahme der Deutschen Gesellschaft für Zytologie (DGZ) zum primären Screening auf Humane Papillom-Viren ( vom 9. Juli 2007 im Internet Archive) (PDF; 120 kB)
- ↑ Schwangerschaft und HPV ( vom 4. Oktober 2012 im Internet Archive), Gesundheitsamt Baden-Württemberg
- ↑ Ersatz für Podophyllin-haltige Rezepturen. dermotopics.de, Ausg. 2/2001, Gesellschaft für Dermopharmazie e. V.
- ↑ S. Georgala, A. C. Katoulis, C. Georgala, E. Bozi, A. Mortakis: Oral isotretinoin in the treatment of recalcitrant condylomata acuminata of the cervix: a randomised placebo controlled trial. In: Sexually Transmitted Infections. 80. Jahrgang, Nr. 3, November 2004, S. 216–218, doi:10.1136/sti.2003.006841.
- ↑ Virendra N. Sehgal, Govind Srivastava, Kabir Sardana: Isotretinoin – unapproved indications/uses and dosage: a physician’s reference. In: International Journal of Dermatology. 45. Jahrgang, Nr. 6, Mai 2006, S. 772–777, doi:10.1111/j.1365-4632.2006.02830.x.
- ↑ Veregen®: lokale Salbe aus Grüntee-Extrakt gegen Genitalwarzen (Condylomata acuminata) ( vom 4. Juli 2010 im Internet Archive) bei Medknowledge, 2010
- ↑ Apotheken Umschau: Geschlechtskrankheiten. 7. Dezember 2020, abgerufen am 22. Dezember 2023.
- ↑ U. Wieland, A. Kreuter, H. Pfister: Human papillomavirus and immunosuppression. In: Current problems in dermatology. Band 45, 2014, S. 154–165, doi:10.1159/000357907, PMID 24643184 (Review).
- ↑ Warts vaccine: one of many in pipeline. The University of Queensland Australia (englisch)
- ↑ L. F. Zhang et al.: HPV6b virus like particles are potent immunogens without adjuvant in man. In: Vaccine. Band 18, Nummer 11–12, Januar 2000, S. 1051–1058, PMID 10590325.
- ↑ Website des International RRP ISA Center ( vom 12. März 2008 im Internet Archive)
- ↑ Protection at a price. australiandoctor.com.au, 26. Oktober 2006 (englisch).
- ↑ Hancock, Hellner, Dorrell: Therapeutic HPV vaccines. In: Best Pract Res Clin Obstet Gynaecol, 2018 Feb;47, S. 59–72, doi:10.1016/j.bpobgyn.2017.09.008, PMID 29108943
- ↑ CD4+FOXP3+ regulatory T cell depletion by low-dose cyclophosphamide prevents recurrence in patients with large condylomata acuminata after laser therapy. PMID 20338811
- ↑ Zervixkarzinom: Kondome verhindern HPV-Infektionen. ( vom 3. September 2007 im Internet Archive) ärzteblatt-studieren.de, 22. Juni 2006
- ↑ Anna R. Giuliano et al.: Efficacy of Quadrivalent HPV Vaccine against HPV Infection and Disease in Males. In: N Engl J Med, Nr. 364, 2011, S. 401–411, doi:10.1056/NEJMoa0909537.
- ↑ HPV-Impfung ohne therapeutische Wirkung. ( vom 23. Januar 2008 im Internet Archive) ärzteblatt.de, 15. August 2007.
- ↑ Früher Rückgang der Zervixläsionen durch HPV-Impfung. In: Deutsches Ärzteblatt. Nachrichten vom 20. Juni 2011, Archivlink abgerufen am 22. Dezember 2023
- ↑ Julia ML Brotherton, Masha Fridman, Cathryn L May, Genevieve Chappell, A Marion Saville, Dorota M Gertig: Early effect of the HPV vaccination programme on cervical abnormalities in Victoria, Australia: an ecological study. In: The Lancet, Nr. 377, 2011, S. 2085–2092, doi:10.1016/S0140-6736(11)60551-5.