Homoallyl-Stellung
Der Begriff der Homoallyl-Stellung leitet sich aus den Silben homo und allyl ab.[1] Dabei ist mit homo in der Organischen Chemie häufig gemeint, dass eine Methylengruppe in eine Grundverbindung eingefügt ist.[2] In diesem Fall ist die Grundverbindung die Allylgruppe, was durch die Silbe allyl gekennzeichnet ist. Homoallyl bedeutet also, dass eine Methylengruppe an die Allylgruppe angehängt ist. Die Konstitutionsformel der Homoallylgruppe lautet demnach: H2C=CH–CH2–CH2–.
Ein Rest R, wie eine funktionelle Gruppe befindet sich also in Homoallyl-Stellung, wenn dieser an das vierte Kohlenstoff-Atom nach einer Doppelbindung gebunden ist. Das Gleiche gilt dabei für Homoallyl-Radikale oder Homoallyl-Carbeniumionen:[1]

Homoallyl-Radikal (Mitte) und Homoallyl-Carbeniumion (rechts) mit blau markierter Homoallylgruppe
Typische Reaktionen
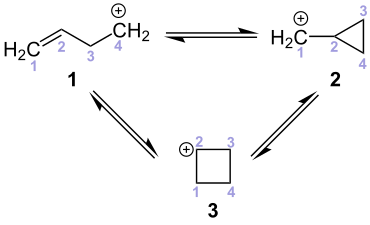
[Bearbeiten | Quelltext bearbeiten]Für Homoallyl-Carbeniumionen (1) sind Umlagerungsreaktionen typisch, die zu Cyclopropan-Carbeniumionen (2) und Cyclobutan-Carbeniumionen (3) führen.[3]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Homoallylalkohole und Homoallylamine sind wichtige Vertreter von chemischen Verbindungen, die funktionelle Gruppen in Homoallyl-Stellung enthalten. Sie sind häufig in der Synthese von pharmazeutisch relevanten Stoffen anzutreffen.[4][5] Dies liegt mitunter daran, dass sie enantioselektiv hergestellt werden können (vgl. Synthese von Homoallylalkoholen mit der Roush-Reaktion) und so zur Bildung von Stereozentren eingesetzt werden.[4] Ein Beispiel dafür ist die Synthese von Stevastelin B, einem Depsipeptid mit immunsuppressiven Effekten. Diese Verbindung wird mithilfe der Roush-Reaktion hergestellt.[4]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b S. Kubik: Eintrag zu Homoallyl-Stellung. In: Römpp Online. Georg Thieme Verlag, abgerufen am 4. August 2017.
- ↑ Eintrag zu Homo.... In: Römpp Online. Georg Thieme Verlag, abgerufen am 4. August 2017.
- ↑ M. Hanack, H.-J. Schneider: Nachbargruppeneffekte und Umlagerungen bei Reaktionen von Cyclopropylmethyl-, Cyclobutyl- und Homoallyl-Systemen. In: Angewandte Chemie. Band 79, Nr. 16, 1967, S. 709–720, doi:10.1002/ange.19670791603.
- ↑ a b c L. Kürti, B. Czakó: Strategic Applications of Named Reactions in Organic Synthesis. Elsevier Academic Press, Burlington / San Diego / London 2005, ISBN 0-12-369483-3, S. 386–387.
- ↑ T. R. Ramadhar, R. A. Matey: Allylation of Imines and Their Derivatives with Organoboron Reagents: Stereocontrolled Synthesis of Homoallylic Amines. In: Synthesis. Band 2011, Nr. 9, S. 1321–1346, doi:10.1055/s-0030-1258434.