Hydraziniumsulfat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
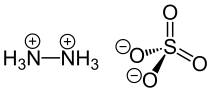
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Hydraziniumsulfat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | N2H6SO4 | |||||||||||||||
| Kurzbeschreibung |
farbloser, kristalliner, geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 130,12 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
1,37 g·cm−3 (20 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
schlecht in Wasser (30 g·l−1 bei 20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Hydraziniumsulfat ist ein Salz des Hydrazins und der Schwefelsäure. Der farblose Stoff ist ein Zwischenprodukt bei der Reindarstellung von Hydrazin.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Durch die Reaktion von Schwefelsäure mit Hydrazin
oder Hydrazinhydrat
lässt sich das Sulfat darstellen.
Im Labormaßstab lässt sich das N2H6SO4 durch die Reaktion einer Harnstofflösung mit basifizierter NaOCl-Lösung und anschließender Ansäuerung mit Schwefelsäure darstellen:[7]
Bei einer weiteren Laborsynthese wird eine Hydraziniumazidlösung mit Schwefelsäure umgesetzt, wobei das schwer lösliche Hydraziniumsulfat ausfällt.[8]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Hydrazinsulfat bildet farblose Kristalle. Es ist in kaltem Wasser wesentlich schlechter löslich als in heißem, was bei der Laborsynthese von Hydrazin (N2H4) ausgenutzt wird, indem man das Hydrazin zur Reinigung als Sulfat auskristallisieren lässt und anschließend noch einmal umkristallisiert, um im weiteren Verlauf wieder das Hydrazin(hydrat) freizusetzen.
Das Salz kristallisiert in einem orthorhombischen Kristallgitter mit der Raumgruppe P212121 (Raumgruppen-Nr. 19).[8] In der festen Phase wurde eine N2H62+SO42−-Struktur nachgewiesen, die wegen einer wesentlich höheren Gitterenergie gegenüber einer N2H5+HSO4−-Struktur bevorzugt ist.[8] In wässriger Lösung erfolgt wegen des sehr niedrigen zweiten KB2-Wertes des Hydrazins eine sofortige Gleichgewichtseinstellung zu N2H5+- und HSO4−-Ionen.[8]
Bei 254 °C schmilzt das N2H6SO4, wobei es schon bei einer Temperatur von etwa 250 °C beginnt, sich zu zersetzen.[6] Beim Glühen des reinen Produkts bleibt kein Rückstand, was als Reinheitstest von Hydrazinsulfat benutzt werden kann.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Das Sulfat findet als Reduktionsmittel Verwendung in der Mineralanalyse und es dient als Trennungsreagenz bei der Herstellung von Polonium. Darüber hinaus benutzt man es zur Synthese von Aziden und Hydrazinhydrat.
Hydraziniumsulfat dient in der Dünnschichtchromatographie als Sprühreagenz zum Nachweis von Piperonal und Vanillin. Dazu werden 90 mL gesättigte wässrige Hydraziniumsulfat-Lösung mit 10 mL 4 mol/L Salzsäure versetzt. Nach dem Aufsprühen dieser Lösung und anschließendem Bedampfen mit Ammoniak erfolgt die Auswertung im UV-Licht.[9]
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Hydraziniumsulfat stellt ein kräftiges Reduktionsmittel dar und sollte daher nicht mit Oxidationsmitteln in Kontakt gebracht werden. Beim Menschen zeigten sich bei einer Gabe von 201 mg/kg Körpergewicht über einen Zeitraum von acht Tagen Schläfrigkeit, Übelkeit und Parästhesie.[3] Es ist die Gefahr der Sensibilisierung bei Hautkontakt möglich. Darüber hinaus ist Hydraziniumsulfat beim Menschen wahrscheinlich krebserzeugend.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Eintrag zu Hydraziniumsulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag salts of hydrazine im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ a b Cancer Chemotherapy Reports, Part 1. Vol. 59, S. 1151, 1975.
- ↑ Gigiena Truda i Professional'nye Zabolevaniya. Labor Hygiene and Occupational Diseases. Vol. 28(12), S. 56, 1984.
- ↑ Sbornik Vysledku Toxixologickeho Vysetreni Latek A Pripravku, Marhold, J.V., Institut Pro Vychovu Vedoucicn Pracovniku Chemickeho Prumyclu Praha, Czechoslovakia, S. 15, 1972.
- ↑ a b Datenblatt Hydraziniumsulfat bei Merck, abgerufen am 11. Februar 2012.
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 468.
- ↑ a b c d Klapötke, T.M.; White, P.S.; Reaction of hydrazinium azide with sulfuric acid: The X-ray structure of [N2H6][SO4] in Polyhedron 15 (1996) 2579–2582, doi:10.1016/0277-5387(95)00527-7.
- ↑ E. Merck AG (Hrsg.): Anfärbereagenzien für Dünnschicht- und Papier-Chromatographie. Darmstadt 1965, S. 27.







