Kollagen-Typ 4α1
| Kollagen Typ IV, alpha 1 | ||
|---|---|---|
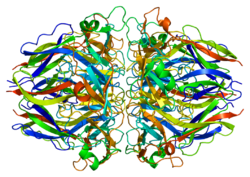
| ||
| Bändermodell des COL4A1-Proteins nach PDB 1LI1 | ||
| Andere Namen |
| |
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 160.615 Dalton / 1.669 Aminosäuren | |
| Isoformen | 2 | |
| Bezeichner | ||
| Gen-Namen | COL4A1 ; ICH; BSVD; RATOR; POREN1 | |
| Externe IDs | ||
| Vorkommen | ||
| Homologie-Familie | Hovergen | |
| Übergeordnetes Taxon | Euteleostomi | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 1282 | 12826 |
| Ensembl | ENSG00000187498 | ENSMUSG00000031502 |
| UniProt | P02462 | P02463 |
| Refseq (mRNA) | NM_001303110 | NM_009931 |
| Refseq (Protein) | NP_001290039.1 | NP_034061.2 |
| Genlocus | Chr 13: 110.15 – 110.31 Mb | Chr 8: 11.2 – 11.31 Mb |
| PubMed-Suche | 1282 | 12826
|
Kollagen Typ IV, alpha 1, auch bekannt als Alpha-1-Typ-IV-Kollagen, ist ein netzbildendes Kollagen, das im menschlichen Organismus vom Gen COL4A1 codiert wird. Zusammen mit zwei anderen α-Typ-IV-Kollagenen (α2 bis α6) formt es ein Trimer, sogenannte α-Ketten, die wiederum die eigentlichen Typ-IV-Kollagene bilden.[1] Typ-IV-Kollagen-Proteine sind integrale Bestandteile der Basalmembran, genauer der Lamina densa. Es wird zum größten Teil im Gehirn und in der Plazenta exprimiert.[2]
Geschichte
[Bearbeiten | Quelltext bearbeiten]Edward I. Solomon et al. fanden im Jahr 1985 heraus, dass mithilfe eines geklonten Gens als Gensonde für das Southern Blot einer DNA von einem Panel aus artübergreifenden somatischen Zellhybriden dem Gen COL4A1 zugewiesen werden kann und sich auf dem 13. Chromosom lokalisiert.[3] Im selben Jahr verwendeten Pihlajaniemi et al. einen Dual-Laser, wobei die Chromosomen bereits sortiert sind, und die Dot-Blot-Analysemethode um eine genomische DNA-Sequenz dem COL4A1 codierenden Gen auf dem 13. Chromosom zuzuordnen.[4]
Durch In-situ-Hybridisierung fanden Boyd et al. im Jahr 1986 heraus, dass das Gen sich am Ende des langen Chromosomenarms des 13. Chromosoms befindet. Durch Southern Blot und Dot Blot konnte herausgefunden werden, dass diese genomischen Sequenzen nur einmal in jedem haploiden Genom präsent sind.[5] Im gleichen Jahr konnten Emanuel et al. das COL4A1-Gen der telomeren Region 13q (13q34) zuordnen.[6] Bowcock et al. stellten fest, dass der COL4A1-Genlocus mit dem D13S3-Locus verbunden ist, welches wiederum durch In-situ-Hybridisierung dem Genlocus 13q33–q34 zugeordnet werden konnte. Dabei betrug der maximale LOD-Score 16,5 bei ϑ = 0,01.[7] Durch die Pulsed-Field-Gelelektrophorese und mit selten vorhandenen Restriktionsenzymen konnten Cutting et al. nachweisen, dass die Gene COL4A1 und COL4A2 einen Abstand von nicht mehr als 400 kb aufweisen.[8]
Bowcock et al. stellten im Jahr 1988 fest, dass die Wahrscheinlichkeit der Kopplung zwischen COL4A1 und COL4A2 bei ca. 2,8 % liegt bei einem LOD-Score von 19,98. Diese mangelnde Kopplung zwischen den beiden Genen zeugt eine Inkonsistenz mit einer relativ hohen Rekombination zwischen den zwei Loci.[9] Außerdem konnten Cutting et al. im selben Jahr nachweisen, dass die zwei Gene innerhalb einer 340-kb-Region lokalisiert sind, wobei das 3′-Ende von COL4A2 und die 5′-Region von COL4A1 einen Abstand von mindestens 100 kb aufweisen, aber nicht mehr als 160 kb betragen kann.[10]
Im Jahr 1995 verwendete Koizumi et al. interspezifische und -subspezifische Mapping-Panels, um das COL4A1-Gen auf der centromeren Region des Chromosoms 8 einer Maus zu lokalisieren. Der Stuart-Prower-Faktor ist in der gleichen Region lokalisiert. Dementsprechend musste eine neue Homologie der Syntänie zwischen dem 8. Chromosom einer Maus und dem 13. Chromosom des Menschen definiert werden.[11]
Genstruktur
[Bearbeiten | Quelltext bearbeiten]COL4A1 und COL4A2 teilen sich einen gemeinsamen bidirektionalen Promoter[12] und die angrenzenden 5′-Regionen dieser beiden Gene überlappen sich.[13] COL4A1 beinhaltet insgesamt 52 codierende Exons.[14]
Proteinstruktur
[Bearbeiten | Quelltext bearbeiten]Mithilfe der Fouriertransformation-Ionenzyklotronresonanz-Massenspektrometrie und der Kernspinresonanzspektroskopie konnten die Bindungsverhältnisse des COL4A1-Proteins erläutert werden. Dabei konnte festgestellt werden, dass die Sulfimid-Bindung (–S=N–) die Aminosäuren Hydroxylysin-211 und Methionin-93 von angrenzenden Promotoren quervernetzt. Diese Bindung, das Stickstoff-Analogon eines Sulfoxids, entstand durch die Divergenz der Tierstämme der Schwämme und der Nesseltiere in Erwiderung auf die mechanische Belastung während der Metazoa-Evolution.[15] Außerdem besitzt das Protein eine N-terminale 7S-Domäne, eine Tripelhelix-formende kollagene Domäne und eine C-terminale nicht-kollagene Domäne.[16]
Funktion
[Bearbeiten | Quelltext bearbeiten]Es wirkt als Teil eines Heterotrimers und interagiert mit anderen extrazellulären Matrixkomponenten, wie z. B. Perlecan, Proteoglykane und Laminine. Außerdem führt eine proteolytische Spaltung einer nicht-kollagenen C-terminalen Domäne zu einem biologisch aktiven Fragment, welcher als Arresten bekannt ist, als Tumorsuppressor seine Verwendung findet und zur Antiangiogenese beiträgt.[16] Speziell inhibiert das Protein die endotheliale Zellproliferation und die Zellmigration. Außerdem hemmt es die Expression von HIF1A, ERK1/2 und die Aktivierung von p38 MAPK. Des Weiteren fungiert das Protein als Ligand für ITGA1 und ITB1.[1]
Interaktion
[Bearbeiten | Quelltext bearbeiten]Für die Bildung von α-Ketten des Kollagen kann COL4A1 mit zwei der anderen fünf Kollagen-IV-Proteinen interagieren. Diese sind:[1]
Klinische Signifikanz
[Bearbeiten | Quelltext bearbeiten]Mutationen im Gen COL4A1 könnten folgende Krankheiten verursachen:[17][18]
- Anfälligkeit einer intrazerebralen Hämorrhage (ICH)
- Familiäre autosomal-dominante Hämaturie
- Familiäre vaskuläre Leukenzephalopathie
- Familiäre Porenzephalie
- HANAC-Syndrom (Hereditäres Angiopathie-Nephropathie-Aneurysmen-Muskelkrampf-Syndrom)[19][20]
- Hereditäre Angiopathie mit Nephropathie, Aneurysmen und Muskelkrämpfen
- Schizenzephalie
- Small-Vessel-Krankheit des Gehirns mit oder ohne okulare Anomalien (BSVD)
- Tortuositas der retinalen Arterien
- Walker-Warburg-Syndrom
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c UniProt P02462
- ↑ Kollagen-Typ 4α1. In: GeneCards (englisch).
- ↑ E. Solomon, L. R. Hiorns, N. Spurr, M. Kurkinen, D. Barlow, B. L. M. Hogan, R. Dalgleish: Chromosomal assignments of the genes coding for human types II, III and IV collagen: a dispersed gene family. In: Proc Natl Acad Sci U S A. 82. Jahrgang, Nr. 10, Mai 1985, S. 3330–3334, PMID 2987919 (englisch, pnas.org [PDF]).
- ↑ T. Pihlajaniemi, K. Tryggvason, J. Myers, J. C., M. Kurkinen, R. Lebo, M.-C. Cheung, D. J. Prockop, C. D. Broyd: cDNA clones coding for the pro-alpha1(IV) chain of human type IV procollagen reveal an unusual homology of amino acid sequences in two halves of the carboxyl-terminal domain. In: J Biol Chem. 260. Jahrgang, Nr. 12, 25. Juni 1985, S. 7681–7687, PMID 2581969 (englisch, jbc.org [PDF]).
- ↑ C. D. Boyd, K. Weliky, S. Toth-Fejel, S. B. Deak, A. M. Christiano, J. W. Mackenzie, L. J. Sandell, K. Tryggvason, E. Magenis: The single copy gene coding for human alpha-1(IV) procollagen is located at the terminal end of the long arm of chromosome 13. In: Hum Genet. 74. Jahrgang, Nr. 2, Oktober 1986, S. 121–125, PMID 3770740.
- ↑ B. S. Emanuel, B. T. Sellinger, L. J. Gudas, J. C. Myers: Localization of the human procollagen alpha 1(IV) gene to chromosome 13q34 by in situ hybridization. In: Am J Hum Genet. 38. Jahrgang, Nr. 1, Januar 1986, S. 38–44, PMID 3753820.
- ↑ A. M. Bowcock, J. M. Hebert, A. M. Christiano, E. Wijsman, L. L. Cavalli-Sforza, C. D. Boyd: The pro alpha 1 (IV) collagen gene is linked to the D13S3 locus at the distal end of human chromosome 13q. In: Cytogenet Cell Genet. 45. Jahrgang, Nr. 3–4, 1987, S. 234–236, PMID 2891465.
- ↑ G. R. Cutting, H. H. Kazazian, Jr., S. E. Antonarakis, P. D. Killen, Y. Yamada, C. A. Francomano: Macrorestriction analysis maps COL4A1 and COL4A2 collagen genes within a 400 kb region on chromosome 13q34. (Abstract). In: Am. J. Hum. Genet. 41. Jahrgang, 1987.
- ↑ A. M. Bowcock, J. M. Hebert, E. Wijsman, I. Gadi, L. L. Cavalli-Sforza, C. D. Boyd: High recombination between two physically close human basement membrane collagen genes at the distal end of chromosome 13q. In: Proc Natl Acad Sci U S A. 85. Jahrgang, Nr. 8, April 1988, S. 2701–2705, PMID 2895928.
- ↑ G. R. Cutting, H. H. Kazazian, Jr., S. E. Antonarakis, P. D. Killen, Y. Yamada, C. A. Francomano: Macrorestriction mapping of COL4A1 and COL4A2 collagen genes on human chromosome 13q34. In: Genomics. 3. Jahrgang, Nr. 3, Oktober 1988, S. 256–263, PMID 3224982.
- ↑ T. Koizumi, E. Hendel, P. A. Lalley, M.-B. N. Tchetgen, J. H. Nadeau: Homologs of genes and anonymous loci on human chromosome 13 map to mouse chromosomes 8 and 14. In: Mammalian Genome. 6. Jahrgang, Nr. 4, April 1995, S. 263–268, PMID 7613031.
- ↑ E. Poschl, R. Pollner, K. Kuhn: The genes for the alpha 1(IV) and alpha 2(IV) chains of human basement membrane collagen type IV are arranged head-to-head and separated by a bidirectional promoter of unique structure. In: EMBO J. 7. Jahrgang, Nr. 9, September 1988, S. 2687–2695, PMID 2846280.
- ↑ R. Soininen, M. Huotari, S. L. Hostikka, D. J. Prockop, K. Tryggvason: The structural genes for alpha 1 and alpha 2 chains of human type IV collagen are divergently encoded on opposite DNA strands and have an overlapping promoter region. In: J Biol Chem. 263. Jahrgang, Nr. 33, 25. November 1988, S. 17217–17220, PMID 3182844.
- ↑ E. Plaisier, Z. Chen, F. Gekeler, S. Benhassine, K. Dahan, B. Marro S. Alamowitch, M. Paques, P. Ronco: Novel COL4A1 mutations associated with HANAC syndrome: a role for the triple helical CB3[IV] domain. In: Am J Med Genet A. 152A. Jahrgang, Nr. 10, Oktober 2010, S. 2550–2555, doi:10.1002/ajmg.a.33659, PMID 20818663.
- ↑ R. Vanacore, A.-J. L. Ham, M. Voehler, C. R. Sanders, T. P. Conrads, T. D. Veenstra, K. B. Sharpless, P. E. Dawson, B. G. Hudson: A sulfilimine bond identified in collagen IV. In: Science. 325. Jahrgang, Nr. 5945, 4. September 2009, S. 1230–1234, doi:10.1126/science.1176811, PMID 19729652 (sciencemag.org).
- ↑ a b GeneID 1282
- ↑ Kollagen-Typ 4α1. In: Online Mendelian Inheritance in Man. (englisch)
- ↑ Mutationen im Gen COL4A1. In: Orphanet. Abgerufen am 11. Juli 2016.
- ↑ Eintrag zu HANAC-Syndrom. In: Orphanet (Datenbank für seltene Krankheiten)
- ↑ Angiopathy, hereditary, with nephropathy, aneurysms, and muscle cramps. In: Online Mendelian Inheritance in Man. (englisch)