Metastabilität
Metastabilität in der Physik und der Chemie ist eine schwache Form der Stabilität. Ein metastabiler Zustand ist stabil gegen kleine Änderungen, jedoch instabil gegenüber größeren Änderungen. Das Compendium of Chemical Terminology (Gold Book) definiert Metastabilität als lokales Minimum der molaren Gibbs-Energie.[1]


Ein Beispiel dafür ist das System Holz und Luftsauerstoff bei Raumtemperatur: Aus thermodynamischer Sicht würde das spontane Verbrennen des darin chemisch gebundenen Kohlenstoffs mit dem Sauerstoff zu Kohlenstoffdioxid zu einem stabileren, energieärmeren Zustand führen. Bei Raumtemperatur findet die Reaktion aber nicht statt, sondern es muss zuerst eine gewisse Mindestenergie aufgebracht werden, bevor sich der Zustand des Systems ändert; zum Verbrennen muss das Holz zunächst auf die Zündtemperatur erwärmt werden. Beenden wir zuvor die Energiezufuhr, kühlt das Holz wieder ab und die Reaktion findet nicht statt.
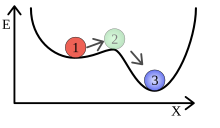
Anschaulich dargestellt ist das im Bild rechts: Ein Ball liegt in einer kleinen Mulde an einem Berghang. Solange der Ball nur wenig in der Mulde ausgelenkt wird, rollt er an ihre tiefste Stelle zurück. Diese stellt ein lokales Minimum der inneren Energie dar. Wird er aber stärker ausgelenkt, kann er den Berghang hinunterrollen und das nächste lokale Minimum erreichen.
Metastabile Phasen haben eine höhere Energie (korrekter: Freie Enthalpie – unter definierten Bedingungen wie konstanter Druck und konstante Temperatur) als die stabile Phase. Auf Grund einer hohen Aktivierungsenergie wandeln sie sich nicht oder nur langsam in die stabile Phase um.[2] Dieses energetische Grundprinzip metastabiler Zustände kann auch als Methode zur Energiespeicherung nutzbar gemacht werden,[3] wie es prinzipiell beispielsweise auch in Latentwärmespeicher speichern geschieht.
Ein Beispiel für eine metastabile Phase ist der Diamant, der sich bei Atmosphärendruck spontan in Graphit verwandeln sollte; die Geschwindigkeit dieses Vorgangs ist allerdings bei Zimmertemperatur verschwindend klein. Ein anderes Beispiel ist die Zinnpest: Die metallische Phase des Zinns wird unterhalb von 13 °C metastabil und wandelt sich langsam in die bei diesen Temperaturen stabilere nichtmetallische Phase um.[4] Weitere Beispiele sind unterkühltes Wasser, Amorphes Material wie Glas (der stabilste Zustand wären die kristallinen Silikate) und übersättigte Lösungen, die zum Beispiel in Handwärmern Verwendung finden.
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ IUPAC Gold Book metastability. International Union of Pure and Applied Chemistry, 2019, abgerufen am 5. Juni 2024 (englisch, https://doi.org/10.1351/goldbook.M03871).
- ↑ Claude H. P. Lupis: Chemical Thermodynamics of Materials. Elsevier, Amsterdam 1983, ISBN 0-444-00713-X.
- ↑ Zukunftskonzept elektrochemischer Energiespeicher. Webseite der Initiative Energiespeicher – Forschungsinitiative der Bundesregierung, 2. Mai 2016, abgerufen am 1. November 2017.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1005.