N-Methylharnstoff
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | N-Methylharnstoff | ||||||||||||||||||
| Andere Namen |
1-Methylharnstoff | ||||||||||||||||||
| Summenformel | C2H6N2O | ||||||||||||||||||
| Kurzbeschreibung |
geruchloser weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 74,08 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
N-Methylharnstoff ist eine chemische Verbindung aus der Gruppe der Harnstoffderivate.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]N-Methylharnstoff ist ein geruchloser weißer kristalliner Feststoff, der löslich in Wasser ist.[1]
Die Verbindung kristallisiert im orthorhombischen System mit der chiralen (also nicht-zentrosymmetrischen) Raumgruppe P212121 (Raumgruppen-Nr. 19).[3]
Darstellung
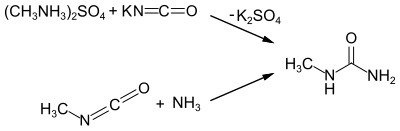
[Bearbeiten | Quelltext bearbeiten]Die Darstellung von N-Methylharnstoff wurde von Charles Adolphe Wurtz beschrieben. Durch Umsetzung von Methylammoniumsulfat[4] mit einer wässrigen Lösung Kaliumcyanat erhält man N‑Methylharnstoff und Kaliumsulfat. Eine weitere Möglichkeit der Darstellung ist die Umsetzung von Methylisocyanat mit Ammoniak.[5]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Durch Umsetzung von N-Methylharnstoff mit Benzil erhält man das substituierte Glycoluril-Derivat 2,8-Dimethyl-1,5-diphenylglycouril. Als Nebenprodukt entsteht das 2,6-Dimethyl-Isomer.[6]
Untersuchungen zum Abbau von Koffein durch Chlorierung zeigen, dass bei diesem Prozess N-Methylharnstoff als Abbauprodukt entsteht.[7]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Datenblatt N-Methylharnstoff bei Alfa Aesar, abgerufen am 4. Mai 2021 (Seite nicht mehr abrufbar).
- ↑ Eintrag zu N-Methylurea bei Toronto Research Chemicals, abgerufen am 4. Mai 2021 (PDF).
- ↑ G. Baaklini, G. Gbabode, S. Clevers, P. Négrier, D. Mondieig, G. Coquerel: Trimorphism of N-methylurea: crystal structures, phase transitions and thermodynamic stabilities. In: CrystEngComm. Band 18, Nr. 25, 2016, S. 4772–4778, doi:10.1039/C6CE00652C (archives-ouvertes.fr).
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Methylammoniumsulfat: CAS-Nr.: 33689-83-7, EG-Nr.: 251-636-2, ECHA-InfoCard: 100.046.928, PubChem: 198133, ChemSpider: 171489, Wikidata: Q82934832.
- ↑ Emil Erlenmeyer: Lehrbuch der organischen Chemie. C.F. Winter’sche Verlagshandlung, Leipzig 1883, S. 195 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ M. M. Antonova, V. V. Baranov, Yu. V. Nelyubina, A. N. Kravchenko: Regioselective Synthesis of 1,5-Diaryl-2-(Hydroxyalkyl)-8-Methylglycolurils. In: Chemistry of Heterocyclic Compounds. Band 50, Nr. 4, 2014, S. 503–513, doi:10.1007/s10593-014-1501-8.
- ↑ Ecotoxicological evaluation of caffeine and its derivatives from a simulated chlorination step. In: Science of The Total Environment. Band 470-471, 2014, S. 453–458, doi:10.1016/j.scitotenv.2013.10.005.