N-Oleoylsarcosin
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | N-Oleoylsarcosin | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C21H39NO3 | ||||||||||||||||||
| Kurzbeschreibung |
klare, schwach-gelbe bis rötlich-gelbe[2] bzw. gelb-braune[3] Flüssigkeit | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 353,54 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[3] | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt |
ca. −10 °C[3] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
N-Oleoylsarcosin (Sarkosyl O) ist ein amphiphiles Ölsäure-Derivat mit einer Sarkosin (N-Methylglycin)-Kopfgruppe, das als Wasser-in-Öl-Emulgator und Korrosionsinhibitor Verwendung findet.
Vorkommen und Darstellung
[Bearbeiten | Quelltext bearbeiten]Ein Standardverfahren zur Darstellung von N-Acylaminosäuren ist die Schotten-Baumann-Methode, bei der zu einer wässrigen Lösung von N-Methylglycin Oleoylchlorid (aus Ölsäure und z. B. Phosphortrichlorid) bei pH 10 (durch Zugabe von Natronlauge konstant gehalten) gegeben wird.[5]
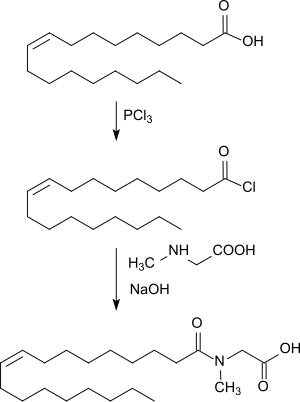
Dabei fällt weitgehend fettsäurefreies N-Oleoylsarcosin als Öl an. Die Methode eignet sich wegen der relativ teuren Herstellung der Carbonsäurechloride und dem Entsorgungsaufwand für die als Nebenprodukt anfallende Phosphonsäure nicht für eine industrielle Tensidsynthese.
N-Oleoylsarcosin wird bei der Reaktion von Ölsäure mit dem Natriumsalz des Sarkosins und Sarkosin bei 170 °C für 8 bis 10 Stunden unter Wasserabspaltung erhalten.[6]
Schonendere Bedingungen (120 °C) und kürzere Reaktionszeiten (3,5 Stunden) bietet die Umsetzung von Ölsäuremethylester (Methyloleat) mit Natriumsarkosinat unter Zugabe äquimolarer Mengen von Natriummethanolat in Methanol, wobei nach Aufnehmen in Wasser, Ansäuern mit konzentrierter Schwefelsäure und Extraktion mit Methylethylketon Sarkosyl O in 92,5%iger Ausbeute anfällt.[7]

Eigenschaften
[Bearbeiten | Quelltext bearbeiten]N-Oleoylsarcosin ist eine klare, gelbe bis braune, viskose Flüssigkeit, die in Wasser schwerlöslich ist und sauer reagiert. Als langkettige N-Acylaminosäure ist das Tensid in vielen organischen Lösungsmitteln und in Mineralöl löslich. Im Alkalischen löst es sich gut in Wasser. Wegen seiner Carbonsäureamid-Struktur ist Sarkosyl O auch bei hohen pH-Werten chemisch stabil und als anionisches Tensid stark schäumend. N-Oleylsarcosin ist wenig toxisch und leicht bioabbaubar.[8][6]
Anwendungen
[Bearbeiten | Quelltext bearbeiten]N-Oleoylsarcosin ist ein mildes Tensid, das Haut und Augen vergleichsweise wenig reizt und daher – zusammen mit anderen grenzflächenaktiven Substanzen – auch wegen seiner antimikrobiellen und viruziden Eigenschaften[9] in Körperpflegeprodukten, wie z. B. Hautreinigungsmitteln eingesetzt wird.
Die Sarcosin-Kopfgruppe der langkettigen amphiphilen N-Acylaminosäure ist für die Ausbildung chelatartiger Strukturen bei der Adsorption auf polare und geladene Oberflächen, z. B. von Metallen.[10]

Die Moleküle bilden orientierte monomolekulare Filme, die die Metalloberfläche vor korrosivem Angriff schützen.[8]
Sarkosyl O besitzt – insbesondere in Kombination mit dem ebenfalls emulgierend und antikorrosiv wirksamen Imidazolin-Derivat 2-(2-Heptadec-8-enyl-2-imidazolin-1-yl)ethanol (Amine® O der BASF SE) wird bereits bei niedrigen Konzentrationen (< 0,5 Gewichtsprozent) sehr gute Rostschutzeigenschaften, auch gegenüber Nichteisenmetallen, wie Aluminium und Kupfer.[4] Daher wird N-Oleoylsarcosin Rostschutzflüssigkeiten und Schmierfetten, Kraft- und Schmierstoffen, Kühlschmiermitteln, wie z. B. Bohr- und Schneidölen als Korrosionsinhibitor und Emulgator zugesetzt.[8]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu OLEOYL SARCOSINE in der CosIng-Datenbank der EU-Kommission, abgerufen am 20. April 2020.
- ↑ Eintrag zu N-Oleoylsarcosine bei TCI Europe, abgerufen am 17. Mai 2016.
- ↑ a b c d e f g h i j k Eintrag zu Oleylsarkosin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ a b Ciba Specialty Chemicals: Ciba Sarkosyl O: Oil soluble corrosion inhibitor ( vom 30. Mai 2016 im Internet Archive).
- ↑ Patent US3544606: Process for making sarcosines. Angemeldet am 21. Januar 1969, veröffentlicht am 1. Dezember 1970, Anmelder: W.R. Grace & Co., Erfinder: J.J. Singer, Jr..
- ↑ a b Patent US5710295: Preparation of alkali metal acyl amino acids. Angemeldet am 6. Juni 1995, veröffentlicht am 20. Januar 1998, Anmelder: Hampshire Chemical Corp., Erfinder: R.P. Woodbury, R.R. Gaudette, F.D. Wood.
- ↑ Patent US5856538: Preparation of N-acylamino carboxylic acids and N-acylamino sulfonic acids and their alkali metal salts. Angemeldet am 12. September 1995, veröffentlicht am 5. Januar 1999, Anmelder: BASF AG, Erfinder: R. Strecker, A. Oftring, D. Hertel, G. Schuh.
- ↑ a b c Schill+Seilacher, Amino Acid Based Surfactants, Perlastan®
- ↑ Chattem Chemicals, Inc., HAMPOSYL N-Acyl Sarcosinate Surfactants
- ↑ G.A. Salensky, M.G. Cobb, D.S. Everhart: Corrosion-inhibitor orientation on steel. In: Ind. Eng. Chem. Prod. Res. Dev. Band 25, Nr. 2, 1986, S. 133–140, doi:10.1021/i300022a002.


