Naphthalin-2-sulfonsäure
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
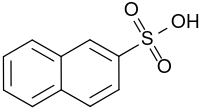
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Naphthalin-2-sulfonsäure | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C10H8O3S | |||||||||||||||||||||
| Kurzbeschreibung |
weißer bis schwach bräunlicher Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 208,24 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||||||||
| Dichte |
1,441 g·cm−3 (25 °C)[2] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
ca. 350,8 °C[1] | |||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Naphthalin-2-sulfonsäure ist eine chemische Verbindung aus der Gruppe der Naphthalinsulfonsäuren.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Naphthalin-2-sulfonsäure kann durch Reaktion von Naphthalin mit Schwefelsäure bei einer Temperatur von 170 °C gewonnen werden.[5] Über die Ausgangsverbindung steht die Naphthalin-2-sulfonsäure im Gleichgewicht mit der Naphthalin-1-sulfonsäure, wobei bei höherer Temperatur das 2-Isomer bevorzugt wird. Bei 160 °C liegt zu 15 % die Naphthalin-1- und zu 85 % die Naphthalin-2-sulfonsäure vor.[6] Das unerwünschte Isomer muss nachfolgend abgetrennt werden.[7][8] Naphthalin-2-sulfonsäure wird durch heiße wässrige Mineralsäuren viel schwieriger desulfoniert als Naphthalin-1-sulfonsäure. Die Geschwindigkeit wurde mit dem 50-fachen der Geschwindigkeit gemessen. Die Halogenierung greift entweder an der 5-Position oder an der 8-Stellung an. Speziell die Bromierung kann deshalb zur Trennung einer Mischung von Naphthalin-1-sulfonsäure von Naphthalin-2-sulfonsäure verwendet werden, da letztere ein lösliches Produkt bildet, während die erstere desulfoniert.[3]
Aus wässrigen Lösungen kristallisiert das Mono- oder Trihydrat aus.[3]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Naphthalin-2-sulfonsäure ist ein brennbarer, schwer entzündbarer, hygroskopischer, kristalliner, weißer bis schwach bräunlicher Feststoff, der leicht löslich in Wasser ist.[1][9]
Bei der Nitrierung entstehen vor allem die 5- und 8-Nitro-Derivate als Zwischenprodukte für die Cleve-Säuren (Aminonaphthalinsulfonsäuren nach Per Teodor Cleve[10]). Naphthalin-2-sulfonsäure kondensiert mit Formaldehyd oder Alkoholen zu oberflächenaktiven Stoffen. Das Zwischenprodukt 2-Thionaphthol kann durch katalytische Hydrierung von Naphthalin-2-sulfonsäure gewonnen werden, wird aber traditionell durch Reduktion von Naphthalin-2-sulfonylchlorid mit Zink hergestellt.[3]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Naphthalin-2-sulfonsäure wird als Zwischenprodukt zur Herstellung von Direktfarbstoffen, Reaktivfarbstoffen und Agrochemikalien verwendet.[4] Sie wird dabei als Ausgangsstoff zur Herstellung von 2-Naphthol verwendet. Ebenso wird sie zur Herstellung der 1,6-, 2,6- und 2,7-Disulfonsäuren sowie der 1,3,6-Trisulfonsäure eingesetzt.[3]
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i Eintrag zu Naphthalin-2-sulfonsäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 18. Februar 2022. (JavaScript erforderlich)
- ↑ a b c d David R. Lide: CRC Handbook of Chemistry and Physics, 85th Edition. CRC Press, 2004, ISBN 978-0-8493-0485-9 (books.google.com).
- ↑ a b c d e Gerald Booth: Ullmann's Encyclopedia of Industrial Chemistry. John Wiley & Sons, Ltd, 2000, ISBN 978-3-527-30673-2, Naphthalene Derivatives, doi:10.1002/14356007.a17_009.
- ↑ a b Datenblatt Naphthalene-2-sulfonic acid, 98% bei Alfa Aesar, abgerufen am 18. Februar 2022 (Seite nicht mehr abrufbar).
- ↑ Heinrich Wieland, Ludwig Gattermann: Die Praxis des organischen Chemikers. Walter de Gruyter, 2010, ISBN 978-3-11-085128-1, S. 249 (books.google.com).
- ↑ Hans Beyer, Wolfgang Walter: Lehrbuch der organischen Chemie. 18. Auflage. S. Hirzel Verlag, Stuttgart 1978, ISBN 3-7776-0342-2, S. 550 ff.
- ↑ Patent US2955134A: Separation of 1-naphthalene sulfonic acid from 2-naphthalene sulfonic acid. Angemeldet am 31. Dezember 1956, veröffentlicht am 4. Oktober 1960, Anmelder: American Cyanamid Co, Erfinder: Robert J. Tedeschi.
- ↑ Sniegoski, L. T., Edward, W. V., & Konash, P. L. (1982). Synthesis of 2-naphthalene-d7-sulfonic acid. Journal of Labelled Compounds and Radiopharmaceuticals, 19(9), 1081–1087. doi:10.1002/jlcr.2580190911
- ↑ Fengbao Zhang, Hui Jing, Wenyu Zhu, Lin Zhang, Bo Liu, Guoliang Zhang, Qing Xia: Solubilities of 2-naphthalenesulfonic acid monohydrate and sodium 2-naphthalenesulfonate in sulfuric acid solution and their application for preparing sodium 2-naphthalenesulfonate. In: Transactions of Tianjin University. Band 22, Nr. 3, 2016, S. 273–278, doi:10.1007/s12209-016-2714-y.
- ↑ Alexander Senning: Elsevier's Dictionary of Chemoetymology: The Whys and Whences of Chemical Nomenclature and Terminology. Elsevier, 2006, ISBN 978-0-08-048881-3 (books.google.com).

