Penicilline
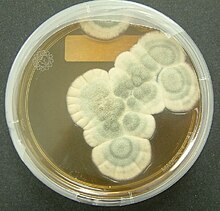
Die Penicilline (Singular: Penicillin, auch Penizillin; von lateinisch penicillium, ‚Pinselschimmel‘) sind eine Gruppe von antibiotisch wirksamen Substanzen, die sich strukturell von der 6-Aminopenicillansäure[1][2] ableiten. Neben natürlich vorkommenden Penicillinen, die als sekundäre Stoffwechselprodukte von verschiedenen Penicillium-, Aspergillus-, Trichophyton- und Streptomyces-Arten gebildet werden, zählt man dazu auch biosynthetisch und teilsynthetisch hergestellte Penicilline. Das zuerst entdeckte natürlich vorkommende Penicillin wurde aus der Pinselschimmelart Penicillium notatum isoliert und wurde ab 1942 therapeutisch eingesetzt.
Penicillin G, ein heute noch therapeutisch verwendetes natürliches Penicillin, gehört zu den ältesten verwendeten Antibiotika, dem neben seinem großen medizinischen Nutzen auch die Vorreiter-Rolle für die wissenschaftliche Verwendung dieser Wirkstoffgruppe zugeschrieben wird. Nach der Neuentdeckung der bereits 1874 von Theodor Billroth erkannten und publizierten antibiotischen Wirksamkeit von Penicillinen durch Alexander Fleming im Jahr 1928 wurde die enorme Bedeutung der Antibiotika für die Medizin erkannt, was das moderne Verständnis der Bedeutung bakterieller Krankheitserreger maßgeblich beeinflusst und revolutioniert hat. In den Jahrzehnten nach seiner Entdeckung trug Penicillin G zur Rettung unzähliger Menschenleben bei. Obwohl es heute zahlreiche Bakterienstämme gibt, die infolge unsachgemäßer Verwendung gegen dieses Antibiotikum resistent sind, kann es noch immer weltweit erfolgreich eingesetzt werden.
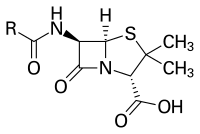
Penicilline gehören zur Gruppe der β-Lactam-Antibiotika. Die Summenformel lautet R-C9H11N2O4S, wobei „R“ für eine variable Seitenkette steht.
Einteilung
[Bearbeiten | Quelltext bearbeiten]Natürlich vorkommende Penicilline
[Bearbeiten | Quelltext bearbeiten]Die Muttersubstanz der Penicilline, die 6-Aminopenicillansäure, entsteht biologisch aus L-α-Aminoadipinsäure und den Aminosäuren L-Cystein und L-Valin, wobei zunächst Isopenicillin N gebildet wird. Durch den durch die Acyltransferase katalysierten Austausch des L-α-Aminoadipylrestes durch andere organische Säurereste entstehen verschiedene Penicilline. Von den natürlichen Penicillinen ist nur Penicillin G (Benzylpenicillin) therapeutisch bedeutsam, das fermentativ aus Penicillium chrysogenum gewonnen wird. Es wird nicht so rasch abgebaut wie das stärker wirksame Penicillin K. Unter Verwendung eines entsprechenden Präkursors, der Phenylessigsäure, lässt es sich zudem gezielt fermentativ herstellen. Neben Penicillium-Arten als biologische Produzenten werden Penicilline auch von anderen Schimmelpilzen wie Acremonium chrysogenum (ehemals Cephalosporium acremonium) und Aspergillus nidulans gebildet,[3] sowie von bestimmten Bakterien, die der Ordnung Actinomycetales angehören, beispielsweise produziert Streptomyces clavuligerus Penicillin N.[4]
 | |||||||
| Name | Weitere Namen | Aktivität | –R | Summenformel | Molare Masse | CAS-Nummer | PubChem |
|---|---|---|---|---|---|---|---|
| Penicillin F | Penicillin I, Penten(2)yl-penicillin | 1500 I.E./ml | –CH2–CH=CH–CH2–CH3 | C14H20N2O4S | 312,38 g·mol−1 | 118-53-6 | 6438232 |
| Penicillin G | Penicillin II, Benzylpenicillin | 1670 I.E./ml (Natriumsalz) | –CH2–C6H5 | C16H18N2O4S | 334,39 g·mol−1 | 61-33-6 | 5904 |
| Penicillin X | Penicillin III, p-Hydroxybenzylpenicillin | 850–900 I.E./ml | –CH2–C6H4–OH | C16H18N2O5S | 350,39 g·mol−1 | 525-91-7 | 120720 |
| Penicillin K | Penicillin IV, Heptylpenicillin | 2200 I.E./ml | –CH2–(CH2)5–CH3 | C16H25N2O4S | 341,45 g·mol−1 | 525-97-3 | 44123577 |
| Penicillin DF | Dihydropenicillin F, Penicillin H2F, Amylpenicillin | 1610 I.E./ml | –CH2–(CH2)3–CH3 | C14H22N2O4S | 314,40 g·mol−1 | 4493-18-9 | 107556 |
| Penicillin N | Adicillin | –(CH2)3–CH(NH2)–COOH | C14H21N3O6S | 359,40 g·mol−1 | 71724 | ||
| Penicillin M | Isopenicillin N | –(CH2)3–CH(NH2)–COOH | C14H21N3O6S | 359,40 g·mol−1 | 440723 | ||
Bio- und partialsynthetische Penicilline
[Bearbeiten | Quelltext bearbeiten]Das oral wirksame Penicillin V (Phenoxymethylpenicillin) entsteht ebenfalls fermentativ, aber nicht spontan, sondern durch Zusatz eines synthetischen Präkursors, der Phenoxyessigsäure („Biosynthese“).
Partialsynthetische Weiterentwicklungen der natürlichen Penicilline entstehen durch Umsetzung von 6-Aminopenicillinsäure mit Carbonsäurehalogeniden. Sie zeichnen sich gegenüber dem Penicillin G durch bestimmte Vorteile aus wie Säure- und Penicillinasestabilität oder ein erweitertes Wirkspektrum.
Säurestabile (oral wirksame) Penicilline ohne bzw. mit geringer Penicillinasestabilität
[Bearbeiten | Quelltext bearbeiten]- Phenoxymethylpenicillin (Penicillin V), Propicillin, Pheneticillin
Durch eine verminderte Nucleophilie des Carbonylsauerstoffs ist der Angriff von Hydronium-Ionen erschwert, wodurch die Umwandlung zur unwirksamen Penillsäure gehemmt wird. Säurestabile Penicilline werden also durch Magensäure nicht zerstört und können daher oral verabreicht werden. Sie haben das gleiche Wirkspektrum wie Penicillin G.
Penicillinasestabile Penicilline
[Bearbeiten | Quelltext bearbeiten]Durch Abschirmung des Betalactamringes mit Isoxazolylstrukturen gegenüber der von manchen Erregern gebildeten Penicillinase sind solche Penicilline auch wirksam gegen penicillinasebildende Staphylokokken („Staphylokokken-Penicillin“). Im Vergleich zu Penicillin G ist ihre Wirkstärke deutlich geringer und gegenüber gramnegativen Erregern sind Isoxazolylpenicilline gänzlich wirkungslos.
Breitspektrumpenicilline
[Bearbeiten | Quelltext bearbeiten]- Aminopenicilline: Amoxicillin, Ampicillin, Bacampicillin, Pivampicillin, Sultamicillin
- Carboxypenicilline: Carbenicillin, Ticarcillin
- Ureidopenicilline (Acylaminopenicilline): Azlocillin, Piperacillin, Mezlocillin
Durch die Einführung polarer Substituenten vermögen solche hydrophilen Penicilline die Zellwände von gramnegativen Erregern zu passieren, wodurch ihr Wirkspektrum erweitert wird. Die Breitspektrumpenicilline sind teilweise säure- und penicillinaseempfindlich, teilweise ist auch die Wirksamkeit gegenüber einigen grampositiven Bakterien vermindert.
Kein Acylierungsprodukt der 6-Aminopenicillansäure ist das Pivmecillinam, es besitzt jedoch das bicyclische Lactam-Grundgerüst der Penicilline.
Pharmakologie
[Bearbeiten | Quelltext bearbeiten]
Wirkungsmechanismus
[Bearbeiten | Quelltext bearbeiten]Penicilline wirken bei der Zellteilung von Bakterien bakteriolytisch, indem sie in die Neubildung der Zellwand eingreifen, dort die innere Vernetzung verhindern und damit die Zellwand so schwächen, dass diese bei Belastung platzt. Insbesondere grampositive Bakterien, die sich teilen, sterben unter Penicillineinfluss. Das Grundgerüst der Penicilline besteht aus 6-Aminopenicillansäure, einem bicyclischen Dipeptid aus Cystein (L-konfiguriert) und Valin (D-konfiguriert, nach Konfigurationsumkehr im Biosyntheseweg). Dieser sogenannte Beta-Lactam-Ring wird (im dann geöffneten Zustand) von dem bakteriellen Enzym D-Alanin-Transpeptidase gebunden, das für die Quervernetzung der Peptidoglykane in den bakteriellen Zellwänden grampositiver Bakterien zuständig ist. Das Enzym wird vor allem bei sich teilenden Bakterien benötigt, da bei diesen die starre Zellwand geöffnet und zumindest teilweise neu synthetisiert werden muss. Da die Bindung an die D-Alanin-Transpeptidase irreversibel ist, wird dieses Enzym funktionslos. Damit kann das Murein nicht mehr vernetzt und die Neubildung der Zellwand nicht abgeschlossen werden. Das grampositive Bakterium verliert somit den festigenden Schutz dieser Hülle. Daneben kommt es durch wiederholten Auf- und Abbau der defekten Zellwand zu toxischen Abbauprodukten.[5]
Die Wirkung der Penicilline trifft also sich vermehrende Bakterien, nicht aber solche, bei denen keine Zellwand-Neusynthese stattfinden muss. Ist die Zellwand bereits vollständig aufgebaut, so fehlt Penicillin ein Angriffspunkt. Sich nicht vermehrende Bakterien stellen für den Wirtsorganismus aber nur eine geringe Gefahr dar und können durch die körpereigene Immunabwehr leicht unschädlich gemacht werden.
Penicilline wirken nicht nur auf Bakterien, inklusive Cyanobakterien, sondern sie blockieren auch die Teilung der Cyanellen, der photosynthetisch aktiven Organellen der Glaucocystaceae (einer Algenfamilie) sowie der Chloroplasten von Blasenmützenmoosen.[6] Auf die Teilung der Plastiden der höher entwickelten Gefäßpflanzen wie beispielsweise bei Tomaten haben sie jedoch keinen Effekt. Dies ist ein Hinweis darauf, dass bei höheren Pflanzen durch erfolgte, evolutionäre Veränderungen der Plastidteilung β-Lactam-Antibiotika im Allgemeinen auf Chloroplasten keine Wirkung mehr zeigen.[6]
Penicillin G und V wirken nicht gegen gramnegative Bakterien (mit Ausnahme gramnegativer Kokken wie beispielsweise Neisserien), die über ihrer Zellmembran noch eine zusätzliche äußere Membran besitzen. Diese macht den Angriff des Penicillins unmöglich, da es in die Ausbildung der darunter liegenden Peptidoglycanschicht eingreifen muss. Daher ist der Einsatz von Penicillin G und V nur bei grampositiven Bakterien sinnvoll. Gegen gramnegative Bakterien werden strukturelle Varianten wie zum Beispiel Aminopenicilline eingesetzt.
Resistenzen
[Bearbeiten | Quelltext bearbeiten]Zahlreiche – aber nicht alle – klinisch vorkommende Bakterien sind heute bereits gegen Penicillin G resistent, was zu einer Reihe von weiterentwickelten β-Lactam-Antibiotika geführt hat. Eine Ausnahme ist etwa das Bakterium Treponema pallidum (Erreger der Syphilis/Lues), gegen das es bisher keine Resistenzentwicklung der Penicilline gab.[7]
Dabei bleibt das Problem der Kreuzresistenzen kritisch, was bedeutet, dass Keime, die einmal eine Resistenz gegen Penicilline entwickelt haben, auch gegen andere β-Lactam-Antibiotika (z. B. Cephalosporine) unempfindlich werden.
Resistente Mutanten würden eigentlich keinen Schaden anrichten, da sie nur in geringem Maße auftreten. Wirkt jedoch das Penicillin auf die anderen, nichtresistenten Bakterien und eliminiert diese, so kann sich ein resistentes Bakterium viel besser fortpflanzen und wird damit zur Gefahr, da es seine Resistenz an die Folgegenerationen weitervererbt. Durch den Austausch von Resistenzgenen zwischen verschiedenen Bakterienarten wird eine Antibiotikaresistenz auch auf andere Arten weitergetragen. Besonders gefürchtet ist die Methicillinresistenz bei Staphylococcus aureus.
Der Vorgang der Resistenzentwicklung ist ein sehr anschauliches Beispiel der darwinschen Evolutionstheorie (natürliche Selektion); aufgrund der raschen Teilung und Generationenfolge werden die an ihre Umwelt angepassten, resistenten Bakterien selektiert und bilden die Grundlage für spätere Generationen. Die Bildung von penicillinresistenten Stämmen gilt als einer der ersten experimentellen Beweise für beobachtete Mikroevolution. Biologische Grundlage der Wirkstoffgruppe ist die Konkurrenz zwischen den beiden Organismenstämmen Pilze und Bakterien, die auf dieselben Ressourcen angewiesen sind, wobei die Pilze sich mit antibakteriellen wachstumshemmenden Substanzen gegen die Bakterien schützen.
Nebenwirkungen
[Bearbeiten | Quelltext bearbeiten]Mit bis zu 10 % der Anwender häufig kommt es zu Hautausschlägen (Arzneimittelexanthem). Ebenso häufig lösen Penicilline Durchfälle durch Reizung der Darmschleimhaut aus. Weniger häufig können durch Penicilline nützliche Bakterien wie die der Darmflora abgetötet werden, insbesondere durch Breitbandpenicilline, die auch gegen gramnegative Bakterien wirken. Im ungünstigsten Fall können sich so schädliche Mikroorganismen im Darm ausbreiten und zu einer antibiotikaassoziierten Diarrhoe führen.[8]
Weit geringer als bisher angenommen ist die Häufigkeit einer Allergie gegen eine Penicillintherapie.[9] Die Allergietestung bei mehr als 90 Prozent jener Patienten, die angaben, eine Penicillinallergie zu haben, ergab, dass diese tatsächlich nicht vorliegt. Mit drei Fragen des PEN-FAST-Instruments kann ein Risikoscore ermittelt werden, der eine vermeintliche von einer echten Penicillinallergie mit hoher Wahrscheinlichkeit diskriminiert. Patienten mit niedrigem Risikoscore können wahrscheinlich ohne klinisch bedeutsames Risiko mit Penicillinen behandelt werden.[10] Allergische Reaktionen können dabei von leichter Hautrötung bis zum anaphylaktischen Schock reichen.
Eine weitere, mit einer Wahrscheinlichkeit von etwa drei Promille seltene unerwünschte Wirkung ist die Auslösung epileptischer Anfälle.[11]
Geschichte
[Bearbeiten | Quelltext bearbeiten]Entdeckung
[Bearbeiten | Quelltext bearbeiten]

Bereits 1874 hatte der Chirurg Theodor Billroth in Wien zweifelsfrei den das Wachstum von Bakterien hemmenden Effekt des Pilzes Penicillium erkannt.[12] Im Jahr 1923 erforschte in San José Clodomiro Picado Twight, ein ehemaliger Wissenschaftler des Institut Pasteur, die wachstumshemmende Wirkung auf Staphylokokken und Streptokokken. Seine Forschungsergebnisse wurden 1927 von der Société de biologie in Paris veröffentlicht.[13] Die weitaus öffentlichkeitswirksamere (Wieder-)Entdeckung der Penicilline begann mit einer verschimmelten Bakterienkultur ein Jahr darauf: Alexander Fleming, der sich am St. Mary’s Hospital in London mit Staphylokokken beschäftigte, hatte 1928 vor den Sommerferien eine Agarplatte mit Staphylokokken beimpft und dann beiseite gestellt. Bei seiner Rückkehr entdeckte er am 28. September 1928, dass auf dem Nährboden ein Schimmelpilz (Penicillium notatum) wuchs und sich in der Nachbarschaft des Pilzes die Bakterien nicht vermehrt hatten. Fleming nannte den bakterientötenden Stoff, der aus dem Nährmedium gewonnen werden konnte, Penicillin und beschrieb ihn für die Öffentlichkeit erstmals 1929 im British Journal of Experimental Pathology.[14] Er untersuchte die Wirkung des Penicillins auf unterschiedliche Bakterienarten und tierische Zellen; dabei stellte er fest, dass Penicillin nur grampositive Bakterien wie Staphylokokken, Streptokokken oder Pneumokokken abtötete, nicht aber gramnegative Bakterien wie beispielsweise Salmonellen. Auch gegenüber weißen Blutkörperchen und menschlichen Zellen oder für Kaninchen erwies es sich als ungiftig. Fleming kam trotz dieser Kenntnis offenbar nicht auf die Idee, Penicillin als Medikament einzusetzen.
Fast zehn Jahre später machten sich 1938 Howard W. Florey, Ernst B. Chain und Norman Heatley daran, systematisch alle von Mikroorganismen gebildeten Stoffe zu untersuchen, von denen bekannt war, dass sie Bakterien schädigten. So stießen sie auch auf Flemings Penicillin. Sie reinigten es und untersuchten seine therapeutische Wirkung zunächst an Mäusen und dann auch an Menschen. Im Jahre 1939 isolierte René Dubos vom Rockefeller Institute for Medical Research aus Bodenproben das Tyrothricin[15] und zeigte, dass es die Fähigkeit besaß, bestimmte bakterielle Infektionen zu heilen. Ende des Jahres 1940 erschien im Lancet der richtungsweisende Artikel „Penicillin als chemotherapeutischer Wirkstoff“ von Ernst Boris Chain und seinen Mitarbeitern.[16] Florey und Chain unternahmen 1941 in Oxford den ersten klinischen Test, der allerdings nur auf wenige Personen beschränkt war.[17] Da die Herstellung von Penicillin noch sehr mühsam war, gewannen sie es sogar aus dem Urin der behandelten Personen zurück.[18]
Mit Beginn des Zweiten Weltkriegs war den Alliierten daran gelegen, für ihre verwundeten Soldaten ein wirksames Medikament zu entwickeln. Die Antibiotika-Forschung verlagerte sich in die USA und nahm dort einen rasanten Verlauf. Man fand heraus, dass es günstiger ist, den Pilz in geeigneten flüssigen Nährmedien zu kultivieren. In den USA, wo bereits 1940 in geringem Umfang Penicillin zur Syphilis-Behandlung von Wehrpflichtigen produziert worden war,[19] züchtete man neue Stämme von Penicillium chrysogenum, die mehr Penicillin produzierten. Damit stand der Stoff als Medikament in der notwendigen Menge zur Verfügung. Erstmals bei Verwundeten eingesetzt wurde Penicillin 1942 bei den Alliierten.[20] 1943 stellte sich heraus, dass Penicillin keine chemisch einheitliche Substanz ist: So bestand das von den britischen Forschern mittels der oberflächlichen Fermentation (emerse Fermentation) gewonnene Rohpenicillin vor allem aus Penicillin F, das in den USA durch submerse Fermentation erzeugte Rohpenicillin im Wesentlichen aus Penicillin G. Früh erkannte man insgesamt vier Varianten,[21] die mit römischen Zahlen als Penicillin I, II, III und IV bzw. mit den Buchstaben F, G, X und K bezeichnet wurden.
1945 erhielten Fleming, Chain und Florey für ihre Entdeckung, die einen Wendepunkt in der Geschichte der Medizin markiert, gemeinsam den Nobelpreis.[22] Der Wirkstoff beendete das seit der Antike bestehende medizinische Problem, dass chirurgische Verletzungen aufgrund einfacher Wundinfektionen auch lange nach den Kriegshandlungen zum Tod der Betroffenen führen können, und wurde deshalb auch nach dem Krieg noch in der Bevölkerung als Wundermedizin angesehen. In Deutschland konzentrierte man sich auf die Weiterentwicklung der auch heute noch eingeschränkt gebräuchlichen Sulfonamide, da der Alliierte Kontrollrat die Nutzung von Penicillin weder in der Forschung noch in der medizinischen Anwendung erlaubt hatte. Erst 1946 gelangte ein Penicillinstamm unter letztlich ungeklärten Umständen zur Stolberger Firma Chemie Grünenthal, wo eine Produktion begonnen wurde. Allgemein erhältlich[23] wurde das zuvor importierte Penicillin in Deutschland erst nach 1949. Auch die Biochemie GmbH in Kundl (heute Sandoz[24]) war beteiligt an der Erforschung und Verbreitung von Penicillin. Im Jahr 1953 entdeckten dort die Chemiker Ernst Brandl und Hans Margreiter und der Pharmakologe Marco Giovannini das säurestabile Penicillin V (Phenoxymethylpenicillin) für die orale Therapie.[25][26][27]
Frühere Arbeiten
[Bearbeiten | Quelltext bearbeiten]Schon die Nubier verwendeten ein Bier mit antibakteriellen Wirkstoffen. Die Alten Ägypter versorgten Entzündungen mit aus Getreide gebrauten Heiltränken. In der Antike und im Mittelalter legten Chirurgen schimmelige Lappen auf Wunden, um Infektionen vorzubeugen. Die Wirkstoffe wurden jedoch nicht als solche erkannt, der Begriff des Antibiotikums wurde erst mit dem Penicillin eingeführt.
Fleming war jedoch nicht der erste neuzeitliche Wissenschaftler, der entdeckte, dass Schimmelpilze Bakterienwachstum hemmen können: Schon 1870 hatte John Scott Burdon-Sanderson einen Zusammenhang zwischen Schimmelpilzen und Bakterienwachstum erkannt. Im Jahr 1884 behandelte Joseph Lister den Abszess einer Krankenschwester mit einem Penicillium-Schimmelpilz (genauer: Penicillium glaucum), veröffentlichte die Ergebnisse jedoch nicht.[28] Ernest Duchesne führte 1896 einen erfolgreichen Tierversuch mit Meerschweinchen durch. Alle diese Erkenntnisse blieben jedoch ohne Resonanz in der wissenschaftlichen Welt und wurden völlig verkannt. Erst Fleming verwendete sicher das Penicillium notatum (welches Penicillin Burdon-Sanderson und Duchesne verwendeten, ist leider unbekannt).[29]
Entwicklung bis zum Durchbruch in der medizinischen Praxis
[Bearbeiten | Quelltext bearbeiten]Flemings Veröffentlichungen fanden zunächst bei Kollegen kaum Beachtung. Erst im Zweiten Weltkrieg erzielte das Penicillin den Durchbruch. Dabei spielte eine Rolle, dass die Sulfonamide, von denen ein Wirkstoff unter dem Handelsnamen Prontosil das erste praktisch eingesetzte Antibiotikum war, in Deutschland hergestellt und von deutschen Firmen patentiert waren, so dass sie für die Kriegsgegner nach Kriegsausbruch nicht mehr in der gleichen Weise verfügbar waren. Erst in der weiteren Forschung stellten sich die Vorzüge des Penicillin G gegenüber dieser Wirkstoffklasse heraus. Die Deutschen setzten jedoch bis Kriegsende weiterhin auf Sulfonamide.
Im Jahre 1939 interessierten sich Howard Walter Florey und Ernst Boris Chain für das Penicillin. Norman Heatley gelang es, das Antibiotikum aus der Kulturflüssigkeit, in der man die Schimmelpilze züchtete, zu extrahieren und zu reinigen. Am 24. August 1940 fand ein Tierversuch an 50 Ratten statt, die mit einer tödlichen Dosis Streptokokken infiziert wurden. Die Hälfte von ihnen erhielt Penicillin, und nur eine aus dieser Gruppe starb. Die Ratten der anderen Gruppe starben alle innerhalb weniger Stunden. Dieses Tierexperiment stellte überraschend die kraftvolle Wirkung des Penicillins heraus, die bei diesem aggressiven Bakterienstamm nicht erwartet wurde.
Am 12. Februar 1941 wurde der erste Patient mit dem gewonnenen Penicillin behandelt. Es handelte sich um den 43-jährigen Londoner Polizisten Albert Alexander, der sich beim Rosenschneiden verletzt und durch Infektion der Wunde eine Blutvergiftung erlitten hatte; ihm wurde eine Dosis von 160 Milligramm injiziert. Nach fünf Tagen Behandlung war das Fieber verschwunden, jedoch war der Penicillinvorrat aufgebraucht, weshalb die Behandlung abgebrochen werden musste. Der Patient starb am 15. März 1941.[30]
Dies ließ retrospektiv vermuten, dass das Penicillin hätte länger eingenommen werden müssen, als die sichtbaren Beschwerden andauern. Der erste Patient hätte nach heutigem Wissensstand fünf bis zehn Tage behandelt werden müssen.[30] Ein vorzeitiger Abbruch birgt immer das Risiko eines Krankheitsrückfalls, auch heute oftmals nur behandelbar durch Einsatz alternativer Antibiotika.
Erst als Florey und Heatley in die USA flogen, um dort für Penicillin zu werben, wurde das allgemeine Interesse geweckt, besonders beim amerikanischen Militär. Zunächst suchte man nach einem Pilzstamm, der mehr Penicillin produziert. Dazu sammelte die amerikanische Luftwaffe Bodenproben von möglichst vielen Flugplätzen weltweit. Der ergiebigste Stamm, Penicillium chrysogenum, wurde jedoch auf einer schimmligen Cantaloupe-Melone auf einem örtlichen Markt gefunden.[31]
Industrielle Produktion
[Bearbeiten | Quelltext bearbeiten]
Nachdem 1940 und 1941 der „Oxforder Kreis“ um E. B. Chain und H. W. Florey ein Verfahren zur Produktion und Isolierung von Penicillin in „Lancet“ veröffentlicht hatte, wurden ab 1942 die ersten industriellen Produktionen gestartet, allen voran durch Glaxo und ICI in England, MSD Sharp & Dohme (MSD), Pfizer & Co. und Squibb & Sons in den USA sowie Schott Jena (vorangetrieben durch Hans Knöll) in Deutschland.
Im Jahre 1943 stellten Pharmafirmen in den USA knapp 1,5 Tonnen reines Penicillin her, 1945 konnte die Produktion bereits auf über 400 Tonnen gesteigert werden.[30]
Ab 1942 wurde auch bei den Farbwerken Hoechst an Penicillin geforscht (die Produktion in kleinerem Maßstab begann dort im Frühjahr 1945[32]). Die Forscher mussten sich dabei auf die knappen Veröffentlichungen Flemings stützen. Hoechst hatte auch nicht den ergiebigen Chrysogenum-Stamm zur Verfügung. Eine Probe dieses Stamms schickte erst 1950 der US-Konzern MSD im Rahmen einer Zusammenarbeit nach Westdeutschland.
Parallel dazu forschte Robert Thren bei Madaus im sächsischen Radebeul an der Penicillinherstellung, aus der in Zusammenarbeit mit dem Chemiker Alfred Kuhn die ostdeutsche Produktion im Arzneimittelwerk Dresden hervorging. Vom Stammhaus des Pharmazeutischen Kombinats GERMED wurde der Ostblock beliefert.
Im Jahre 1945 war die in den USA produzierte Penicillinmenge 20-mal größer als die in Europa produzierte Menge.[33] Gewöhnlicher Mais, in Wasser eingeweicht, von den Amerikanern corn steep liquor genannt (Maisquellwasser), erwies sich als ideales Nährmedium für den Pilz. Dabei wurde (1944 bei Pfizer) das zunächst angewandte Oberflächenverfahren (Emerskultur) durch das Submersverfahren (Flüssigkultur im Rührkesselreaktor) abgelöst, mit dem höhere Produktivitäten erreicht wurden. Im Oktober 1944 wurden die ersten Injektionspräparate hergestellt. 1943 boten 22 Firmen Penicillin an.[34] Es blieb zunächst hauptsächlich verwundeten Soldaten vorbehalten, denn die Produktionsmenge reichte noch nicht aus, um auch alle zivilen Patienten damit zu behandeln. Seit 1944 waren die USA jedoch in der Lage, ihren gesamten zivilen und militärischen Bedarf an Penicillin zu decken. Hingegen war in Europa nach dem Zweiten Weltkrieg die Nachfrage groß und die Penicillinproduktion reichte hier nicht für alle Patienten. Es entwickelten sich Schmuggel und Schwarzhandel mit Penicillin, was auch Thema des Films Der dritte Mann ist.
In den 1950er Jahren vertrieb die Deutsche Novocillin-Gesellschaft mbH (München-Pasing), kurz DNG, Penicillin.[35][36] Zur „bakteriotropen“ Wirkungssteigerung wurde Penicillin zur Kombinationstherapie mit Streptomycin angeboten.[37] In den Jahrzehnten nach dem Zweiten Weltkrieg entwickelte sich die Nederlandsche Gist-en Spiritusfabrik (NG & SF), später Gist Brocades, heute DSM, zum weltgrößten Penicillinhersteller. Heute produziert die DSM Penicilline im Rahmen von Joint Ventures in der Volksrepublik China, während die Sandoz GmbH in Kundl (Österreich) heute den größten Produktionsstandort für Penicilline in der westlichen Welt betreibt.
Menschenversuche
[Bearbeiten | Quelltext bearbeiten]Literatur
[Bearbeiten | Quelltext bearbeiten]- Charles R. Cramer: Über Reinigung und Chemie der Penicilline, Zürich 1949, DNB 570057728 (Dissertation ETH-Zürich 1949, 106 Seiten).
- Christof Goddemeier: Alexander Fleming (1881–1955): Penicillin. In: Deutsches Ärzteblatt, Jahrgang 103, Nr. 36, 2006, S. A2286.
- Peter Imming: Wie macht der Pilz das Penicillin? Aktuelle Forschung, Trends bei β-Lactam-Antibiotika. Biosynthese der Penicilline und Cephalosporine. In: Pharmazie in unserer Zeit, Band 18, Nr. 1, 1989, S. 20–24, doi:10.1002/pauz.19890180104.
- Christian Mähr: Von Alkohol bis Zucker – Zwölf Substanzen, die die Welt veränderten. DuMont, Köln 2015, ISBN 978-3-8321-9549-6.
- Ingrid Pieroth: Penicillinherstellung: von den Anfängen bis zur Grossproduktion (= Heidelberger Schriften zur Pharmazie- und Naturwissenschaftsgeschichte, Band 9), Wissenschaftliche Verlagsgesellschaft, Stuttgart 1992, ISBN 3-8047-1248-7 (Dissertation Universität Regensburg 1991, 168 Seiten, unter dem Titel: Zur Geschichte der industriellen Penicillinherstellung von den Anfängen bis zum Aufbau der Grossproduktion).
- Vladimir Pliška: Penicillin und Suilfonamide im Kampf gegen Infektionen: zwischen Begeisterung und Skepsis = La penicilline et les sulfonamides dans la lutte contre les infections: benediction ou malédiction (= BioFokus, Jahrgang 24, Nr. 87), Verein Forschung für Leben, Zürich 2014, DNB 1049772873 (deutsch und französisch, Volltext (PDF; 1,6 MB) PDF, kostenfrei, 9 Seiten, 1,6 MB).
- Barbara I. Tshisuaka: Penizillin. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 1120.
- Susanne Krejsa MacManus: Penicillin aus Urin. In: Deutsche Apotheker Zeitung, 160. Jahrgang, Nr. 21, 21. Mai 2020, S. 71–74.
- Susanne Krejsa MacManus, Herwig Czech: Medikamentenversorgung Österreichs in Krisenzeiten. Am Beispiel Penizillin zwischen 1945 und 1949, in: Jahrbuch des Vereins für die Geschichte der Stadt Wien, 2022, ISSN 1027-8788, S. 61–116.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Biographie von Fleming (englisch)
- Nobelpreisrede von Fleming (PDF; 336 kB)
- Penicillin - Eine Erfolgsgeschichte mit Nebenwirkungen von Schweizer Radio und Fernsehen vom 27. Februar 2016 (Audio)
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ 6-Aminopenicillansäure ( vom 11. Mai 2015 im Internet Archive); Universität Hamburg, Department Chemie.
- ↑ Penicilline ( vom 24. April 2015 im Internet Archive): Bausteine u. Stoffwechselprodukte, Urban & Fischer 2003 – Roche Lexikon Medizin, 5. Aufl.
- ↑ Michael T. Madigan, John M. Martinko, Jack Parker: Brock Mikrobiologie. Deutsche Übersetzung herausgegeben von Werner Goebel, 1. Auflage. Spektrum Akademischer Verlag, Heidelberg/Berlin 2000, ISBN 3-8274-0566-1, S. 440–441.
- ↑ C. E. Higgens, R. E. Kastner: Streptomyces clavuligerus sp. nov., a β-Lactam Antibiotic Producer. In: International Journal of Systematic and Evolutionary Bacteriology. Band 21, Nummer 4, Oktober 1971, S. 326–331, doi:10.1099/00207713-21-4-326.
- ↑ H. Cho, T. Uehara, T. G. Bernhardt: Beta-lactam antibiotics induce a lethal malfunctioning of the bacterial cell wall synthesis machinery. In: Cell. Band 159, Nummer 6, Dezember 2014, S. 1300–1311, doi:10.1016/j.cell.2014.11.017. PMID 25480295.
- ↑ a b Britta Kasten, Ralf Reski: β-Lactam Antibiotics Inhibit Chloroplast Division in a Moss (Physcomitrella patens) but not in Tomato (Lycopersicon esculentum). In: J. Plant Physiol., 1997, 150, S. 137–140 (englisch); freier Volltextzugriff ( vom 4. Februar 2012 im Internet Archive; PDF)
- ↑ ÖÄZ v. 25. 2. 2021, S. 3.
- ↑ S2k-Leitlinie Gastrointestinale Infektionen. (PDF) Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS), November 2023, S. 64–65, abgerufen am 19. Oktober 2024.
- ↑ Erica S. Shenoy, Eric Macy, Theresa Rowe et al.: Evaluation and Management of Penicillin Allergy: A Review. PMID 30644987.
- ↑ Chang Su, Ami Belmont, Jane Liao, John K. Kuster, Jason A. Trubiano, Jason H. Kwah: Evaluating the PEN-FAST Clinical Decision-making Tool to Enhance Penicillin Allergy Delabeling. In: JAMA Internal Medicine. 20. Juni 2023, ISSN 2168-6106, doi:10.1001/jamainternmed.2023.1572.
- ↑ Epileptische Anfälle durch Antibiotika? (PDF) Schweizerische Epilepsie-Liga, 2016, abgerufen am 22. Oktober 2024.
- ↑ Ernst Kern: Echter und vermeintlicher Fortschritt in der Chirurgie. In: Würzburger medizinhistorische Mitteilungen. Band 9, 1991, S. 417–429, hier: S. 418.
- ↑ Dr. Clodomiro Picado Twight Honored with WIPO medal (PDF) In: WIPO Magazine, S. 11. Abgerufen am 2. März 2008
- ↑ A. Fleming: On the antibacterial action of cultures of a penicillium, with special reference to their use in the isolation of B. influenzæ. Br J Exp Pathol 10 (3): S. 226–236. (1929). PMC 2048009 (freier Volltext)
- ↑ H. L. Van Epps: René Dubos: unearthing antibiotics. In: Journal of Experimental Medicine (JEM), Band 203, 2006, S 259. doi:10.1084/jem.2032fta PMC 2118194 (freier Volltext)
- ↑ Alfred Marchionini, Hans Götz: Neuere Erfahrungen mit der antibiotischen Behandlung der Hautkrankheiten (Aureomycin, Chloromycetin, Terramycin). In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. 71–74, hier: S. 71.
- ↑ Jonathan Wood: Penicillin: the Oxford story. Oxford Science Blog, 16. Juli 2010.
- ↑ Alfred Marchionini, Hans Götz: Penicillinbehandlung der Hautkrankheiten. Springer-Verlag, Heidelberg 1950, S. 11 und 131.
- ↑ Florian G. Mildenberger: Kein Heil durch Arsen? Die Salvarsandebatte und ihre Konsequenzen. In: Fachprosaforschung – Grenzüberschreitungen, 8/9, 2012/2013, S. 327–390, hier: S. 365.
- ↑ Ernst Kern: Sehen – Denken – Handeln eines Chirurgen im 20. Jahrhundert. ecomed, Landsberg am Lech 2000, ISBN 3-609-20149-5, S. 298.
- ↑ Robert Bud: Penicillin – Triumph and Tragedy. Oxford University Press, 2007, S. 51 books.google.de
- ↑ Nobelpreis für Medizin 1945. nobelprize.org
- ↑ Ernst Kern: Sehen – Denken – Handeln eines Chirurgen im 20. Jahrhundert. ecomed, Landsberg am Lech 2000, ISBN 3-609-20149-5, S. 198.
- ↑ Penicillin als Tablette. Erinnerungen an eine Weltsensation. In: sandoz.at. 6. Oktober 2021, abgerufen am 27. Mai 2024.
- ↑ Zenab Helmy, A. W. El Borolossy: A Note on the Pharmacology of Phenoxymethyl-Penicillin (Penicillin V). In: Journal of pharmacy and pharmacology. 1956, Band 8, Nummer 1, S. 33–36 doi:10.1111/j.2042-7158.1956.tb12127.x.
- ↑ Ernst Brandl: Zur Entdeckungsgeschichte des Penicillin V in Kundl (Tirol). In: Veröffentlichungen des Tiroler Landesmuseums Ferdinandeum. Band 71, 1991, S. 5–16 (zobodat.at [PDF]).
- ↑ E. Brandl, M. Giovannini, H. Margreiter: [Studies on the acid stable, orally efficacious phenoxymethylpenicillin (penicillin V)]. In: Wiener medizinische Wochenschrift. Band 103, Nummer 33–34, August 1953, S. 602–607, PMID 13090756.
- ↑ Wer hat das Penicillin entdeckt – Fleming oder Lister? In: Ärzte Zeitung, 9. November 2004
- ↑ David Wootton: Bad Medicine. Doctors doing harm since Hippocrates. Oxford, S. 248.
- ↑ a b c Martin Winkelheide: Der lange Weg zum Antibiotikum. In: Kalenderblatt (Rundfunksendung auf DLF). 12. Februar 2021, abgerufen am 16. Februar 2021.
- ↑ David Greenwood: Antimicrobial Drugs: Chronicle of a Twentieth Century Medical Triumph. Oxford University Press, New York 2008, ISBN 978-0-19-953484-5, S. 106 (englisch).
- ↑ Florian G. Mildenberger (2012/13), S. 365.
- ↑ I. Pieroth: Penicillinherstellung. Von den Anfängen bis zur Großproduktion (Heidelberger Schriften zur Pharmazie- und Naturwissenschaftsgeschichte, Band 9). Wissenschaftliche Verlagsgesellschaft, Stuttgart 1992, ISBN 978-3-8047-1248-5.
- ↑ L. Marshall: Im Schatten der chemischen Synthese. Industrielle Biotechnologie in Deutschland (1900–1970). Campus Verlag, Frankfurt 2000, ISBN 3-593-36585-5.
- ↑ Markenzeichen der Heilmittelindustrie. Marken-Arzneimittel. In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. XXXVIII.
- ↑ Vgl. auch www.spiegel.de.
- ↑ Peni-Strept und Supracillin-E. In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. LXVI und LXIX.