Ruthenium(VI)-fluorid
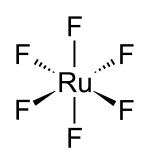
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Ruthenium(VI)-fluorid | ||||||||||||
| Andere Namen |
Rutheniumhexafluorid | ||||||||||||
| Summenformel | RuF6 | ||||||||||||
| Kurzbeschreibung |
dunkelbrauner kristalliner Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 215,07 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Dichte |
3,68 g·cm−3 (−140 °C)[2] | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Ruthenium(VI)-fluorid (RuF6), meist auch Rutheniumhexafluorid, ist eine chemische Verbindung der Elemente Ruthenium und Fluor und gehört zur Stoffgruppe der Hexafluoride.
Darstellung
[Bearbeiten | Quelltext bearbeiten]Rutheniumhexafluorid wird durch direkte Umsetzung des Metalls in einem Gasstrom von F2/Ar bei 400–450 °C dargestellt. Die Ausbeuten liegen unter 10 %.[2]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Rutheniumhexafluorid ist ein dunkelbrauner kristalliner Feststoff, der bei 54 °C schmilzt.[1] Es kristallisiert im orthorhombischen Kristallsystem (gemessen bei −140 °C) in der Raumgruppe Pnma (Nr. 62) mit den Gitterparametern a = 931,3 pm, b = 848,4 pm und c = 491,0 pm und vier Formeleinheiten pro Elementarzelle mit einer berechneten Dichte von 3,68 g·cm−3.[2] Das RuF6-Molekül ist oktaedrisch (Oh); die Ru–F-Bindungslänge beträgt 181,8 pm.[2]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Properties of the Elements and Inorganic Compounds, S. 4-86.
- ↑ a b c d T. Drews, J. Supeł, A. Hagenbach, K. Seppelt: "Solid State Molecular Structures of Transition Metal Hexafluorides", in: Inorganic Chemistry, 2006, 45 (9), S. 3782–3788; doi:10.1021/ic052029f; PMID 16634614.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
Literatur
[Bearbeiten | Quelltext bearbeiten]- Gmelins Handbuch der anorganischen Chemie, System Nr. 63, Ruthenium, Ergänzungsband, S. 266–268.
