Diffusionskoeffizient
Der Diffusionskoeffizient , auch Diffusionskonstante oder Diffusivität genannt, ist ein Transportkoeffizient und dient in den Fickschen Gesetzen zur Berechnung des thermisch bedingten Transports eines Stoffes aufgrund der zufälligen Bewegung der Teilchen. Dabei kann es sich um einzelne Atome in einem Feststoff oder um Teilchen in einem Gas oder einer Flüssigkeit handeln. Der Diffusionskoeffizient ist daher ein Maß für die Beweglichkeit der Teilchen und lässt sich nach der Einstein-Smoluchowski-Gleichung aus dem durchschnittlichen Quadrat der zurückgelegten Wegstrecke pro Zeit ermitteln:
- (oder alternativ mittels der Green-Kubo-Relationen).
Die SI-Einheit des Diffusionskoeffizienten ist daher . Zur Angabe des Diffusionskoeffizienten gehört immer die Angabe, welcher Stoff in welchem Stoff diffundiert, sowie als wichtigste Einflussgröße die Temperatur.
In Gasen
[Bearbeiten | Quelltext bearbeiten]| System | Temperatur in °C | Diffusionskoeffizient in m²/s |
|---|---|---|
| Luft – Sauerstoff | 0 | 1,76 × 10−5 |
| Luft – Kohlendioxid | 8,9 | 1,48 × 10−5 |
| 44,1 | 1,77 × 10−5 | |
| Wasserstoff – Stickstoff | 24,1 | 7,79 × 10−5 |
Diffusionskoeffizienten in Gasen[1][2] sind stark abhängig von Temperatur und Druck. In erster Näherung gilt, dass eine Verdopplung des Druckes zur Halbierung des Diffusionskoeffizienten führt.
Der Diffusionskoeffizient folgt gemäß der Chapman-Enskog-Theorie folgender Gleichung für zwei gasförmige Stoffe (Indizes 1 und 2):[3]
mit den physikalischen Größen
- – Diffusionskoeffizient
- N – Avogadro-Konstante
- M1,2 – molare Massen der Stoffe
- kB – Boltzmann-Konstante
- T – Temperatur
- p – Druck
- – (mittlerer) Kollisionsdurchmesser (Werte tabelliert[3])
- – Kollisionsintegral, abhängig von Temperatur und Stoffen (Werte tabelliert[3], Größenordnung: 1).
Für die Selbstdiffusion (d. h. für den Fall, dass nur eine Teilchensorte vorhanden ist) vereinfacht sich o. g. Zusammenhang zu:[4]
mit
- – mittlere thermische Geschwindigkeit der Teilchen
- l – mittlere freie Weglänge
- n – Teilchenzahldichte
- d – Teilchendurchmesser
- kB – Boltzmann-Konstante
- m – Molekülmasse
In Flüssigkeiten
[Bearbeiten | Quelltext bearbeiten]| Stoff | Diffusionskoeffizient in m²/s |
|---|---|
| Sauerstoff | 2,1 × 10−9 |
| Schwefelsäure | 1,73 × 10−9 |
| Ethanol | 0,84 × 10−9 |
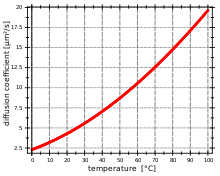
Diffusionskoeffizienten in Flüssigkeiten[1] betragen in der Regel etwa ein Zehntausendstel von Diffusionskoeffizienten in Gasen. Sie werden beschrieben durch die Stokes-Einstein-Gleichung:[5]
mit
- kB – Boltzmann-Konstante
- T – Temperatur
- η – dynamische Viskosität des Lösungsmittels
- R0 – hydrodynamischer Radius der diffundierenden Teilchen
Auf dieser Gleichung basieren viele empirische Korrelationen.
Da die Viskosität des Lösungsmittels eine Funktion der Temperatur ist, ist die Abhängigkeit des Diffusionskoeffizienten von der Temperatur nichtlinear.
In Feststoffen
[Bearbeiten | Quelltext bearbeiten]| System | Temperatur in °C | Diffusionskoeffizient in m²/s |
|---|---|---|
| Wasserstoff in Eisen | 10 | 1,66 × 10−13 |
| 50 | 11,4 × 10−13 | |
| 100 | 124 × 10−13 | |
| Kohlenstoff in Eisen | 800 | 15 × 10−13 |
| 1100 | 450 × 10−13 | |
| Gold in Blei | 285 | 0,46 × 10−13 |
Diffusionskoeffizienten in Feststoffen[1] sind in der Regel mehrere tausend Mal kleiner als Diffusionskoeffizienten in Flüssigkeiten.
Für die Diffusion in Festkörpern sind Sprünge zwischen verschiedenen Gitterplätzen erforderlich. Dabei müssen die Teilchen eine Energiebarriere E überwinden, was bei höherer Temperatur leichter möglich ist als bei niedrigerer. Dies wird beschrieben durch den Zusammenhang:[6]
mit
- E – Energiebarriere
- R – allgemeine Gaskonstante
- T – Temperatur.
D0 lässt sich näherungsweise berechnen als:
mit
- α0 – Atomabstand
- N – Anteil der vakanten Gitterplätze
- ω – Sprungfrequenz
Allerdings empfiehlt es sich, insbesondere Diffusionskoeffizienten in Feststoffen experimentell zu bestimmen.
Effektiver Diffusionskoeffizient
[Bearbeiten | Quelltext bearbeiten]Der effektive Diffusionskoeffizient[7] beschreibt Diffusion durch den Porenraum poröser Medien. Da er nicht einzelne Poren, sondern den gesamten Porenraum betrachtet, ist er eine makroskopische Größe:
mit
- εt – Porosität, die für den Transport zur Verfügung steht; sie entspricht der Gesamtporosität abzüglich Poren, die aufgrund ihrer Größe für die diffundierenden Teilchen nicht zugänglich sind, und abzüglich Sackgassen- und blinder Poren (Poren ohne Verbindung zum restlichen Porensystem)
- δ – Konstriktivität; sie beschreibt die Verlangsamung der Diffusion durch eine Erhöhung der Viskosität in engen Poren als Folge der größeren durchschnittlichen Nähe zur Porenwand und ist eine Funktion von Porendurchmesser und Größe der diffundierenden Teilchen.
- τ – Tortuosität („Gewundenheit“)
Scheinbarer Diffusionskoeffizient
[Bearbeiten | Quelltext bearbeiten]Der scheinbare (apparente) Diffusionskoeffizient[7] erweitert den effektiven Diffusionskoeffizienten um den Einfluss der Sorption.
Für lineare Sorption berechnet er sich zu:
mit
- Kd – linearer Sorptionskoeffizient
- ρ – Rohdichte
- ε – Porosität
Bei nichtlinearer Sorptionsisotherme ist der scheinbare Diffusionskoeffizient stets eine Funktion der Konzentration, was die Berechnung der Diffusion erheblich erschwert.
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c E. L. Cussler: Diffusion – Mass Transfer in Fluid Systems. Cambridge University Press, Cambridge/New York, 1997, ISBN 0-521-56477-8.
- ↑ T. R. Marrero, E. A. Mason: Gaseous Diffusion Coefficients. In: Journal of Physical and Chemical Reference Data. Band 1, Nr. 1, 1. Januar 1972, ISSN 0047-2689, S. 3–118, doi:10.1063/1.3253094 (nist.gov [PDF; abgerufen am 8. Oktober 2017]).
- ↑ a b c J. Hirschfelder, C. F. Curtiss, R. B. Bird: Molecular Theory of Gases and Liquids. Wiley, New York, 1954, ISBN 0-471-40065-3
- ↑ Franz Durst: Grundlagen der Strömungsmechanik: Eine Einführung in die Theorie der Strömung von Fluiden. Springer, Berlin, 2006, ISBN 3-540-31323-0.
- ↑ A. Einstein: Über die von der molekularkinetischen Theorie der Wärme geforderte Bewegung von in ruhenden Flüssigkeiten suspendierten Teilchen (PDF; 733 kB), Annalen der Physik. 17, 1905, S. 549ff.
- ↑ W. Jost: Diffusion in solids, liquids and gases. Academic Press Inc., New York, 1960.
- ↑ a b P. Grathwohl: Diffusion in natural porous media: Contaminant transport, sorption/desorption and dissolution kinetics. Kluwer Academic Publishers, 1998, ISBN 0-7923-8102-5.
















