Spirometrie

Die Spirometrie, heute mit bzw. als Spirographie, ist ein medizinisches Verfahren zur Messung und Aufzeichnung des Lungen- bzw. Atemvolumens und der Luftflussgeschwindigkeiten zur Beurteilung der Lungenfunktion. Die Spirometrie ist das am häufigsten eingesetzte Verfahren in der Pneumologie.
Dabei können das gesamte Lungenvolumen und einzelne Teile sowie seine Änderungen im Laufe des Atemzyklus bestimmt werden. Diese so genannten Ventilationsgrößen können z. B. mittels Spirometer gemessen werden.
Unterteilt wird die Spirometrie in Ruhe-Spirometrie und Ergo-Spirometrie (Spiroergometrie).
Geschichte
[Bearbeiten | Quelltext bearbeiten]→ Siehe Geschichte der Spiroergometrie
Aufbau und Funktionsweise
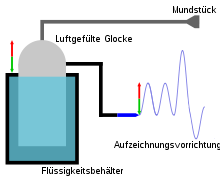
[Bearbeiten | Quelltext bearbeiten]Modellhaft beschrieben atmet die Person, deren Atemvolumina bestimmt werden sollen, über ein Mundstück-Schlauch-System in ein geschlossenes Behältnis ein und aus. Dieser Behälter ist frei höhenbeweglich, da er in einer Flüssigkeit wie z. B. Wasser schwimmt. Über ein System aus Umlenkrollen ist der Spirometrie-Behälter mit einem Schreibrekorder verbunden, der die Höhenänderung grafisch in Form des Spirogramms aufzeichnet. Um nicht zu viel Kohlenstoffdioxid nach erfolgter Exspiration zurückzuatmen und somit einer Hyperkapnie vorzubeugen, wird in der Regel ein Absorberbehälter (z. B. Natronkalkbehälter) in das Schlauchsystem eingebracht.
Durch den Atemvorgang ändert sich nun das Volumen im Spirometrie-Behälter. So wird bei der Exspiration (Ausatmung) Volumen aus der Lunge in den Behälter gepresst. Da Luft leichter als Wasser ist, steigt der Behälter auf. Die Rekordernadel senkt sich mittels der Umlenkung über das Rollensystem ab und es kommt zu einem negativen Ausschlag auf der Ordinate. Das Exspirationsvolumen fehlt nun der Lunge.
Umgekehrt wird bei der Inspiration (Einatmung) dem Spirometriebehälter Luft entzogen, er schwimmt somit nicht mehr so weit oben. Der Behälter sinkt also ab und über die Umlenkrollen schlägt die Rekordernadel nach oben hin aus. Die Lunge hat Volumen hinzugewonnen.
Moderne Spirometer messen in der Regel ausschließlich die Flussgeschwindigkeit und können dann über Aufintegration auf die Lungenvolumina schließen.
Am häufigsten werden folgende Techniken zur Messung des Atemflusses verwendet:
BTPS-Korrektur
[Bearbeiten | Quelltext bearbeiten]Um aus dem Atemfluss korrekt auf das Lungenvolumen zu schließen, müssen die Messwerte „BTPS“ korrigiert werden. BTPS-Bedingungen („body temperature, pressure, saturated with water vapor“) beschreiben die Bedingungen im Inneren des Körpers. Die Luft in der Lunge hat demnach Körpertemperatur (37 °C) und ist zu 100 % mit Wasser gesättigt. Bei der Ausatmung kühlt die Luft ab und verliert an Feuchtigkeit, wodurch das Spirometer geringere Volumina berechnet als eigentlich vorhanden sind. Hochwertige Spirometer müssen daher auch immer über eine Messung von mindestens Temperatur und im Idealfall auch Feuchtigkeit verfügen, um diesen Fehler korrigieren zu können.
Diagnostische Bedeutung
[Bearbeiten | Quelltext bearbeiten]Weichen Ventilationsgrößen in Ruhe von der jeweiligen Norm ab, kann dies auf Lungenerkrankungen hinweisen. Hierzu wird ein Vergleich mit Erwartungswerten durchgeführt. Patienten mit COPD und Asthmatiker unterziehen sich oft regelmäßig der Spirometrie zur Lungenfunktionsprüfung. Die Spiroergometrie wird vor allem zur Erfassung der körperlichen Leistungsfähigkeit durchgeführt.
Früherkennung
[Bearbeiten | Quelltext bearbeiten]Für Menschen mit Atembeschwerden ist die Spirometrie eine Kassenleistung. Für Menschen ohne Atembeschwerden ist sie eine Selbstzahlerleistung (IGeL). Ob die Untersuchung in diesem Fall nutzt oder schadet, hat 2017 der IGeL-Monitor des MDS (Medizinischer Dienst des Spitzenverbandes Bund der Krankenkassen) untersucht und die Spirometrie zur Überprüfung der Lungenfunktion mit „tendenziell negativ“ bewertet.[1] Denn die Wissenschaftler fanden keine Studien zu Nutzen oder Schaden der Spirometrie bei Menschen ohne Beschwerden. Wichtigste Quellen sind zwei Übersichtsarbeiten.[2] Es sei unklar, so der IGeL-Monitor, ob man mehr Lebenszeit oder mehr Lebensqualität gewinnt, wenn Asthma oder COPD früh erkannt und behandelt werden. Es gebe aber Hinweise auf Schäden, da durch Früherkennung Krankheiten behandelt werden können, die keine Probleme bereitet hätten.[3] Auch vier internationale, hochwertige Leitlinien empfehlen die Spirometrie nicht zur Früherkennung oder raten sogar davon ab.[4]
Messparameter
[Bearbeiten | Quelltext bearbeiten]Die wichtigsten Parameter sind:
- Flussparameter
- Einsekundenkapazität (FEV1)
- Peak Flow (PEF)
- Volumenparameter
- Vitalkapazität (VC) und forcierte Vitalkapazität (FVC)
- Atemzugvolumen (AZV)
- inspiratorisches Reservevolumen (IRV), beschreibt das Volumen, das nach normaler Inspiration noch zusätzlich eingeatmet werden kann
- exspiratorisches Reservevolumen (ERV), beschreibt das Volumen, das nach normaler Exspiration noch ausgeatmet werden kann
- FEV1% (Quotient von FEV1 und FVC)
Aus der Amplitude des inspiratorischen und exspiratorischen Volumens errechnet sich die Vitalkapazität. Residualvolumen (RV), also die Luftmenge, welche nach maximaler Ausatmung noch in der Lunge verbleibt und die totale Lungenkapazität (TLC) können mit der Spirometrie nicht bestimmt werden. Hierzu muss ein Bodyplethysmograph verwendet werden.
Ablauf
[Bearbeiten | Quelltext bearbeiten]Während der Untersuchung wird der Tiffeneau- oder FVC-Test durchgeführt. Hierbei atmet der Patient zunächst so tief aus wie möglich. Danach folgt eine maximal mögliche und zügige Einatmung, woraufhin der Patient so schnell, stark und wieder maximal ausatmet, wie es ihm möglich ist. Die Nasenatmung wird durch eine aufgesetzte Klammer unterbunden.
Während der Messung stellt die Software des Spirometers das Spirogramm dar. Dafür wird das geatmete Volumen über der Zeit aufgetragen, sowie eine Fluss-Volumen-Kurve erstellt, in der die Geschwindigkeit der Luft über dem geatmeten Volumen dargestellt wird.
-
Diagramm Atemvolumen über Zeit, mit Erklärung der Parameter
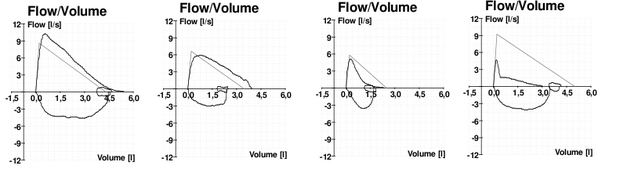
Bei forcierter Ausatmung bei gesunden Menschen steigt der Fluss zunächst sehr stark auf den Maximalwert (PEF) an und sinkt dann langsamer linear auf 0 l/s ab, bis die forcierte Vitalkapazität (FVC, maximal ausgeatmetes Volumen, im Beispieldiagramm bei 4,5 l) erreicht ist. Die Kurve über der y-Achse bildet dadurch ein nach Dreieck mit stark nach links verschobener Spitze. Die Kurve unter der y-Achse bildet bei normaler Einatmung eine halbrunde Form. Die beiden Kurven umfassen dasselbe Volumen auf der x-Achse und treffen sich jeweils am Ende auf der y-Achse. Ein zusätzlicher kleiner Kreis (hier um die 4,5-Liter-Marke herum) bildet die normale Atmung des Patienten ab (Atemzugvolumen). Die normale Fluss-Volumen-Kurve bei guter Mitarbeit des Patienten, abhängig von Alter, Größe und Geschlecht, wird in den Beispielen oben zusätzlich durch eine dünne Linie dargestellt.
Es ist anhand des etwas komplexen Manövers ersichtlich, dass der Erfolg der Untersuchung auch von der Motivation und Mitarbeit des Patienten abhängt. Der Patient sollte vor der Untersuchung klar instruiert werden. Zudem sollte die Untersuchung wiederholt werden und die Parameter sollten bei guter Mitarbeit nicht mehr als 5 % voneinander abweichen. Mitarbeitsunabhängige Methoden wie die Oszillometrie sind in der Praxis nur selten verbreitet. Im zweiten Beispiel-Diagramm oben ist zu sehen, dass die Kurven für Ein- und Ausatmung nicht dasselbe Volumen abbilden; der Patient hat entweder nicht tief genug ein- oder nicht genug ausgeatmet. In diesem Beispiel ist außerdem der maximale Fluss gegenüber der Normalkurve stark verringert, und die Kurve um den Maximalwert abgeflacht; die Ausatmung fand nicht stark genug statt.
Die Beispiel-Diagramme für Asthma und COPD sind gekennzeichnet durch einen nach dem Maximalwert (PEF) stark abfallenden Fluss (Abflachung der Kurve). Das letzte Diagramm zeigt eine starke Obstruktion (gegenüber dem Normalwert verringerter PEF sowie starker Abfall danach, Knickbildung), sowie zusätzlich eine verringerte forcierte Vitalkapazität (FVC).
Ebenso ist im Falle von COPD der PEF-Wert gegenüber der normalen Atmung verringert. Der Fluss fällt nach Erreichen des Maximums durch die Obstruktion sehr stark ab.
Literatur
[Bearbeiten | Quelltext bearbeiten]- Robert E. Hyatt u. a.: Interpretation of Pulmonary Function Tests: A Practical Guide. 4. Auflage. Wolters Kluwer, Philadelphia 2014, ISBN 978-1-4511-4380-5.
- S2k-Leitlinie Spirometrie der Deutschen Gesellschaft für Pneumologie und Beatmungsmedizin (DGP). In: AWMF online (Stand 2015)
- Deutsche Atemwegsliga: Abbildungen Spirometrie
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Spirometrie auf Vimeo (Untersuchungsablauf / Deutsche Atemwegsliga e. V.)
- Empfehlungen der Deutschen Atemwegsliga zur Spirometrie Erscheinungsjahr: 2006 (PDF; 1,1 MB)
- Martin Bösch, Martin Thalmann: Praxis-Website
- Dynamic Measurement Technologies: Online-Rechner zur Berechnung des BTPS-Korrekturfaktors, altersspezifischer Erwartungswerte und weitere Berechnungen.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ IGeL-Monitor: Spirometrie zur Überprüfung der Lungenfunktion, abgerufen am 14. März 2019. Mehr zur Begründung der Bewertung in „Evidenz ausführlich“, abgerufen am 14. März 2019.
- ↑ Eisenmann et al.: Effektivität eines COPD-Screenings mittels Spirometrie, Quick Assessment, 2010, sowie Guirguis-Blake et al.: Screening for chronic obstructive pulmonary disease: A systematic Evidence Review for the U.S. Preventive Service Task Force, 2016, Agency for Healthcare Research and Quality; Evidence Synthesis Number 130; AHRQ Publication No. 14-05205-EF-1. 2016
- ↑ Süddeutsche Zeitung, Viele Selbstzahler-Gesundheitsleistungen bringen mehr Schaden als Nutzen, 16. Februar 2017.
- ↑ 1.: US Preventive Services Task Force (USPSTF), Siu, A.L. et al. Screening for Chronic Obstructive Pulmonary Disease: US Preventive Services Task Force Recommendation Statement. Jama, 2016; 315 (13): 1372-137. 2.: American College of Physicians, American College of Chest Physicians, American Thoracic Society, and European Respiratory Society. Diagnosis and Management of Stable Chronic Obstructive Pulmonary Disease, 2011. 3.: Global initiative for Chronic Obstructive Lung Disease (GOLD). Global Strategy for the Diagnosis, Management and Prevention of Chronic Obstructive Pulmonary Disease. 2016. 4.: The Royal Australian College of General Practitioners (RACGP). Guidelines for preventive activities in general practice. 2012. Auflistung auch in „Evidenz ausführlich“, S. 21f