Suberonitril
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
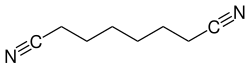
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Suberonitril | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H12N2 | ||||||||||||||||||
| Kurzbeschreibung |
farblos bis gelbliche Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 136,20 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
0,954 g·cm−3 (25 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
schwer löslich in Wasser[1] | ||||||||||||||||||
| Brechungsindex |
1,4436 (20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Suberonitril ist eine organisch-chemische Verbindung aus der Stoffgruppe der Nitrile.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Suberonitril wird kommerziell meist aus Korksäure und Ammoniak bei erhöhten Temperaturen und in Gegenwart eines Trockenmittels (z. B. Phosphorpentoxid) gewonnen.[3]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Korksäuredinitril hat eine relative Gasdichte von 4,7 (Dichteverhältnis zu trockener Luft bei gleicher Temperatur und gleichem Druck).[1]
Chemische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Suberonitril ist eine brennbare, jedoch schwer entzündbare Flüssigkeit aus der Stoffgruppe der Nitrile. Die schwer flüchtige Verbindung ist schwer löslich in Wasser. Eine Lösung der Konzentration 10 g/l besitzt bei 20 °C einen pH-Wert von 8,4–8,8.[1]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Suberonitril findet aufgrund seiner Bifunktionalität als Nitril Anwendung, insbesondere bei der Herstellung von Pflanzenschutzmitteln (zum Beispiel über das Zwischenprodukt 1,8-Diaminooctan).[4][5]
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Die Hauptaufnahmewege von Suberonitril beschränken sich hauptsächlich auf die Atemwege und die Haut. Bei Aufnahme oder Verschlucken kann es akut zu (auch neurologischen) Herz-Kreislauf-Störungen kommen. Oft treten dabei Hypoxie oder Atemfunktionsstörungen auf. Bei direkten Kontakt mit der reinen Flüssigkeit sind leichte Augenreizungen bei geringer bis fehlender Hautreizung möglich. Chronisch und bei wiederholtem Kontakt sind Hautirritationen möglich. Ansonsten sind keine ausreichenden Angaben für den Menschen vorhanden. Zur Reproduktionstoxizität, Kanzerogenität sowie Mutagenität sind ebenfalls keine substanzspezifischen Informationen vorhanden. Suberonitril weist eine untere Explosionsgrenze (UEG) von ca. 8,5 Vol.-% und eine obere Explosionsgrenze (OEG) von ca. 29 Vol.-% auf. Die Zündtemperatur beträgt ca. 460 °C. Der Stoff fällt somit in die Temperaturklasse T1 und in die Explosionsgruppe IIA. Mit einem Flammpunkt von 110 °C gilt Suberonitril als schwer entflammbar.[1]
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j k l m Eintrag zu Suberonitril in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. April 2021. (JavaScript erforderlich)
- ↑ W. M. Haynes (Hrsg.): CRC Handbook of Chemistry and Physics. 97. Auflage. (Internet-Version: 2016), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-426.
- ↑ Patent CN105001033A: Manufacturing method for nitrile and corresponding amine thereof. Veröffentlicht am 28. Oktober 2015, Anmelder: China Petroleum & Chemical Corporation, SINOPEC Yangzi Petrochemical Company Ltd., Erfinder: Bai Jiye, Chen Shaohui, Chen Xinhua, Gao Yilong, Kan Lin, Li Na, Miao Jun, Sun Hailong, Wei Yanyu, Xu Yuexing, Yang Aiwu.
- ↑ Ullmann's Fine Chemicals. Wiley, 2014, ISBN 978-3-527-68359-8, S. 176-IA2 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Ronny Neumann, Y. Sasson: Handbook of Phase Transfer Catalysis. Springer Netherlands, 2012, ISBN 978-94-009-0023-3, S. 185 (eingeschränkte Vorschau in der Google-Buchsuche).
